1 . Ⅰ.25℃时,0.1 mol/L的HA溶液中 =1010,0.01 mol/L的BOH溶液pH=12。
=1010,0.01 mol/L的BOH溶液pH=12。
(1)BOH是_____ (填“强电解质”或“弱电解质”),HA的电离方程式是____
(2)在加水稀释HA的过程中,随着水量的增加而减小的是_____ (填字母)。
A.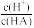 B.
B.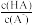 C.c(H+)与c(OH—)的乘积 D.c(OH—)
C.c(H+)与c(OH—)的乘积 D.c(OH—)
(3)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体____ (填“多”、“少”或“相等”)。
Ⅱ.在25 ℃时,请进行有关计算(假定溶液体积有加和性)
(4)现有pH=2的HCl溶液100 mL,要使它的pH=3,如果加入蒸馏水,需要____ mL。 如果加入pH=4的HCl溶液,需加入此HCl溶液____ mL。
(5)pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性,已知a+b=15,则X:Y=_____ 。
 =1010,0.01 mol/L的BOH溶液pH=12。
=1010,0.01 mol/L的BOH溶液pH=12。(1)BOH是
(2)在加水稀释HA的过程中,随着水量的增加而减小的是
A.
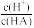 B.
B.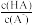 C.c(H+)与c(OH—)的乘积 D.c(OH—)
C.c(H+)与c(OH—)的乘积 D.c(OH—)(3)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体
Ⅱ.在25 ℃时,请进行有关计算(假定溶液体积有加和性)
(4)现有pH=2的HCl溶液100 mL,要使它的pH=3,如果加入蒸馏水,需要
(5)pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性,已知a+b=15,则X:Y=
您最近一年使用:0次
2021-05-09更新
|
673次组卷
|
2卷引用:四川省阆中中学2020-2021学年高二下学期期中教学质量检测化学试题
2 . 按要求填空:
(1)相对分子质量为72的烷烃的分子式为___________ ,结构有___________ 种,分别写出它们的结构简式___________ 。
(2)下列物质熔沸点由高到低的顺序是:①CH4;②C3H8;③CH3CH(CH3)2 ;④CH3CH2CH2CH3;___________ (填序号)
(3)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式___________ 。
(4)已知:①Fe(s)+ O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
②2Al(s)+ O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
Al和FeO发生反应的热化学方程式是___________ 。
(1)相对分子质量为72的烷烃的分子式为
(2)下列物质熔沸点由高到低的顺序是:①CH4;②C3H8;③CH3CH(CH3)2 ;④CH3CH2CH2CH3;
(3)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式
(4)已知:①Fe(s)+
 O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1②2Al(s)+
 O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1Al和FeO发生反应的热化学方程式是
您最近一年使用:0次
名校
解题方法
3 . 25.6g铜投入一定浓度的硝酸溶液中,铜完全溶解,共收集到NO和NO2的混合气体8.96L气体(标准状况)。
(1)计算产生NO和NO2的物质的量分别为多少mol?___________ (请写出计算过程)
(2)将盛有此混合气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为___________ L。
(3)向100mL0.7mol•L-1硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反应后,放出标准状况下的气体224mL(假设该气体全部为NO),且测得溶液中铁只以Fe2+形式存在,为使Fe2+完全沉淀,可向反应后的溶液中加入1mol•L-1的NaOH___________ mL
(1)计算产生NO和NO2的物质的量分别为多少mol?
(2)将盛有此混合气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为
(3)向100mL0.7mol•L-1硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反应后,放出标准状况下的气体224mL(假设该气体全部为NO),且测得溶液中铁只以Fe2+形式存在,为使Fe2+完全沉淀,可向反应后的溶液中加入1mol•L-1的NaOH
您最近一年使用:0次
2021-04-23更新
|
549次组卷
|
2卷引用:四川省绵阳东辰国际学校2020-2021学年高一下学期第一次月考化学试题
名校
解题方法
4 . 叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。
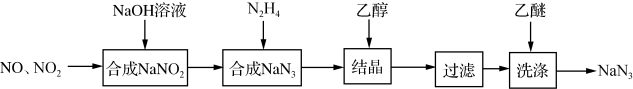
(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式___ ,生成1molNaNO2时转移电子___ mol。
(2)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3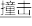 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
①该反应中的氧化剂为___ ,还原剂为___ (填化学式)。
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___ ?(写出计算过程,保留一位小数,不考虑固体的体积)。

(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式
(2)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
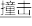 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。①该反应中的氧化剂为
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
您最近一年使用:0次
名校
5 . 请回答下列问题(注意:溶液混合时,均忽略溶液体积变化):
(1)已知:常温下HCN的Ka=4.9×10−10,H2CO3的Ka1=4×10−7,Ka2=5.6×10−11,写出将少量CO2气体通入NaCN溶液中的离子方程式______ 。
(2)25℃时,pH=2的盐酸溶液与pH=4的H2SO4溶液等体积混合,求混合后的pH=______ 。
(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为______ 。
(4)常温下,将0.1mol·L-1氢氧化钠溶液与0.06mol·L-1硫酸溶液等体积混合,溶液的pH=______ ;
(5)25℃时,pH=5的H2SO4溶液加水稀释至原溶液体积的1000倍,求稀释后的溶液中离子浓度比c(H+):c(SO )=
)=______ 。
(6)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于______ 。
(1)已知:常温下HCN的Ka=4.9×10−10,H2CO3的Ka1=4×10−7,Ka2=5.6×10−11,写出将少量CO2气体通入NaCN溶液中的离子方程式
(2)25℃时,pH=2的盐酸溶液与pH=4的H2SO4溶液等体积混合,求混合后的pH=
(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为
(4)常温下,将0.1mol·L-1氢氧化钠溶液与0.06mol·L-1硫酸溶液等体积混合,溶液的pH=
(5)25℃时,pH=5的H2SO4溶液加水稀释至原溶液体积的1000倍,求稀释后的溶液中离子浓度比c(H+):c(SO
 )=
)=(6)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于
您最近一年使用:0次
6 . 下图是氮气及几种氮的化合物间的转换关系。请回答下列问题:

(1)请写出工业合成氨的化学方程式_______ 。
(2)工业上常用NH3制取NO,请写出反应的化学方程式_______ 。
(3)实验室里常用Cu与稀硝酸反应制取NO,当生成标准状况下3.36LNO时,转移的电子数为_______ 。
(4)生产硝酸时排放的NO会污染环境,一种治理方案是用氨气在催化剂作用下将NO还原成N2,请写出化学方程式:_______ 。
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为_______ L。

(1)请写出工业合成氨的化学方程式
(2)工业上常用NH3制取NO,请写出反应的化学方程式
(3)实验室里常用Cu与稀硝酸反应制取NO,当生成标准状况下3.36LNO时,转移的电子数为
(4)生产硝酸时排放的NO会污染环境,一种治理方案是用氨气在催化剂作用下将NO还原成N2,请写出化学方程式:
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
您最近一年使用:0次
名校
7 . (1)将 铜镁合金与足量稀硝酸完全反应,放出
铜镁合金与足量稀硝酸完全反应,放出 气体(标况下),转移电子数为
气体(标况下),转移电子数为___________ ,向反应后的溶液中加入 溶液至完全沉淀,得到沉淀的质量为
溶液至完全沉淀,得到沉淀的质量为___________ 。
(2)将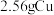 放入
放入 浓
浓 中正好完全反应。随着
中正好完全反应。随着 的不断减少,反应生成气体的颜色逐渐变浅,最终共生成气体
的不断减少,反应生成气体的颜色逐渐变浅,最终共生成气体 (标准状况)。则该浓硝酸的物质的量浓度是
(标准状况)。则该浓硝酸的物质的量浓度是___________  ;若将生成的气体溶于水被全部吸收,还需要消耗标准状况下
;若将生成的气体溶于水被全部吸收,还需要消耗标准状况下
___________  。
。
 铜镁合金与足量稀硝酸完全反应,放出
铜镁合金与足量稀硝酸完全反应,放出 气体(标况下),转移电子数为
气体(标况下),转移电子数为 溶液至完全沉淀,得到沉淀的质量为
溶液至完全沉淀,得到沉淀的质量为(2)将
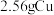 放入
放入 浓
浓 中正好完全反应。随着
中正好完全反应。随着 的不断减少,反应生成气体的颜色逐渐变浅,最终共生成气体
的不断减少,反应生成气体的颜色逐渐变浅,最终共生成气体 (标准状况)。则该浓硝酸的物质的量浓度是
(标准状况)。则该浓硝酸的物质的量浓度是 ;若将生成的气体溶于水被全部吸收,还需要消耗标准状况下
;若将生成的气体溶于水被全部吸收,还需要消耗标准状况下
 。
。
您最近一年使用:0次
8 . 向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
(1)Cu与稀HNO3反应的离子方程式为_____ 。
(2)混合物中Cu与Cu2O的物质的量分别为______ 、______ 。(要求写出计算过程)
(1)Cu与稀HNO3反应的离子方程式为
(2)混合物中Cu与Cu2O的物质的量分别为
您最近一年使用:0次
9 . 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
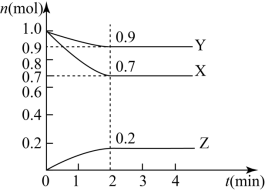
(1)X的转化率是___________ ;
(2)由图中所给数据进行分析,该反应的化学方程式为___________ ;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=___________ .

(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=
您最近一年使用:0次
2021-03-31更新
|
184次组卷
|
3卷引用:四川省平昌县驷马中学2020-2021学年下学期高二第一次月考化学试题
名校
解题方法
10 . (1)区别溶液和胶体的一种常用的物理方法是______ 。
(2)分离两种相互溶解但沸点相差较大的液体常用的实验方法是______ 。
(3)0.1 mol/L Al2(SO4)3中Al3+的物质的量浓度是______ ;同温同压下,等体积的CO和CO2所含分子数之比为________ 。
(4)已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中的氧化剂是______ (写化学式),被氧化的元素是____ (写元素符号)。
(5)若该反应中生成标准状况下的Cl2为67.2 L,则转移的电子个数是_________ 。
(2)分离两种相互溶解但沸点相差较大的液体常用的实验方法是
(3)0.1 mol/L Al2(SO4)3中Al3+的物质的量浓度是
(4)已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中的氧化剂是
(5)若该反应中生成标准状况下的Cl2为67.2 L,则转移的电子个数是
您最近一年使用:0次



