1 . (1)若t=25℃时,Kw=___________ ,若t=100℃时,Kw=1.0×10-12,则100℃时0.05 mol•L-1 Ba(OH)2 溶液的pH=___________ 。
(2)已知25℃时,0.1 L 0.1 mol•L-1的Na2A溶液的pH=11,用离子方程式表示其原因为___________ 。
(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH___________ NaOH溶液的pH(填“>”“=”或“<”) 。
(4)室温下,pH=2的H2SO4溶液、pH=12的NaOH溶液、pH=12的Na2CO3溶液,水电离出的c(H+)之比为___________ 。
(5)相同物质的量浓度的①NH4HSO4、②NH4HCO3、③NH4Cl三种溶液,pH值从大到小的顺序为___________ (用数字标号填空,下同);相同温度下,NH 浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为
浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为___________ 。
(6)含有Cr2O 的废水毒性较大。某工厂酸性废水中含5.0×10-3 mol•L-1的Cr2O
的废水毒性较大。某工厂酸性废水中含5.0×10-3 mol•L-1的Cr2O ,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。
,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。
①写出加入绿矾的离子方程式___________ 。
②若处理后的废水中残留的c(Fe3+)=4.0×10-13 mol•L-1,则残留的Cr3+的浓度为___________ mol•L-1(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-33)。
(2)已知25℃时,0.1 L 0.1 mol•L-1的Na2A溶液的pH=11,用离子方程式表示其原因为
(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH
(4)室温下,pH=2的H2SO4溶液、pH=12的NaOH溶液、pH=12的Na2CO3溶液,水电离出的c(H+)之比为
(5)相同物质的量浓度的①NH4HSO4、②NH4HCO3、③NH4Cl三种溶液,pH值从大到小的顺序为
 浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为
浓度相等的上述三种溶液,物质的量浓度从大到小的顺序为(6)含有Cr2O
 的废水毒性较大。某工厂酸性废水中含5.0×10-3 mol•L-1的Cr2O
的废水毒性较大。某工厂酸性废水中含5.0×10-3 mol•L-1的Cr2O ,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。
,可先向废水中加入绿矾(FeSO4·7H2O),搅拌后撒入生石灰处理。①写出加入绿矾的离子方程式
②若处理后的废水中残留的c(Fe3+)=4.0×10-13 mol•L-1,则残留的Cr3+的浓度为
您最近一年使用:0次
名校
解题方法
2 . 铁和氧化铁的混合物15 g中加入150 mL稀H2SO4放出氢气1.68 L(标准状况)。当反应停止后,铁和氧化铁均无剩余,且溶液中无Fe3+存在。为了中和过量H2SO4,并使Fe2+完全转化为Fe(OH)2沉淀,共耗用3 mol/L NaOH溶液200 mL。求:
(1)稀H2SO4的物质的量浓度为_________ 。
(2)混合物中铁的质量分数________ 。(保留2位小数,写出具体计算过程)
(1)稀H2SO4的物质的量浓度为
(2)混合物中铁的质量分数
您最近一年使用:0次
3 . 利用“化学计量在实验中的应用”的相关知识进行填空。
(1)______ molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(2)同温同压下,等质量的SO2和O2,两者体积比为______ ,分子个数比为______ ,密度比为______ 。
(3)在一定条件下,44.8g单质R与1.2molCl2完全反应,生成0.8molRClx,则x=______ ,R的摩尔质量为______ 。
(4)合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。某FeO、Fe2O3混合物中铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为______ 。
(5)已知ag A和bg B恰好完全反应生成0.2mol C和dg D,则C的摩尔质量为______ 。
(1)
(2)同温同压下,等质量的SO2和O2,两者体积比为
(3)在一定条件下,44.8g单质R与1.2molCl2完全反应,生成0.8molRClx,则x=
(4)合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。某FeO、Fe2O3混合物中铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为
(5)已知ag A和bg B恰好完全反应生成0.2mol C和dg D,则C的摩尔质量为
您最近一年使用:0次
名校
4 . 已知N2O4(g) 2NO2(g),△H>0,在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g),△H>0,在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)20s时,N2O4的分解率是___ 。
(2)40s时,NO2的浓度为___ ,0~40s内N2O4的平均反应速率为____ 。
(3)在80℃时该反应的平衡常数K值为___ 。
(4)判断t2、t3、t4时刻对该反应采取的措施。
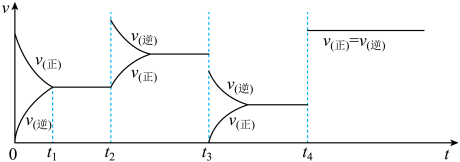
t2:___ ;t3:___ ;t4:___ 。
 2NO2(g),△H>0,在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g),△H>0,在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.12 | c | d | e |
| c(NO2) | 0.00 | 0.08 | b | 0.20 | 0.20 | 0.20 |
(1)20s时,N2O4的分解率是
(2)40s时,NO2的浓度为
(3)在80℃时该反应的平衡常数K值为
(4)判断t2、t3、t4时刻对该反应采取的措施。

t2:
您最近一年使用:0次
名校
5 . ①在 _____ mol Al2(SO4)3 中含 0.3mol SO ,含 Al3+
,含 Al3+______ 个。
②相同质量的 SO2 气体和 SO3 气体,其分子数之比为___________ ,相同条件下(同温同压)的体积之比为 ___________ 。
③已知 n 个铜原子的质量是 a,则铜的摩尔质量是___________
④在标准状况下,CO2 和 CO 的混合气体密度是 H2 的密度的 19 倍,则其体积比为___________
 ,含 Al3+
,含 Al3+②相同质量的 SO2 气体和 SO3 气体,其分子数之比为
③已知 n 个铜原子的质量是 a,则铜的摩尔质量是
④在标准状况下,CO2 和 CO 的混合气体密度是 H2 的密度的 19 倍,则其体积比为
您最近一年使用:0次
解题方法
6 . 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16 g白色沉淀,再向所得浊液中逐渐加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。
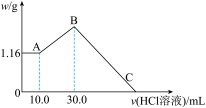
(1)A点的沉淀物的化学式为___________ 。
(2)写出A点至B点发生反应的离子方程式:___________ 。
(3)某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为:NaOH溶液、___________ (填化学式)和盐酸。
(4)C点(此时沉淀恰好完全溶解)HCl溶液的体积为___________ mL。

(1)A点的沉淀物的化学式为
(2)写出A点至B点发生反应的离子方程式:
(3)某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为:NaOH溶液、
(4)C点(此时沉淀恰好完全溶解)HCl溶液的体积为
您最近一年使用:0次
2020-12-19更新
|
259次组卷
|
2卷引用:四川省成都市实验外国语学校(西区)2019-2020学年高一上学期11月月考化学试题
名校
解题方法
7 . 填空
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石___ (填“>”或“<”)石墨。
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1____ (填“>”或“<”)ΔH2。
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:________ 。
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=____ 。
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=______ 。
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是________ 。
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
2020-12-15更新
|
320次组卷
|
6卷引用:2015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷
2015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷河北省安平中学2017-2018学年高一下学期期末考试化学试题1贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题(已下线)第六章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题
解题方法
8 . (1)0.5 mol H2SO4 的质量是_____ g,含__ 个分子,含____ mol氧原子,该硫酸所含氢元素的质量与___ mol HCl中所含氢元素的质量相同。
(2)在相同条件下,含有相同分子个数的SO2和SO3,物质的量之比为____ ,其中所含氧原子个数比为____ ,SO2和SO3质量之比为_____ 。
(3)含3.01×1023个HCl分子的气体在标准状况下的体积是______ ,将该气体溶于水配成50mL溶液,HCl的物质的量浓度是_______ ,如果要配制100mL1mol/L的稀盐酸需要该浓盐酸______ mL
(2)在相同条件下,含有相同分子个数的SO2和SO3,物质的量之比为
(3)含3.01×1023个HCl分子的气体在标准状况下的体积是
您最近一年使用:0次
9 . 计算题
(1)3.6g H2O的物质的量是________ ,约含有____________________________ 个水分子,含有________ mol H。
(2)3.01×1023个H2O分子的物质的量为________ ,质量为________ ,含有质子的物质的量为________ ,含有电子的数目为________ ,这些H2O分子所含的H原子数目与________ mol CH4所含的H原子数目相同,和________ g CO2含有的分子数相同。
(3)质量为3.9g的Na2X中含有Na+的物质的量为0.1mol,则Na2X的摩尔质量为___________________ 。
(1)3.6g H2O的物质的量是
(2)3.01×1023个H2O分子的物质的量为
(3)质量为3.9g的Na2X中含有Na+的物质的量为0.1mol,则Na2X的摩尔质量为
您最近一年使用:0次
解题方法
10 . (1)0.4molCH4的质量为______ g;标况下,4.48LCO2的分子数为______ 。
(2)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为______ 。
(3)将4gNaOH溶解在水中配成10mL溶液,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为_______ mol·L-1。
(4)VLAl2(SO4)3溶液中含有Al3+ag,则溶液中 的物质的量浓度为
的物质的量浓度为________ mol∙L-1
(5)某混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则 的物质的量浓度为
的物质的量浓度为_______ mol∙L-1。
(2)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
(3)将4gNaOH溶解在水中配成10mL溶液,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为
(4)VLAl2(SO4)3溶液中含有Al3+ag,则溶液中
 的物质的量浓度为
的物质的量浓度为(5)某混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol∙L-1、0.25mol∙L-1、0.4mol∙L-1,则 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次



