名校
1 . 某温度下,往密闭容器中加入一定量的A和B,发生 的反应。C的物质的浓度随反应时间(t)的变化如下表。下列说法中
的反应。C的物质的浓度随反应时间(t)的变化如下表。下列说法中不正确 的是
 的反应。C的物质的浓度随反应时间(t)的变化如下表。下列说法中
的反应。C的物质的浓度随反应时间(t)的变化如下表。下列说法中| t/s | 2 | 4 | 6 | 8 | 10 | 12 |
C的浓度/( ) ) | 0.22 | 0.36 | 0.42 | 0.46 | 0.46 | 0.46 |
A.在0~6s内,平均反应速率v(A)为0.14 |
| B.0~8s正反应速率大于逆反应速率 |
| C.8s后反应物消耗完,反应停止 |
| D.8~12s该反应处于化学平衡状态 |
您最近一年使用:0次
名校
2 . 在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g)  2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,用SO2的浓度变化表示的平均反应速率v(SO2)=___________ 。
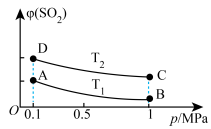
(3)若反应温度降低,SO2的转化率___________ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1___________ T2(填“>”“<”或“=”)。
(4)已知反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
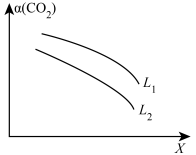
①X表示的物理量是___________ 。
②L1___________ L2(填“<”或“>”),判断理由是___________ 。
 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

(4)已知反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
CH4(g)+2H2O(g) ΔH<0。在一定条件下,反应体系中CO2的平衡转化率α(CO2)与L和X的关系如图所示,L和X表示温度或压强。
①X表示的物理量是
②L1
您最近一年使用:0次
名校
解题方法
3 . 由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。

已知:
反应①: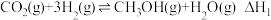
反应②: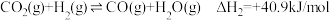
反应③:
(1)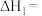
_________________ ;
(2)某研究小组将2molCH3OH通入2L的刚性密闭容器内,只发生反应③,5分钟后容器压强变为原来的2.5倍,则这段时间内,
______________ ;CH3OH的转化率为:______________ ;
(3)某研究小组采用上述催化剂,向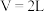 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,只发生反应①和反应②,在不同条件下达到平衡。其中,在
,只发生反应①和反应②,在不同条件下达到平衡。其中,在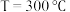 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强P的变化、在
随压强P的变化、在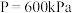 下
下 随温度T的变化,如图所示。
随温度T的变化,如图所示。

①Y点对应的温度和压强为_____________  、
、_____________  ;
;
②M点时容器中CO2为 mol,CO为
mol,CO为 mol,反应①的化学平衡常数
mol,反应①的化学平衡常数
_____________ 。
③图中M点的 高于N点的原因是
高于N点的原因是___________________________ 。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。
已知:
反应①:
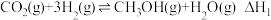
反应②:
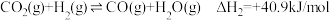
反应③:

(1)
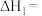
(2)某研究小组将2molCH3OH通入2L的刚性密闭容器内,只发生反应③,5分钟后容器压强变为原来的2.5倍,则这段时间内,

(3)某研究小组采用上述催化剂,向
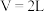 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,只发生反应①和反应②,在不同条件下达到平衡。其中,在
,只发生反应①和反应②,在不同条件下达到平衡。其中,在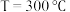 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强P的变化、在
随压强P的变化、在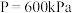 下
下 随温度T的变化,如图所示。
随温度T的变化,如图所示。
①Y点对应的温度和压强为
 、
、 ;
;②M点时容器中CO2为
 mol,CO为
mol,CO为 mol,反应①的化学平衡常数
mol,反应①的化学平衡常数
③图中M点的
 高于N点的原因是
高于N点的原因是
您最近一年使用:0次
名校
解题方法
4 . 小组同学探究影响 分解反应速率的因素。
分解反应速率的因素。
(1)在 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为_______________ 。
【实验方案】
(2)对比实验①和实验②,目的是探究______ 对 分解反应速率的影响。
分解反应速率的影响。
(3)对比实验②和实验③,目的是_____ 对 分解反应速率的影响,则实验③中x的值是
分解反应速率的影响,则实验③中x的值是_____ 。
(4)如果实验②中 时共收集到气体的体积为
时共收集到气体的体积为 (已折算成标准状况下),则用过氧化氢表示的
(已折算成标准状况下),则用过氧化氢表示的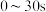 的平均反应速率为
的平均反应速率为__________  。
。
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如图所示。
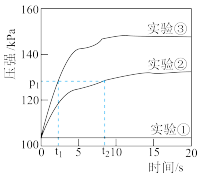
(5)上述实验中, 分解速率最快的是
分解速率最快的是_______ (填序号 );
(6)图中能证明 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是__________ 。
 分解反应速率的因素。
分解反应速率的因素。(1)在
 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为【实验方案】
| 实验编号 |  溶液 溶液 | 蒸馏水 | 催化剂 | 温度 | |
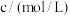 |  |  | |||
| ① | 3 | 10 | 20 | 无催化剂 | 20 |
| ② | 3 | 10 | 20 | 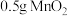 固体 固体 | 20 |
| ③ | 3 | 15 | x | 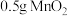 固体 固体 | 20 |
(2)对比实验①和实验②,目的是探究
 分解反应速率的影响。
分解反应速率的影响。(3)对比实验②和实验③,目的是
 分解反应速率的影响,则实验③中x的值是
分解反应速率的影响,则实验③中x的值是(4)如果实验②中
 时共收集到气体的体积为
时共收集到气体的体积为 (已折算成标准状况下),则用过氧化氢表示的
(已折算成标准状况下),则用过氧化氢表示的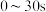 的平均反应速率为
的平均反应速率为 。
。【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如图所示。

(5)上述实验中,
 分解速率最快的是
分解速率最快的是(6)图中能证明
 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是
您最近一年使用:0次
名校
5 . 甲醇是21世纪的新型燃料,而据统计,我国没经处理便排放的焦炉煤气超250亿立方米,这是能源的浪费。为解决这一问题,我国在2004年起利用焦炉煤气制取甲醇。
(1)已知 中的
中的 与
与 之间为三键连接,且合成甲醇的主要反应原理为
之间为三键连接,且合成甲醇的主要反应原理为 。表中所列为常见化学键的键能数据:
。表中所列为常见化学键的键能数据:
则该反应的
___________  。
。
(2)以 和
和 为原料也可合成甲醇,反应的能量变化如图所示。
为原料也可合成甲醇,反应的能量变化如图所示。

图中 处应填入
处应填入___________ 。
(3)工业上可以用 和
和 为原料,先制备
为原料,先制备 和
和 气体,再制备甲醇。现将
气体,再制备甲醇。现将
 和
和 通入容积为
通入容积为 的反应室,在一定条件下发生反应:
的反应室,在一定条件下发生反应: 的平衡转化率与温度、压强的关系如图:
的平衡转化率与温度、压强的关系如图:

①已知 ,压强为
,压强为 时,达到平衡需时
时,达到平衡需时 ,则用
,则用 表示的平均反应速率为
表示的平均反应速率为___________ 。
②其它条件不变,升高温度,化学平衡常数将___________ (填“增大”“减小”或“不变”)。
③图2中的
_______  (填“<”、“>”或“=”),在
(填“<”、“>”或“=”),在 ,压强为
,压强为 时平衡常数为
时平衡常数为___________ 。
④保持反应体系 ,压强为
,压强为 后再向容器中充入
后再向容器中充入 各
各 ,化学平衡将
,化学平衡将___________ 移动(填“向左”“向右”或“不”)。
(1)已知
 中的
中的 与
与 之间为三键连接,且合成甲醇的主要反应原理为
之间为三键连接,且合成甲醇的主要反应原理为 。表中所列为常见化学键的键能数据:
。表中所列为常见化学键的键能数据:| 化学键 |  |  |  |  |  |  |
键能 | 348 | 414 | 436 | 326.8 | 1032 | 464 |

 。
。(2)以
 和
和 为原料也可合成甲醇,反应的能量变化如图所示。
为原料也可合成甲醇,反应的能量变化如图所示。
图中
 处应填入
处应填入(3)工业上可以用
 和
和 为原料,先制备
为原料,先制备 和
和 气体,再制备甲醇。现将
气体,再制备甲醇。现将
 和
和 通入容积为
通入容积为 的反应室,在一定条件下发生反应:
的反应室,在一定条件下发生反应: 的平衡转化率与温度、压强的关系如图:
的平衡转化率与温度、压强的关系如图:
①已知
 ,压强为
,压强为 时,达到平衡需时
时,达到平衡需时 ,则用
,则用 表示的平均反应速率为
表示的平均反应速率为②其它条件不变,升高温度,化学平衡常数将
③图2中的

 (填“<”、“>”或“=”),在
(填“<”、“>”或“=”),在 ,压强为
,压强为 时平衡常数为
时平衡常数为④保持反应体系
 ,压强为
,压强为 后再向容器中充入
后再向容器中充入 各
各 ,化学平衡将
,化学平衡将
您最近一年使用:0次
名校
解题方法
6 . 下列方案设计能达到实验目的的是


| A.甲装置可以定量测定化学反应速率 |
| B.乙装置可以由球中气体颜色的深浅判断浓度对平衡的影响 |
| C.丙装置由褪色快慢研究反应物浓度对反应速率的影响 |
| D.比较乙醇中羟基氢原子和水分子中氢原子的活泼性 |
您最近一年使用:0次
名校
解题方法
7 . 氮的氧化物是大气污染物之一,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)碘蒸气的存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: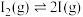 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: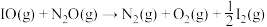 (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程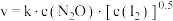 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________
(2)对反应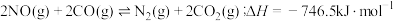 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
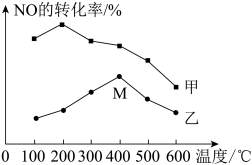
图中M点对应的速率(对应温度 )
)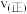
___________ 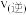 (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是___________ 。
(3)在密闭容器中充入 和
和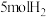 ,发生反应:
,发生反应: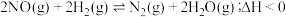 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。

①下列物理量中,图中d点大于b点的是___________ (填字母)。
A.正反应速率 B.逆反应速率
C. 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数
②c点NO的平衡转化率为___________ 。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的___________ 点。
(4) 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、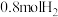 ,发生反应:
,发生反应: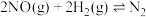
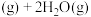 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示:
①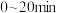 内该反应的平均反应速率
内该反应的平均反应速率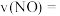
___________  。
。
②该温度下反应的平衡常数
___________  (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(1)碘蒸气的存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
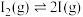 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
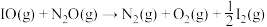 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程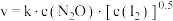 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能比第三步小 |
C. 为反应的催化剂 为反应的催化剂 |
D. 分解反应的速率与是否含碘蒸气有关 分解反应的速率与是否含碘蒸气有关 |
(2)对反应
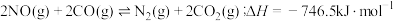 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
图中M点对应的速率(对应温度
 )
)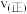
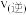 (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是(3)在密闭容器中充入
 和
和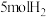 ,发生反应:
,发生反应: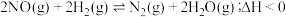 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中d点大于b点的是
A.正反应速率 B.逆反应速率
C.
 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数②c点NO的平衡转化率为
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的
(4)
 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、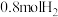 ,发生反应:
,发生反应: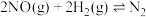
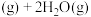 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示: | 0 | 10 | 20 | 30 | 40 |
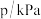 | 240 | 226 | 216 | 210 | 210 |
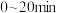 内该反应的平均反应速率
内该反应的平均反应速率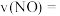
 。
。②该温度下反应的平衡常数

 (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
您最近一年使用:0次
2023-12-18更新
|
165次组卷
|
2卷引用:广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题
8 . 某恒定温度下,在一个 的密闭容器中充入
的密闭容器中充入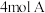 气体、
气体、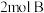 气体,发生如下反应:
气体,发生如下反应: ,已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成
,已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成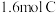 ,且反应前后压强比为
,且反应前后压强比为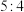 ,则下列说法中正确的是
,则下列说法中正确的是
①该反应的化学平衡常数表达式: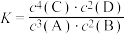
②此时B的转化率为40%
③增大该体系压强,平衡向右移动,化学平衡常数增大
④增加C的量,A、B转化率不变
 的密闭容器中充入
的密闭容器中充入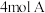 气体、
气体、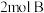 气体,发生如下反应:
气体,发生如下反应: ,已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成
,已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成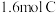 ,且反应前后压强比为
,且反应前后压强比为 ,则下列说法中正确的是
,则下列说法中正确的是①该反应的化学平衡常数表达式:
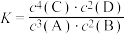
②此时B的转化率为40%
③增大该体系压强,平衡向右移动,化学平衡常数增大
④增加C的量,A、B转化率不变
| A.①②③ | B.②③④ | C.②④ | D.③④ |
您最近一年使用:0次
解题方法
9 . 我国力争在2060年前实现“碳中和”,综合利用CO2具有重要的意义。300MP、200oC条件下,CO2与H2反应可制得气态甲醇(CH3OH),其反应方程式为CO2+3H2 CH3OH+H2O(g)。
CH3OH+H2O(g)。
(1)该反应的能量变化如图所示:
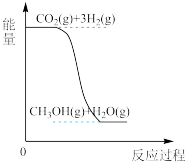
该反应是_______ 反应(填“吸热”或“放热”),判断的理由是 _______ 。
(2)为了加快该反应的速率,可以采取措施_______ (任写一种)。
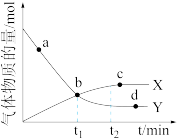
(3)在实际生产中,测得合成塔中H2及H2O(g)的物质的量随时间变化如下图所示,则图中代表 的曲线是
的曲线是_______ (填“X”或“Y”),v(正)与v(逆)相等的点为_______ (填字母)。
(4)在一定温度下,将2molCO2与6molH2气体混合于2L密闭容器中制甲醇,2min末生成0.8mol H2O(g)。
①用单位时间内 浓度的减小来表示2min内该反应的平均速率为
浓度的减小来表示2min内该反应的平均速率为_______ mol· L-1· min-1;
②2min末容器中H2的物质的量浓度_______ 。
 CH3OH+H2O(g)。
CH3OH+H2O(g)。(1)该反应的能量变化如图所示:

该反应是
(2)为了加快该反应的速率,可以采取措施
(3)在实际生产中,测得合成塔中H2及H2O(g)的物质的量随时间变化如下图所示,则图中代表
 的曲线是
的曲线是
(4)在一定温度下,将2molCO2与6molH2气体混合于2L密闭容器中制甲醇,2min末生成0.8mol H2O(g)。
①用单位时间内
 浓度的减小来表示2min内该反应的平均速率为
浓度的减小来表示2min内该反应的平均速率为②2min末容器中H2的物质的量浓度
您最近一年使用:0次
名校
解题方法
10 . 反应 ,在不同条件下的反应速率分别为:①
,在不同条件下的反应速率分别为:① ,②
,② ,③
,③ ,④
,④ ,则此反应在不同条件下进行得最快的是
,则此反应在不同条件下进行得最快的是
 ,在不同条件下的反应速率分别为:①
,在不同条件下的反应速率分别为:① ,②
,② ,③
,③ ,④
,④ ,则此反应在不同条件下进行得最快的是
,则此反应在不同条件下进行得最快的是| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次



