解题方法
1 . 已知:常温下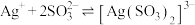 ,
,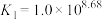 ,
,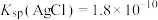 ,某实验小组利用AgCl与Na2SO3反应生成
,某实验小组利用AgCl与Na2SO3反应生成 来“分银”,“分银”时,
来“分银”,“分银”时, 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 与H+形成的微粒的浓度分数
与H+形成的微粒的浓度分数 随溶液pH变化的关系如图2,下列叙述错误的是
随溶液pH变化的关系如图2,下列叙述错误的是
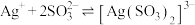 ,
,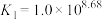 ,
,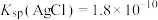 ,某实验小组利用AgCl与Na2SO3反应生成
,某实验小组利用AgCl与Na2SO3反应生成 来“分银”,“分银”时,
来“分银”,“分银”时, 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 与H+形成的微粒的浓度分数
与H+形成的微粒的浓度分数 随溶液pH变化的关系如图2,下列叙述错误的是
随溶液pH变化的关系如图2,下列叙述错误的是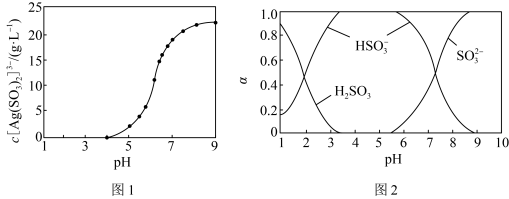
A. 中的∠O—S—O小于 中的∠O—S—O小于 中的∠O—S—O 中的∠O—S—O |
| B.“分银”时,pH需控制的范围大约是8~9 |
C. 溶液中存在 溶液中存在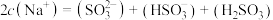 |
D.AgCl与 反应生成 反应生成 和 和 ,该反应的平衡常数 ,该反应的平衡常数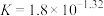 |
您最近半年使用:0次
解题方法
2 . 结构决定性质,下列关于物质结构或性质及有关解释不正确的是
| A.稳定性:H2O>H2S,是由于水分子间存在氢键 |
| B.酸性:一氟乙酸>一氯乙酸,是由于F的电负性大于Cl,F—C的极性大于Cl—C的极性 |
| C.键角:NCl3>PCl3,是由于N的电负性比P大,N的成键电子对之间距离较近,斥力较大 |
| D.溶解度:O3在CCl4中的溶解度高于在水中的溶解度,是由于O3的极性微弱 |
您最近半年使用:0次
3 . 短周期元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示,已知戊的非金属性最强且其基态原子p轨道只有一个未成对电子。下列说法错误的是
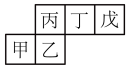
| A.简单离子半径:丁>戊 | B.第一电离能:丙<丁<戊 |
| C.简单氢化物的沸点:乙<丙 | D.简单氢化物的键角:甲>乙 |
您最近半年使用:0次
4 . 下列化学用语或图示表达正确的是
A.NaOH的电子式: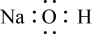 |
B.基态Cu的价层电子排布式: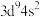 |
C.基态硅原子的价层电子轨道表示式: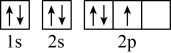 |
D. 分子的空间结构: 分子的空间结构: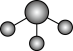 |
您最近半年使用:0次
名校
5 . 下列各组微粒的空间构型相同的是
①NH3和H2O ②NH 和H3O+ ③NH3和H3O+ ④BF3和NO
和H3O+ ③NH3和H3O+ ④BF3和NO ⑤CO2和BeCl2 ⑥PO
⑤CO2和BeCl2 ⑥PO 和SO
和SO ⑦O3和SO2
⑦O3和SO2
①NH3和H2O ②NH
 和H3O+ ③NH3和H3O+ ④BF3和NO
和H3O+ ③NH3和H3O+ ④BF3和NO ⑤CO2和BeCl2 ⑥PO
⑤CO2和BeCl2 ⑥PO 和SO
和SO ⑦O3和SO2
⑦O3和SO2| A.全部 | B.除④⑥⑦以外都相同 | C.②⑤⑥ | D.③④⑤⑥⑦ |
您最近半年使用:0次
名校
解题方法
6 . 下列说法正确的是
A. 的第一电离能高于 的第一电离能高于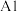 ,则 ,则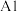 的金属性强于 的金属性强于 |
B. 是非极性分子,则 是非极性分子,则 也是非极性分子 也是非极性分子 |
| C.分子晶体中分子间作用力越大,对应的物质越稳定 |
| D.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
您最近半年使用:0次
名校
解题方法
7 . 下列化学用语表述正确的是
A. 的价电子排布式: 的价电子排布式: | B. 的球棍模型: 的球棍模型: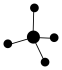 |
C. 的电子式: 的电子式: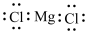 | D. 分子的VSEPR模型: 分子的VSEPR模型: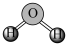 |
您最近半年使用:0次
解题方法
8 . 某抗病毒试剂由原子半径依次增大的短周期主族元素X、Y、Z、M组成。其中M以+1价离子形式存在,阴离子的结构如下图所示。下列说法错误的是
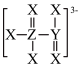
| A.原子半径:M>Z |
| B.基态X原子核外有3种能量不同的电子 |
| C.最高价氧化物对应水化物的酸性:Y <Z |
D.Z的简单氢化物分子的VSEPR模型: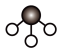 |
您最近半年使用:0次
名校
解题方法
9 . 下列各组微粒的中心原子杂化类型相同但微粒的空间结构不同的是
A. 、 、 | B. 、 、 | C. 、 、 | D. 、 、 |
您最近半年使用:0次
解题方法
10 . 已知:硫代硫酸根( )可看作是
)可看作是 中的一个O原子被S原子取代的产物,
中的一个O原子被S原子取代的产物, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成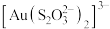 。下列有关说法正确的是
。下列有关说法正确的是
 )可看作是
)可看作是 中的一个O原子被S原子取代的产物,
中的一个O原子被S原子取代的产物, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成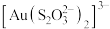 。下列有关说法正确的是
。下列有关说法正确的是A.SO3与 的键角相等 的键角相等 |
B. 与 与 的空间构型相同 的空间构型相同 |
| C. SO3是极性分子,故SO3易溶于水 |
D. 作为配体时,两种硫原子中只有端基硫原子能提供孤电子对 作为配体时,两种硫原子中只有端基硫原子能提供孤电子对 |
您最近半年使用:0次



