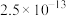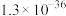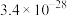1 . 五氧化二钒( )为橙黄色晶性粉末,在冶金、化工、催化等领域有重要应用,也是制备其他钒化合物的重要原料。实验室以含钒废料(主要成分为
)为橙黄色晶性粉末,在冶金、化工、催化等领域有重要应用,也是制备其他钒化合物的重要原料。实验室以含钒废料(主要成分为 ,还含有Fe、Cu、Mn、Si、AI等元素的氧化物以及有机物)为原料制备
,还含有Fe、Cu、Mn、Si、AI等元素的氧化物以及有机物)为原料制备 的一种流程如图所示:
的一种流程如图所示:
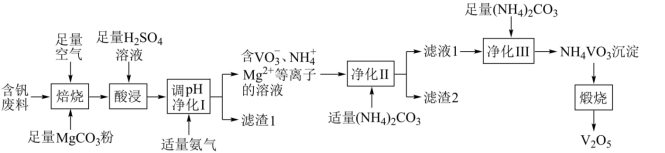
已知:①含钒离子在溶液中的存在形式与溶液pH的关系
②25℃时,难溶电解质的溶度积常数如表所示:
请回答下列问题:
(1)写出基态V原子的价层电子排布式:___________ 。
(2)“焙烧”的目的之一是将 转化成
转化成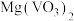 ,请写出转化的化学方程式:
,请写出转化的化学方程式:___________ 。
(3)“酸浸”时,为了提升各物质的浸出速率,除了适当升高温度外,还可以采取的措施是___________ (写一条即可)。
(4)25℃,“调pH净化Ⅰ”时需将 、
、 、
、 三种离子去除干净(浓度
三种离子去除干净(浓度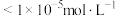 时视为去除干净)外,还需要考虑V的存在形式,则需调节pH范围为
时视为去除干净)外,还需要考虑V的存在形式,则需调节pH范围为___________ 。
(5)“净化Ⅱ”的目的是除 、
、 ,若该过程加入过量
,若该过程加入过量 ,可能导致的结果是
,可能导致的结果是___________ 。
(6)“滤液1”中加入 的目的是将
的目的是将 变成沉淀偏钒酸铵(
变成沉淀偏钒酸铵( ),简称“沉钒”。“沉钒”得到的
),简称“沉钒”。“沉钒”得到的 需进行洗涤、干燥,请写出证明
需进行洗涤、干燥,请写出证明 已洗净的实验操作及现象:
已洗净的实验操作及现象:___________ 。
(7)煅烧 得到的产物中,可以在该流程中循环利用的物质是
得到的产物中,可以在该流程中循环利用的物质是___________ 。
(8)为测定该产品的纯度,某同学准确称取 产品1.000g,加入过量稀硫酸使其完全转化成
产品1.000g,加入过量稀硫酸使其完全转化成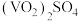 ,并配成100mL溶液(此溶液pH=1)。取10.00mL溶液用0.1000mol/L的
,并配成100mL溶液(此溶液pH=1)。取10.00mL溶液用0.1000mol/L的 标准溶液滴定,滴定到终点时消耗标准液5mL。已知滴定过程中
标准溶液滴定,滴定到终点时消耗标准液5mL。已知滴定过程中 被氧化为
被氧化为 ,该产品的纯度为
,该产品的纯度为___________ 。(计算结果保留两位小数)
 )为橙黄色晶性粉末,在冶金、化工、催化等领域有重要应用,也是制备其他钒化合物的重要原料。实验室以含钒废料(主要成分为
)为橙黄色晶性粉末,在冶金、化工、催化等领域有重要应用,也是制备其他钒化合物的重要原料。实验室以含钒废料(主要成分为 ,还含有Fe、Cu、Mn、Si、AI等元素的氧化物以及有机物)为原料制备
,还含有Fe、Cu、Mn、Si、AI等元素的氧化物以及有机物)为原料制备 的一种流程如图所示:
的一种流程如图所示:
已知:①含钒离子在溶液中的存在形式与溶液pH的关系
| 溶液pH | <4.0 | 6.0≤pH≤8.0 | >8.0 |
| 钒元素存在形式 |  |  | 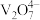 |
| 难溶电解质 |  |  |  |  |  |  |
 | 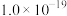 | 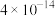 |  |  | 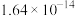 |  |
(1)写出基态V原子的价层电子排布式:
(2)“焙烧”的目的之一是将
 转化成
转化成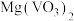 ,请写出转化的化学方程式:
,请写出转化的化学方程式:(3)“酸浸”时,为了提升各物质的浸出速率,除了适当升高温度外,还可以采取的措施是
(4)25℃,“调pH净化Ⅰ”时需将
 、
、 、
、 三种离子去除干净(浓度
三种离子去除干净(浓度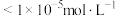 时视为去除干净)外,还需要考虑V的存在形式,则需调节pH范围为
时视为去除干净)外,还需要考虑V的存在形式,则需调节pH范围为(5)“净化Ⅱ”的目的是除
 、
、 ,若该过程加入过量
,若该过程加入过量 ,可能导致的结果是
,可能导致的结果是(6)“滤液1”中加入
 的目的是将
的目的是将 变成沉淀偏钒酸铵(
变成沉淀偏钒酸铵( ),简称“沉钒”。“沉钒”得到的
),简称“沉钒”。“沉钒”得到的 需进行洗涤、干燥,请写出证明
需进行洗涤、干燥,请写出证明 已洗净的实验操作及现象:
已洗净的实验操作及现象:(7)煅烧
 得到的产物中,可以在该流程中循环利用的物质是
得到的产物中,可以在该流程中循环利用的物质是(8)为测定该产品的纯度,某同学准确称取
 产品1.000g,加入过量稀硫酸使其完全转化成
产品1.000g,加入过量稀硫酸使其完全转化成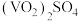 ,并配成100mL溶液(此溶液pH=1)。取10.00mL溶液用0.1000mol/L的
,并配成100mL溶液(此溶液pH=1)。取10.00mL溶液用0.1000mol/L的 标准溶液滴定,滴定到终点时消耗标准液5mL。已知滴定过程中
标准溶液滴定,滴定到终点时消耗标准液5mL。已知滴定过程中 被氧化为
被氧化为 ,该产品的纯度为
,该产品的纯度为
您最近一年使用:0次
名校
2 . 常温下,用HCl(g)调节SrF2浊液的pH,测得在通入HCl(g)的过程中,体系中-lgc(X)(X代表Sr2+或F-)与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是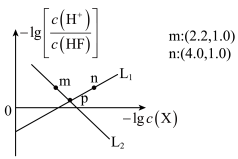
A.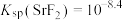 |
B.L2表示 的变化情况 的变化情况 |
| C.随着HCl的加入,SrF2溶解度逐渐增大 |
D.m、n点对应的溶液中均存在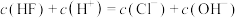 |
您最近一年使用:0次
2024-03-19更新
|
419次组卷
|
4卷引用:湖南省资兴市立中等多校联考2023-2024学年高二下学期3月月考化学试题
名校
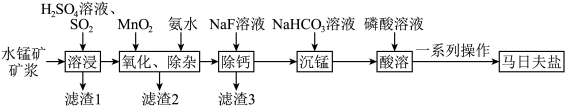
3 . 马日夫盐[Mn(H2PO4)2•2H2O]常用于机械设备的磷化处理,可起到防锈效果。以水锰矿[主要成分为MnO(OH),还含有少量的Fe2O3、SiO2及微量的CaO、Al2O3]为原料制备马日夫盐的一种工艺流程如图所示。
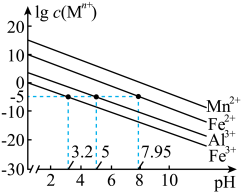
已知:①25℃时,金属离子在水溶液中的平衡浓度的对数与溶液的pH的关系如图所示。此实验条件下Mn2+开始沉淀的pH=7.54。
②当溶液中剩余的某金属离子浓度≤1×10-5mol/L时,通常认为该金属离子已沉淀完全。
回答下列问题:
(1)“溶浸”过程中主要成分发生反应的化学方程式为_______ ,为提高SO2的吸收率,可采取的措施是_______ (写出两条即可)。
(2)“滤渣2”的主要成分为_______ (写化学式)。“氧化、除杂”步骤中不宜使用H2O2替代MnO2,原因是_______ 。加入氨水的目的是调节pH,应控制pH的范围是________ 之间。
(3)加入NaF可以使Ca2+转化为CaF,沉淀除去,要使Ca2+完全沉淀,该步骤中应控制溶液中F-浓度不小于______ mol/L。[已知:Ksp(CaF2)=3.6×10-12]。
(4)“沉锰”步骤中Mn2+转化为MnCO3沉淀,反应的离子方程式为_______ 。
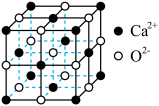
(5)CaO晶胞的结构如图所示,CaO晶体中Ca2+的配位数为______ ,距离最近的Ca2+和O2-的核间距为apm,则CaO晶体的密度为_______ g/cm3(列出计算式,阿伏加德罗常数的值为NA)。

已知:①25℃时,金属离子在水溶液中的平衡浓度的对数与溶液的pH的关系如图所示。此实验条件下Mn2+开始沉淀的pH=7.54。

②当溶液中剩余的某金属离子浓度≤1×10-5mol/L时,通常认为该金属离子已沉淀完全。
回答下列问题:
(1)“溶浸”过程中主要成分发生反应的化学方程式为
(2)“滤渣2”的主要成分为
(3)加入NaF可以使Ca2+转化为CaF,沉淀除去,要使Ca2+完全沉淀,该步骤中应控制溶液中F-浓度不小于
(4)“沉锰”步骤中Mn2+转化为MnCO3沉淀,反应的离子方程式为
(5)CaO晶胞的结构如图所示,CaO晶体中Ca2+的配位数为

您最近一年使用:0次
2024-03-18更新
|
416次组卷
|
3卷引用:湖南省衡阳市第八中学2024届高三模拟预测信息卷(一)化学试题
名校
解题方法
4 . 废旧钴酸锂电池的正极材料主要含有难溶于水的LiCoO2及少量Al、Fe、炭黑等,常用如图1所示的一种工艺分离并回收其中的金属钴和锂。
②相关金属离子形成氢氧化物沉淀的pH如下表:
回答下列问题:
(1)LiCoO2中元素Co的化合价为___________ 。
(2)为提高碱浸率,可采取的措施有___________ (答出一条即可)。
(3)碱浸时的离子反应方程式为___________ 。
(4)沉钴的离子方程式为___________ 。
(5)加氨水控制沉钴的pH,当a≥___________ 时,此时溶液中c(Co2+)≤10-5mol⋅L-1,即认为“沉钴”完全。
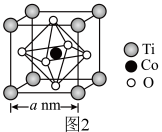
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为___________ 。___________ molAgCl,该配合物中Co3+的配位数为___________ 。
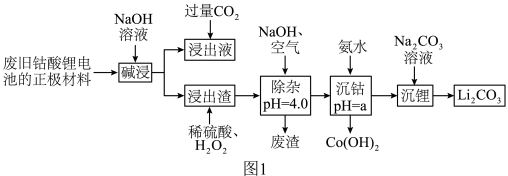
②相关金属离子形成氢氧化物沉淀的pH如下表:
| 金属阳离子 | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 4.2 | 2.7 | 7.6 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 |
(1)LiCoO2中元素Co的化合价为
(2)为提高碱浸率,可采取的措施有
(3)碱浸时的离子反应方程式为
(4)沉钴的离子方程式为
(5)加氨水控制沉钴的pH,当a≥
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为
您最近一年使用:0次
2024-03-17更新
|
160次组卷
|
2卷引用:湖南省雅礼教育集团2023-2024学年高二下学期期中考试化学试题
5 . 磷酸亚铁锂 是重要的锂电池正极材料,一种利用硫酸法生产钛白粉过程的副产物硫酸亚铁(含钛、铜、锰、铅、锌、钙、镁等杂质离子)制备磷酸亚铁锂的生产流程如图.
是重要的锂电池正极材料,一种利用硫酸法生产钛白粉过程的副产物硫酸亚铁(含钛、铜、锰、铅、锌、钙、镁等杂质离子)制备磷酸亚铁锂的生产流程如图.

常温下各种硫化物溶度积常数如下:
回答下列问题:
(1)为提高硫酸亚铁浸取速率,可以采取的措施是___________ (答一点即可)。
(2)基态亚铁离子的电子排布式为__________________________ 。
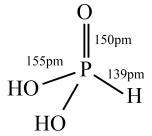
(3)磷元素可以形成多种含氧酸,亚磷酸 结构如图所示,则亚磷酸属于
结构如图所示,则亚磷酸属于___________ 元酸。
(4)在滤液2中加入磷酸需控制 ,其目的是①磷酸根过量,可以减少铁的其他形式的沉淀,提高
,其目的是①磷酸根过量,可以减少铁的其他形式的沉淀,提高 的纯度;②
的纯度;②______________________ 。
(5)聚丙烯的作用是___________________________________ 。
(6)已知当溶液中 时视为沉淀完全,又知
时视为沉淀完全,又知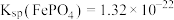 ,
, ,则要使滤液2中铁离子沉淀完全且不生成
,则要使滤液2中铁离子沉淀完全且不生成 沉淀,应控制
沉淀,应控制
___________ 。[已知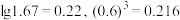 ]
]
(7)科研人员新研发了一种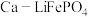 可充电电池,工作原理如图,电池总反应为
可充电电池,工作原理如图,电池总反应为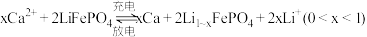
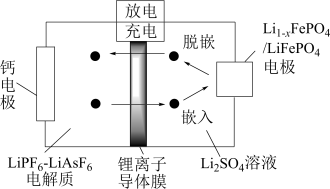
①充电时,钙电极与电源___________ 相连。
②放电时的正极反应式为___________________________ 。
 是重要的锂电池正极材料,一种利用硫酸法生产钛白粉过程的副产物硫酸亚铁(含钛、铜、锰、铅、锌、钙、镁等杂质离子)制备磷酸亚铁锂的生产流程如图.
是重要的锂电池正极材料,一种利用硫酸法生产钛白粉过程的副产物硫酸亚铁(含钛、铜、锰、铅、锌、钙、镁等杂质离子)制备磷酸亚铁锂的生产流程如图.
常温下各种硫化物溶度积常数如下:
物质 |
|
|
|
|
|
|
|
|
|
|
|
(1)为提高硫酸亚铁浸取速率,可以采取的措施是
(2)基态亚铁离子的电子排布式为
(3)磷元素可以形成多种含氧酸,亚磷酸
 结构如图所示,则亚磷酸属于
结构如图所示,则亚磷酸属于
(4)在滤液2中加入磷酸需控制
 ,其目的是①磷酸根过量,可以减少铁的其他形式的沉淀,提高
,其目的是①磷酸根过量,可以减少铁的其他形式的沉淀,提高 的纯度;②
的纯度;②(5)聚丙烯的作用是
(6)已知当溶液中
 时视为沉淀完全,又知
时视为沉淀完全,又知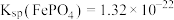 ,
, ,则要使滤液2中铁离子沉淀完全且不生成
,则要使滤液2中铁离子沉淀完全且不生成 沉淀,应控制
沉淀,应控制
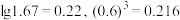 ]
](7)科研人员新研发了一种
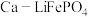 可充电电池,工作原理如图,电池总反应为
可充电电池,工作原理如图,电池总反应为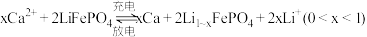

①充电时,钙电极与电源
②放电时的正极反应式为
您最近一年使用:0次
解题方法
6 . 根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有等体积、等浓度的 溶液的两支试管中分别加入 溶液的两支试管中分别加入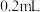 等浓度 等浓度 溶液和 溶液和 溶液 溶液 | 加 溶液的试管中产生气泡速率更快 溶液的试管中产生气泡速率更快 |  比 比 的催化效果好 的催化效果好 |
| B | 向盛有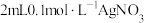 溶液的试管中滴加 溶液的试管中滴加 溶液,再向其中滴加 溶液,再向其中滴加 滴 滴 溶液. 溶液. | 先有白色沉淀生成,后又产生黄色沉淀 |  |
| C | 向苯酚浊液中滴加少量 溶液 溶液 | 浊液变澄清 | 酸性:苯酚> |
| D | 向某溶液中滴加 溶液并将湿润的红色石蕊试纸置于试管口 溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 能正确表示下列反应的离子方程式为
A.用碳酸钠溶液处理水垢中的硫酸钙: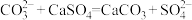 |
B. 溶液中能入少量的 溶液中能入少量的 : :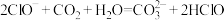 |
C.明矾净水原理: |
D.氯化铜溶液中通入硫化氢: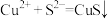 |
您最近一年使用:0次
8 . 由下列实验操作及现象能得出相应结论的是
| 实验操作 | 现象 | 结论 | |
| A | 用相同浓度的NaOH溶液分别滴定等体积等pH的HA和HB溶液 | HA溶液消耗NaOH溶液体积多 | HA酸性强于HB |
| B | 向盛有少量水的试管中滴加2滴K3[Fe(CN)6]溶液,然后滴加2滴KSCN溶液 | 溶液未变红 | CN-的配位能力强于SCN- |
| C | 向浓度均为0.1mol•L-1的NaCl和NaI的混合溶液中滴加少量AgNO3溶液 | 产生黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| D | 常温下,向0.1mol•L﹣1NaHCO3溶液中滴加酚酞 | 溶液变红 |  >Ka2 >Ka2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-13更新
|
50次组卷
|
2卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
9 . 常温下,向含 、
、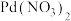 和
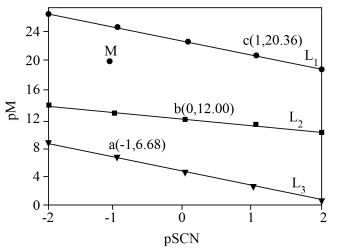
和 的溶液中滴加KSCN溶液,浊液中
的溶液中滴加KSCN溶液,浊液中 [
[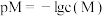 ,
,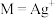 、
、 或
或 ]与
]与 的关系如图所示。已知:常温下,
的关系如图所示。已知:常温下,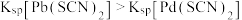 ,平衡常数K大于
,平衡常数K大于 时认为该反应能完全进行。
时认为该反应能完全进行。
下列叙述错误的是
 、
、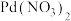 和
和 的溶液中滴加KSCN溶液,浊液中
的溶液中滴加KSCN溶液,浊液中 [
[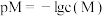 ,
,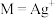 、
、 或
或 ]与
]与 的关系如图所示。已知:常温下,
的关系如图所示。已知:常温下,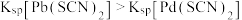 ,平衡常数K大于
,平衡常数K大于 时认为该反应能完全进行。
时认为该反应能完全进行。
下列叙述错误的是
A.直线 代表pPd与pSCN的关系 代表pPd与pSCN的关系 |
B.饱和AgSCN溶液中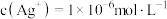 |
C.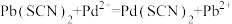 不可逆 不可逆 |
D.M点溶液可析出AgSCN和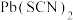 |
您最近一年使用:0次
2024-03-10更新
|
253次组卷
|
2卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
名校
10 . 锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是ZnS,含少量FeS等杂质)为原料采用多种方法冶炼锌,流程如图。回答下列问题:

已知:① 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应: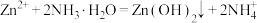 、
、
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
(1)已知 中
中 采用
采用 杂化,则
杂化,则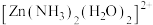 有
有___________ 种结构。
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,……然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红……冷定,毁罐取出。……即倭铅也。”(炉甘石主要成分是 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的___________ (填标号,下同)。从环保的角度来看,这三种方法中,最佳方法是___________ 。
a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为___________ 。
(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是___________ 。
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为___________ 。航母外壳常镶嵌一些锌块,这种保护航母的方法叫___________ 。
(6)通常认为离子浓度 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算
___________ 。

已知:①
 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应: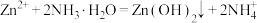 、
、
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | 6.5 | 9.7 |
 | 5.4 | 8.0 |
 | 2.3 | 4.1 |
 中
中 采用
采用 杂化,则
杂化,则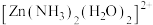 有
有(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,……然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红……冷定,毁罐取出。……即倭铅也。”(炉甘石主要成分是
 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入
 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为
(6)通常认为离子浓度
 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算
您最近一年使用:0次