名校
1 . 一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述不正确的是
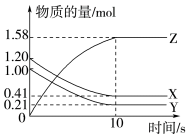
| A.反应开始到10 s,用Z表示的反应速率为0.158 mol·L-1·s-1 |
| B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10 s时,Y的转化率为79.0% |
| D.反应的化学方程式为X(g)+Y(g)⇌Z(g) |
您最近半年使用:0次
名校
解题方法
2 . 按要求回答下列问题:
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、
)、 、
、 等物质。
等物质。
①汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是_______ (填字母)。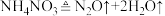 ,推测安全气囊中
,推测安全气囊中 的作用有
的作用有_______ 。
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。_______ 转化为化学能。
②根据数据计算,分解1 mol 需
需_______ (填“吸收”或“释放”)_______ kJ的能量。
(3)汽车尾气净化装置中,三元催化剂能将一氧化碳、碳氢化合物和氮氧化物转化为无毒气体,某研究小组模拟实验,计算反应速率。一定条件下,在2 L密闭容器内,反应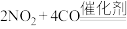
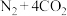 ,
,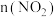 时间变化如表:
时间变化如表:
0~2s内用CO表示该反应的平均速率为_______ 。
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: 。
。
①能说明该反应已达到平衡状态的标志是_______ (填标号)
A.反应速率
B.容器内压强不再随时间而发生变化
C.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
D.容器内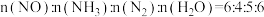
②某次实验中测得容器内NO及 的物质的量随时间变化如图。
的物质的量随时间变化如图。
_______  (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是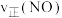
_______ 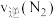 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠(
 )、
)、 、
、 等物质。
等物质。①汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是A.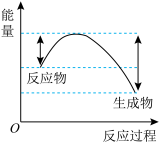 B.
B.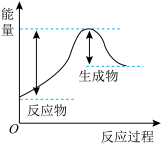 C.
C.
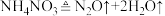 ,推测安全气囊中
,推测安全气囊中 的作用有
的作用有(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
②根据数据计算,分解1 mol
 需
需(3)汽车尾气净化装置中,三元催化剂能将一氧化碳、碳氢化合物和氮氧化物转化为无毒气体,某研究小组模拟实验,计算反应速率。一定条件下,在2 L密闭容器内,反应
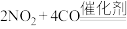
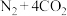 ,
,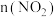 时间变化如表:
时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
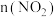 /mol /mol | a | b | c | d | e | f |
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: 。
。①能说明该反应已达到平衡状态的标志是
A.反应速率

B.容器内压强不再随时间而发生变化
C.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化D.容器内
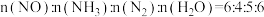
②某次实验中测得容器内NO及
 的物质的量随时间变化如图。
的物质的量随时间变化如图。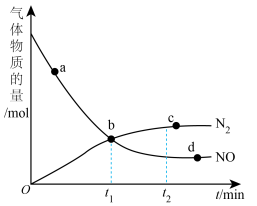

 (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是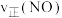
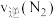 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近半年使用:0次
3 . 甲醇(CH3OH)是重要的化工原料,应用前景广阔。回答下列问题:
Ⅰ.某温度下,二氧化碳加氢制甲醇的总反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g),将8 mol CO2和8 mol H2充入2 L的恒温刚性密闭容器中,测得氢气物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),将8 mol CO2和8 mol H2充入2 L的恒温刚性密闭容器中,测得氢气物质的量随时间变化如图所示。___ (填序号)。
A.容器内气体的压强保持不变 B.混合气体的平均相对分子质量不变
C.υ逆(CO2)=3υ正(H2) D.混合气体的密度不变
E.n(CO2):n(H2)保持不变 F.CO2的物质的量分数不变
(2)a点正反应速率_______ (填“大于”、“等于”或“小于”)b点逆反应速率。
(3)前12min,用CH3OH表示的反应速率为_____ 。平衡时CO2 的转化率为___ 。(计算结果均保留两位有效数字)
Ⅱ.甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,工作原理如下图所示;_____ (填“正”或“负”)极,该电极反应式为_____ 。
(5)当电路中通过2mol电子时,消耗O2的体积为_____ L(标准状况);电极B附近溶液的碱性_____ (填“增强”、“减弱”或“不变”)。
Ⅰ.某温度下,二氧化碳加氢制甲醇的总反应为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),将8 mol CO2和8 mol H2充入2 L的恒温刚性密闭容器中,测得氢气物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),将8 mol CO2和8 mol H2充入2 L的恒温刚性密闭容器中,测得氢气物质的量随时间变化如图所示。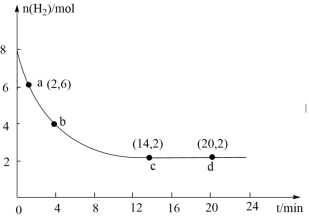
A.容器内气体的压强保持不变 B.混合气体的平均相对分子质量不变
C.υ逆(CO2)=3υ正(H2) D.混合气体的密度不变
E.n(CO2):n(H2)保持不变 F.CO2的物质的量分数不变
(2)a点正反应速率
(3)前12min,用CH3OH表示的反应速率为
Ⅱ.甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,工作原理如下图所示;
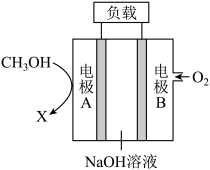
(5)当电路中通过2mol电子时,消耗O2的体积为
您最近半年使用:0次
4 . 2L的恒温密闭容器中,充入2molA和3molB发生反应2A(s)+3B(g)  C(g)+2D(g),经2min后B的浓度减少0.3mol·L-1.下列说法正确的是
C(g)+2D(g),经2min后B的浓度减少0.3mol·L-1.下列说法正确的是
 C(g)+2D(g),经2min后B的浓度减少0.3mol·L-1.下列说法正确的是
C(g)+2D(g),经2min后B的浓度减少0.3mol·L-1.下列说法正确的是| A.用A表示2min内的反应速率是0.1mol·L-1·min-1 |
| B.2min末容器内气体的压强比起始时压强小 |
| C.当C、D浓度之比不变时说明反应达平衡状态 |
| D.缩小容器体积,正、逆反应速率均增大 |
您最近半年使用:0次
解题方法
5 . 在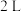 恒容密闭容器中加入足量的炭和
恒容密闭容器中加入足量的炭和 水蒸气发生反应
水蒸气发生反应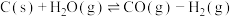 ,
, 时测得
时测得 的物质的量浓度为
的物质的量浓度为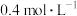 。下列说法正确的是
。下列说法正确的是
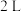 恒容密闭容器中加入足量的炭和
恒容密闭容器中加入足量的炭和 水蒸气发生反应
水蒸气发生反应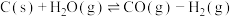 ,
, 时测得
时测得 的物质的量浓度为
的物质的量浓度为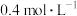 。下列说法正确的是
。下列说法正确的是A. | B. 时 时 的转化率为 的转化率为 |
C.因C足量,所以 可以完全转化 可以完全转化 | D. 时 时 |
您最近半年使用:0次
解题方法
6 . 某温度时,在 容器中,
容器中, 、
、 、
、 三种气体物质的量的变化曲线如图所示。下列说法错误的是
三种气体物质的量的变化曲线如图所示。下列说法错误的是
 容器中,
容器中, 、
、 、
、 三种气体物质的量的变化曲线如图所示。下列说法错误的是
三种气体物质的量的变化曲线如图所示。下列说法错误的是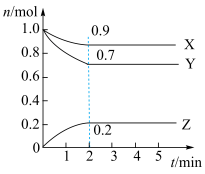
A.反应方程式为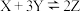 |
B.该反应条件下, 时 时 的转化率达到最大 的转化率达到最大 |
C.第 时的化学反应速率 时的化学反应速率 |
D. 后虽然 后虽然 的浓度不再变化,但 的浓度不再变化,但 仍在发生反应 仍在发生反应 |
您最近半年使用:0次
7 . 一定温度下,在容积为VL的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:___________ ;
(2)t 1到t 2时刻,以M的浓度变化表示的平均反应速率为:___________ ;(用符号表示)
(3)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol⋅L−1⋅min−1,则此容器的容积为V=___________ L。

(2)t 1到t 2时刻,以M的浓度变化表示的平均反应速率为:
(3)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol⋅L−1⋅min−1,则此容器的容积为V=
您最近半年使用:0次
8 . 化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在 稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大___________ min(填“0~1”、“1~2”、“2~3”、“3~4”或“4~5”),原因是___________ 。
②2~3min内,以盐酸的浓度变化表示的平均反应速率为___________ mol/(L·min) (设溶液体积不变)。
(2)某温度下在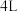 恒容密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
恒容密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:___________ mol/L,该反应的化学方程式是___________ 。
②5min时,Z的生成速率___________ (填“大于”、“小于”或“等于”)6min时Z的生成速率。
③若升高温度,则逆反应速率___________ (填“增大”、“减小”或“不变”)。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在
 稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 109 | 220 | 332 | 412 | 480 |
②2~3min内,以盐酸的浓度变化表示的平均反应速率为
(2)某温度下在
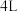 恒容密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示:
恒容密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图所示: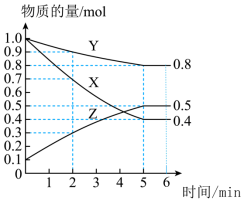
②5min时,Z的生成速率
③若升高温度,则逆反应速率
您最近半年使用:0次
9 . 学习化学反应速率和限度能够指导促进工业生产。
Ⅰ.汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成NO的能量变化如图所示,
等污染大气,其中生成NO的能量变化如图所示,_______ ;若反应生成2molNO气体应_______ (填“释放”或“吸收”)_______ kJ能量。
Ⅱ.某研究小组用CO和H2模拟工业合成甲醇,发生反应: 在1L的恒容密闭容器内充入1molCO和2mol
在1L的恒容密闭容器内充入1molCO和2mol ,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
(2)①下列说法正确的是_______ (填标号)。
a.容器内气体的密度不变,则反应达到平衡
b.容器内气体的平均相对分子质量不变,则反应达到平衡
c.若向平衡体系中充入Ar后,甲醇的生成速率降低
d.容器内CO和 物质的量之比不变,则反应达到平衡
物质的量之比不变,则反应达到平衡
e.CO的转化率不再变化,则反应达到平衡
②从反应开始到20min时, 的平均反应速率为
的平均反应速率为_______ 。
③该条件下,反应 达到平衡时CO的转化率为
达到平衡时CO的转化率为_______ 。
(3)从断键和成键角度分析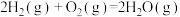 反应中能量的变化。部分化学键的键能如下表:
反应中能量的变化。部分化学键的键能如下表:
则生成 放出热量
放出热量_______ kJ。
(4)NaClO溶液在不同温度下可对烟气中的硫、硝脱除,一定时间内,其脱除率如图所示: 脱除率高于NO,可能的原因是
脱除率高于NO,可能的原因是_______ 。
②烟气中 和NO体积比为4:1,烟气与50℃时的吸收液转化生成的
和NO体积比为4:1,烟气与50℃时的吸收液转化生成的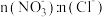 =
=_______ 。
Ⅰ.汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成NO的能量变化如图所示,
等污染大气,其中生成NO的能量变化如图所示,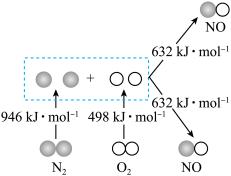
Ⅱ.某研究小组用CO和H2模拟工业合成甲醇,发生反应:
 在1L的恒容密闭容器内充入1molCO和2mol
在1L的恒容密闭容器内充入1molCO和2mol ,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:| 反应时间/min0 | 0 | 5 | 10 | 15 | 20 | 30 |
| 压强/MPa | 25.2 | 21.6 | 18.9 | 17.4 | 16.8 | 16.8 |
(2)①下列说法正确的是
a.容器内气体的密度不变,则反应达到平衡
b.容器内气体的平均相对分子质量不变,则反应达到平衡
c.若向平衡体系中充入Ar后,甲醇的生成速率降低
d.容器内CO和
 物质的量之比不变,则反应达到平衡
物质的量之比不变,则反应达到平衡e.CO的转化率不再变化,则反应达到平衡
②从反应开始到20min时,
 的平均反应速率为
的平均反应速率为③该条件下,反应
 达到平衡时CO的转化率为
达到平衡时CO的转化率为(3)从断键和成键角度分析
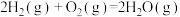 反应中能量的变化。部分化学键的键能如下表:
反应中能量的变化。部分化学键的键能如下表:| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 放出热量
放出热量(4)NaClO溶液在不同温度下可对烟气中的硫、硝脱除,一定时间内,其脱除率如图所示:
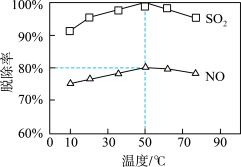
 脱除率高于NO,可能的原因是
脱除率高于NO,可能的原因是②烟气中
 和NO体积比为4:1,烟气与50℃时的吸收液转化生成的
和NO体积比为4:1,烟气与50℃时的吸收液转化生成的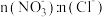 =
=
您最近半年使用:0次
解题方法
10 . 为了实现“碳中和”, 的综合利用成为科学家研究的热点。
的综合利用成为科学家研究的热点。
(1)将 催化加氢制取
催化加氢制取 ,通过下列步骤实现,反应过程中能量变化如图1所示。
,通过下列步骤实现,反应过程中能量变化如图1所示。

___________  。
。
(2)在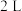 的绝热密闭容器中,按
的绝热密闭容器中,按 充入
充入 和
和 ,在催化剂作用下合成甲醇。下列说法中说明主反应
,在催化剂作用下合成甲醇。下列说法中说明主反应 达到平衡状态的是___________(填字母)。
达到平衡状态的是___________(填字母)。
(3)在密闭容器中通入 和
和 的混合气体,制取甲醇过程中,存在竞争反应:
的混合气体,制取甲醇过程中,存在竞争反应:
 .
. ;
;
 .
.
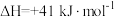 。
。
在不同压强下,当按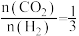 进料,反应达到平衡时,测得甲醇的物质的量分数与温度的关系如图2所示物质ⅰ的物质的量分数:
进料,反应达到平衡时,测得甲醇的物质的量分数与温度的关系如图2所示物质ⅰ的物质的量分数: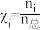 )
)___________ ,判断的依据是___________ 。
②图2中,当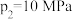 、发生上述反应,反应
、发生上述反应,反应 达到平衡时,
达到平衡时,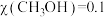 ,则在
,则在 内用
内用 的分压变化表示的速率
的分压变化表示的速率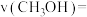
___________ 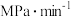 ,此时反应I中
,此时反应I中 的转化率为
的转化率为___________ (保留小数点后1位)。
③在压强为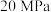 时,发生上述反应并达到平衡状态,
时,发生上述反应并达到平衡状态, 平衡转化率为
平衡转化率为 ,
,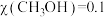 ,该温度下反应
,该温度下反应 的平衡常数
的平衡常数
___________ (保留1位有效数字,用各组分的分压代替浓度计算平衡常数 ,气体分压=总压×物质的量分数)。
,气体分压=总压×物质的量分数)。
 的综合利用成为科学家研究的热点。
的综合利用成为科学家研究的热点。(1)将
 催化加氢制取
催化加氢制取 ,通过下列步骤实现,反应过程中能量变化如图1所示。
,通过下列步骤实现,反应过程中能量变化如图1所示。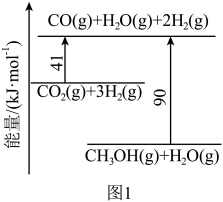


 。
。(2)在
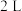 的绝热密闭容器中,按
的绝热密闭容器中,按 充入
充入 和
和 ,在催化剂作用下合成甲醇。下列说法中说明主反应
,在催化剂作用下合成甲醇。下列说法中说明主反应 达到平衡状态的是___________(填字母)。
达到平衡状态的是___________(填字母)。A. 的转化率保持不变 的转化率保持不变 | B.混合气体的密度保持不变 |
C.断裂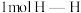 键同时形成 键同时形成 键 键 | D.容器内混合气体温度保持不变 |
(3)在密闭容器中通入
 和
和 的混合气体,制取甲醇过程中,存在竞争反应:
的混合气体,制取甲醇过程中,存在竞争反应: .
. ;
; .
.
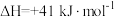 。
。在不同压强下,当按
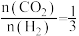 进料,反应达到平衡时,测得甲醇的物质的量分数与温度的关系如图2所示物质ⅰ的物质的量分数:
进料,反应达到平衡时,测得甲醇的物质的量分数与温度的关系如图2所示物质ⅰ的物质的量分数: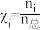 )
)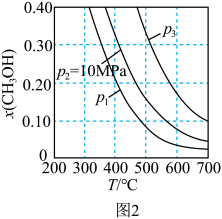
②图2中,当
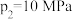 、发生上述反应,反应
、发生上述反应,反应 达到平衡时,
达到平衡时,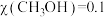 ,则在
,则在 内用
内用 的分压变化表示的速率
的分压变化表示的速率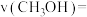
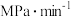 ,此时反应I中
,此时反应I中 的转化率为
的转化率为③在压强为
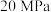 时,发生上述反应并达到平衡状态,
时,发生上述反应并达到平衡状态, 平衡转化率为
平衡转化率为 ,
,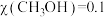 ,该温度下反应
,该温度下反应 的平衡常数
的平衡常数
 ,气体分压=总压×物质的量分数)。
,气体分压=总压×物质的量分数)。
您最近半年使用:0次



