名校
解题方法
1 . 氮氧化物(NO、 )、
)、 是大气污染物,但在生活、生产中又有着广泛应用。
是大气污染物,但在生活、生产中又有着广泛应用。
Ⅰ.如图所示是酸雨的形成示意图。_______ (用化学方程式表示)。
(2)你认为减少酸雨的产生可采取的措施是_______(填字母)。
①减少用煤作燃料②开发新能源③化石燃料脱硫④在已酸化的土壤中洒石灰⑤监测并治理汽车排出的大量尾气⑥收集大气中氮氧化物制备硝酸
Ⅱ.某学习小组在实验室中利用下图装置制备 并进行相关性质的探究。
并进行相关性质的探究。_______ ;装置A中反应的化学方程式为_______ 。
(4)装置B是为了观察气体的流速,则试剂M为_______(填字母)。
(5)装置E中出现_______ (填现象)可说明 具有还原性。
具有还原性。
(6)装置F中过量的NaOH溶液吸收尾气发生的离子方程式为_______ 。
(7)装置C中反应的离子方程式是_______ ,甲同学设计了以下三个方案用于证实此反应中 具有还原性,你认为方案正确的是
具有还原性,你认为方案正确的是_______ 。
a.反应后溶液由黄色变为浅绿色
b.取反应后的少许溶液于试管中,加入 溶液,产生白色沉淀
溶液,产生白色沉淀
c.取反应后的少许溶液于试管中,加入 溶液,产生白色沉淀
溶液,产生白色沉淀
乙同学查阅资料发现反应分为两步:
第一步: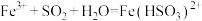 (棕红色)
(棕红色)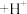 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
由此乙同学预测实验现象是_______ 。
(8)实验开始后,发现装置D中的溶液迅速变黄,继续通入 ,装置D中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
,装置D中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: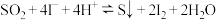 。有同学认为除
。有同学认为除 的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证(
的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证( 体积已折算为标准状况下体积)。
体积已折算为标准状况下体积)。
限选试剂:0.1mol/LKI溶液、1.0mol/LKI溶液、2.0mol/LKI溶液、蒸馏水、浓硝酸、浓盐酸
Ⅲ.电化学法处理 是目前研究的热点。利用过氧化氢吸收
是目前研究的热点。利用过氧化氢吸收 可消除
可消除 污染,设计装置如图所示(质子即
污染,设计装置如图所示(质子即 )。
)。_______ (填“正极”或“负极”)。
(10)石墨2的电极反应式为_______ 。
(11)若22.4L(标准状况) 参与反应,则迁移
参与反应,则迁移 的物质的量为
的物质的量为_______ mol。
Ⅳ.
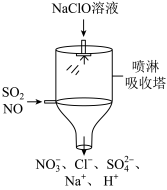
(12)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。其中,脱硝(NO)反应的离子方程式为_______ 。
 )、
)、 是大气污染物,但在生活、生产中又有着广泛应用。
是大气污染物,但在生活、生产中又有着广泛应用。Ⅰ.如图所示是酸雨的形成示意图。

| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.75 | 4.60 | 4.58 | 4.50 | 4.50 |
(2)你认为减少酸雨的产生可采取的措施是_______(填字母)。
①减少用煤作燃料②开发新能源③化石燃料脱硫④在已酸化的土壤中洒石灰⑤监测并治理汽车排出的大量尾气⑥收集大气中氮氧化物制备硝酸
| A.①②③④⑤⑥ | B.①②③⑤ | C.①②③④⑤ | D.②③⑤⑥ |
Ⅱ.某学习小组在实验室中利用下图装置制备
 并进行相关性质的探究。
并进行相关性质的探究。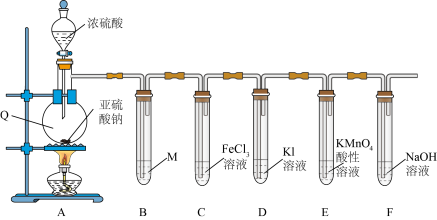
(4)装置B是为了观察气体的流速,则试剂M为_______(填字母)。
| A.NaOH溶液 | B.饱和 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(5)装置E中出现
 具有还原性。
具有还原性。(6)装置F中过量的NaOH溶液吸收尾气发生的离子方程式为
(7)装置C中反应的离子方程式是
 具有还原性,你认为方案正确的是
具有还原性,你认为方案正确的是a.反应后溶液由黄色变为浅绿色
b.取反应后的少许溶液于试管中,加入
 溶液,产生白色沉淀
溶液,产生白色沉淀c.取反应后的少许溶液于试管中,加入
 溶液,产生白色沉淀
溶液,产生白色沉淀乙同学查阅资料发现反应分为两步:
第一步:
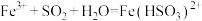 (棕红色)
(棕红色)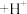 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)由此乙同学预测实验现象是
(8)实验开始后,发现装置D中的溶液迅速变黄,继续通入
 ,装置D中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
,装置D中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: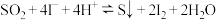 。有同学认为除
。有同学认为除 的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证(
的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证( 体积已折算为标准状况下体积)。
体积已折算为标准状况下体积)。限选试剂:0.1mol/LKI溶液、1.0mol/LKI溶液、2.0mol/LKI溶液、蒸馏水、浓硝酸、浓盐酸
| 影响因素 | 编号 | 操作 | 现象 |
 | i | 取50mL | 溶液变为浅黄色 |
| ii | 取50mL1.0mo1/LKI溶液于锥形瓶中,向其中通入20mL | 溶液迅速变黄 | |
 | iii | 取50mL1.0mol/LKI溶液和 | 溶液迅速变黄 |
| iv | 取50mL1.0mol/LKI溶液和5mL | 溶液迅速变黄且出现乳黄色浑浊 |
Ⅲ.电化学法处理
 是目前研究的热点。利用过氧化氢吸收
是目前研究的热点。利用过氧化氢吸收 可消除
可消除 污染,设计装置如图所示(质子即
污染,设计装置如图所示(质子即 )。
)。
(10)石墨2的电极反应式为
(11)若22.4L(标准状况)
 参与反应,则迁移
参与反应,则迁移 的物质的量为
的物质的量为Ⅳ.
(12)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。其中,脱硝(NO)反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
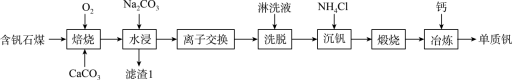
已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
②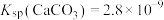 ,
,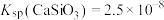 ,
,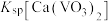 远大于
远大于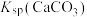 。
。
回答下列问题:
(1)基态Fe3+的价电子轨道表示式为______ 。
(2)“焙烧”时,V2O3、V2O4都转化为 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:____________ 。
(3)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有______ :“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是______ 。(列式计算平衡常数分析该反应进行的趋势,一般认为, 时反应进行较完全,
时反应进行较完全,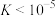 时反应难以进行)
时反应难以进行)
(4)“离子交换”与“洗脱”可表示为 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用______ 。
(5)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是____________ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是______(填字母)。

已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
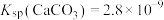 ,
,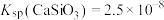 ,
,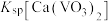 远大于
远大于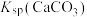 。
。回答下列问题:
(1)基态Fe3+的价电子轨道表示式为
(2)“焙烧”时,V2O3、V2O4都转化为
 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:(3)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
 时反应进行较完全,
时反应进行较完全,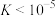 时反应难以进行)
时反应难以进行)(4)“离子交换”与“洗脱”可表示为
 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(5)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是______(填字母)。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
解题方法
3 . 铅(Pb)元素的主要化合价有+2价和+4价,溶液中铅为+2价(Pb2+或 ,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
,铅单质及其化合物在日常生活和工业生产中具有非常广泛的用途。
(1)Pb3O4 俗名红丹,在涂料工业中用作防锈颜料,Pb3O4中+2价铅和+4价铅的原子个数之比为
(2)Pb、PbO2可用于制造铅蓄电池,铅蓄电池工作时的反应方程式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,该反应中还原产物为
(3)工业上利用铅渣(主要成分是PbO、Pb,以及少量不溶于硝酸的杂质)生产PbSO4的流程如图:
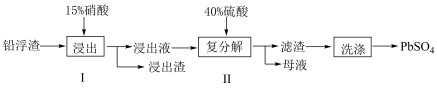
已知步骤1有NO产生,试写出Pb与硝酸反应的化学方程式
(4)血铅是指血液中铅元素的含量。血铅超标会引起机体的神经系统、血液系统、消化系统的一系列异常表现。某人血液中铅的浓度为0.4μg/mL,若转化为物质的量浓度为
您最近一年使用:0次
解题方法
4 . Co2O3主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含Co、Fe,还含有少量的CoO、FeO,Fe2O3、CaO、SiO2)制备氧化钴(Co2O3)的工艺流程如图所示。
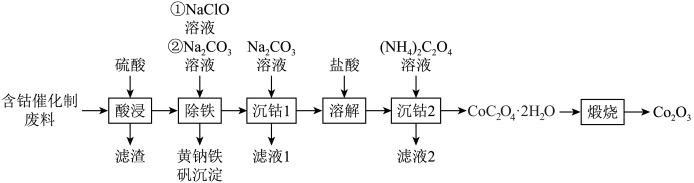
已知:ⅰ.黄钠铁矾的化学式为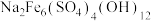 ;
;
ⅱ.金属钴与铁具有相似的化学性质;
ⅲ.氧化性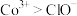 。
。
回答下列问题:
(1)钴元素基态原子的电子排布式为_______ 。
(2)“酸浸”时滤渣的主要成分为_______ (填化学式)。
(3)“除铁”时先加入NaClO溶液,主要发生反应的离子方程式为_______ ,再加入 溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
(4)常温下,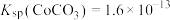 ,
,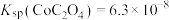 ,向
,向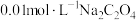 溶液中加入足量
溶液中加入足量 固体,能否生成
固体,能否生成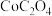 沉淀?
沉淀?_______ (通过计算说明)。
(5)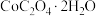 在空气中加热煅烧得到
在空气中加热煅烧得到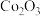 的化学方程式为
的化学方程式为_______ 。
(6)(a)钴被称为无机配合物之王,配合物 的中心离子的配位数为
的中心离子的配位数为_______ 。
(b)钴的一种化合物的晶胞结构如图所示。
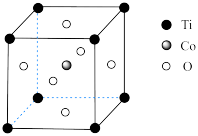
①晶体中一个Ti周围与其最近的O的个数为_______ 。
②在该晶胞中氧、钴、钛的粒子个数比为_______ 。

已知:ⅰ.黄钠铁矾的化学式为
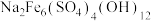 ;
;ⅱ.金属钴与铁具有相似的化学性质;
ⅲ.氧化性
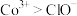 。
。回答下列问题:
(1)钴元素基态原子的电子排布式为
(2)“酸浸”时滤渣的主要成分为
(3)“除铁”时先加入NaClO溶液,主要发生反应的离子方程式为
 溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。(4)常温下,
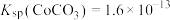 ,
,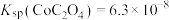 ,向
,向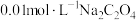 溶液中加入足量
溶液中加入足量 固体,能否生成
固体,能否生成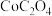 沉淀?
沉淀?(5)
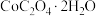 在空气中加热煅烧得到
在空气中加热煅烧得到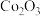 的化学方程式为
的化学方程式为(6)(a)钴被称为无机配合物之王,配合物
 的中心离子的配位数为
的中心离子的配位数为(b)钴的一种化合物的晶胞结构如图所示。

①晶体中一个Ti周围与其最近的O的个数为
②在该晶胞中氧、钴、钛的粒子个数比为
您最近一年使用:0次
名校
解题方法
5 . 氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。错误 的是

A.过程①: |
B.过程②总反应式: |
C.过程③: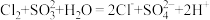 |
D. 溶于水: 溶于水: |
您最近一年使用:0次
2024-03-06更新
|
983次组卷
|
5卷引用:广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题
广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题福建省泉州市2024届高三下学期高中毕业班质量监测(三)化学试卷云南省云南师范大学实验中学2023-2024学年高一下学期三月月考化学试题(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
6 . 碳酸锰MnCO3是制造电信器材的软磁铁氧体,也用作脱硫的催化剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO2,还含有Fe2O3、CaCO3、CuO等杂质)制取碳酸锰的流程如图所示:

已知:①还原焙烧的主反应为2MnO2+C=2MnO+CO2↑
②氧化能力S2O >MnO
>MnO >
>
可能用到的数据如下:
根据要求回答下列问题:
(1)基态锰原子的价层电子排布式为_____ ,
(2)在实验室进行步骤A操作时,可能用到的主要仪器为_____ 。
A.坩埚 B.蒸发皿 C.烧杯
(3)步骤E中调节3.7<pH<8.3,其目的是_____ 。
(4)步骤G发生的离子方程式为___ ,若Mn2+恰好沉淀完全时测得溶液中CO 的浓度为2.2×10-6mol•L-1,则Ksp(MnCO3)=
的浓度为2.2×10-6mol•L-1,则Ksp(MnCO3)=_____ (mol/L)2。
(5)实验室可以用Na2S2O8溶液来检验Mn2+是否完全发生反应,S2O 中存在过氧键(-O-O-),请问S2O
中存在过氧键(-O-O-),请问S2O 中S的化合价为
中S的化合价为_____ 。请写出对应的离子方程式_____ 。

已知:①还原焙烧的主反应为2MnO2+C=2MnO+CO2↑
②氧化能力S2O
 >MnO
>MnO >
>
可能用到的数据如下:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 1.5 | 6.5 | 4.2 | 8.3 |
| 沉淀完全pH | 3.7 | 9.7 | 7.4 | 9.8 |
(1)基态锰原子的价层电子排布式为
(2)在实验室进行步骤A操作时,可能用到的主要仪器为
A.坩埚 B.蒸发皿 C.烧杯
(3)步骤E中调节3.7<pH<8.3,其目的是
(4)步骤G发生的离子方程式为
 的浓度为2.2×10-6mol•L-1,则Ksp(MnCO3)=
的浓度为2.2×10-6mol•L-1,则Ksp(MnCO3)=(5)实验室可以用Na2S2O8溶液来检验Mn2+是否完全发生反应,S2O
 中存在过氧键(-O-O-),请问S2O
中存在过氧键(-O-O-),请问S2O 中S的化合价为
中S的化合价为
您最近一年使用:0次
名校
解题方法
7 . I.某化学自主实验小组利用如图所示装置探究 能否被
能否被 还原
还原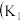 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。________ 。 装置发生的化学反应方程式为
装置发生的化学反应方程式为_________ 。
(2)甲、乙分别是___________  填标号
填标号 。
。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下: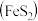 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:___________ 。
(6)写出催化反应室中SO2被氧化为SO3的化学方程式___________ 。
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用___________ 吸收。
 能否被
能否被 还原
还原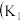 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。
 装置发生的化学反应方程式为
装置发生的化学反应方程式为(2)甲、乙分别是
 填标号
填标号 。
。a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若
 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:(4)此实验装置存在一个明显的缺陷是
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:
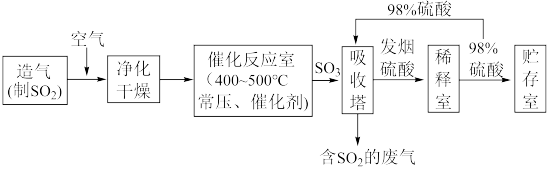
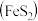 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:(6)写出催化反应室中SO2被氧化为SO3的化学方程式
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用
您最近一年使用:0次
2024-02-24更新
|
720次组卷
|
4卷引用:广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
8 . 某小组在实验室用NaClO溶液和NH3反应制备肼(N2H4),并进行相关性质探究实验。
Ⅰ.实验室制备N2H4
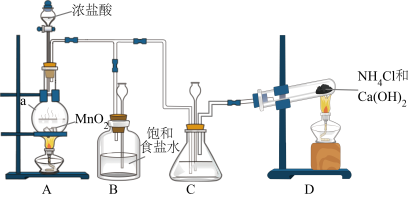
(1)装置D中反应的化学方程式是___________ 。
(2)装置C中盛放的试剂是___________ 。
(3)制备N2H4的离子方程式___________ 。
Ⅱ.测定产品中水合肼(N2H4·H2O)的含量
(4)称取产品6.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.3000mol/L的碘标准溶液滴定(已知:N2H4·H2O +2I2 = N2↑+ 4HI + H2O)。
①滴定到达终点的现象是___________ 。
②重复上述滴定实验2~3次,测得消耗碘标准溶液的平均值为20.00mL,产品中水合肼的质量分数为___________ 。
Ⅲ.探究肼的化学性质。将制得的肼分离提纯后,进行如下实验。
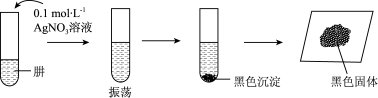
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】
(5)设计如下方案,进行实验。
③综合上述实验,肼具有的性质是___________
(6)N2H4是一种二元弱碱,在水中的电离与NH3相似,写出肼的第一步电离方程式___________
Ⅰ.实验室制备N2H4

(1)装置D中反应的化学方程式是
(2)装置C中盛放的试剂是
(3)制备N2H4的离子方程式
Ⅱ.测定产品中水合肼(N2H4·H2O)的含量
(4)称取产品6.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.3000mol/L的碘标准溶液滴定(已知:N2H4·H2O +2I2 = N2↑+ 4HI + H2O)。
①滴定到达终点的现象是
②重复上述滴定实验2~3次,测得消耗碘标准溶液的平均值为20.00mL,产品中水合肼的质量分数为
Ⅲ.探究肼的化学性质。将制得的肼分离提纯后,进行如下实验。

【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】
(5)设计如下方案,进行实验。
| 操作 | 现象 | 结论 |
| ⅰ.取少量黑色固体于试管中,加入足量① | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ⅱ.取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ② | 黑色固体是Ag和Ag2O |
(6)N2H4是一种二元弱碱,在水中的电离与NH3相似,写出肼的第一步电离方程式
您最近一年使用:0次
解题方法
9 . 黑木耳是常见食品,可以补充入体所必需的微量元素铁,某兴趣小组设计实验,检验黑木耳中的铁元素,实验流程如图;
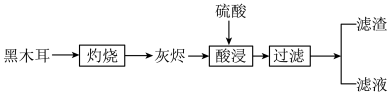
(1)灼烧黑木耳必须用到下列仪器中的___________(填字母)。
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是___________ 。
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有___________ ;另取滤液检验,滤液能使KMnO4溶液紫色褪去,说明滤液中存在具有___________ (填“氧化性”或“还原性”)的粒子。
(4)为进一步探究 Fe3+和 Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
(5)由 和硫黄制取
和硫黄制取 的废水中含有一定量的
的废水中含有一定量的 ,Cr元素含量达标才能排放,可以加入
,Cr元素含量达标才能排放,可以加入 溶液去除酸性废水中的
溶液去除酸性废水中的 ,使
,使 转化为
转化为 而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程
而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程 溶液与
溶液与 发生的反应中氧化剂与还原剂的物质的量之比为
发生的反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)某兴趣小组同学想根据上述反应原理测出某酸性废水中残留的 的物质的量浓度,采样后,经初步预算需要
的物质的量浓度,采样后,经初步预算需要 的
的 溶液240mL,配制该溶液时至少需称量
溶液240mL,配制该溶液时至少需称量___________ g 。下列操作会导致所配制的溶液物质的量浓度偏低的是
。下列操作会导致所配制的溶液物质的量浓度偏低的是___________ 。
A.配制前,容量瓶中有少量蒸馏水 B.定容时仰视容量瓶刻度线
C.向容量瓶转移溶液时有少量液体溅出 D.定容、摇匀后,发现液面低于刻度线
(7)往配制好的FeSO4溶液滴入少量的氢氧化钠溶液,出现的现象是___________ ,用化学方程式来解释该过程颜色变化的原因 ___________ 。

(1)灼烧黑木耳必须用到下列仪器中的___________(填字母)。
A. | B. | C. | D. |
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有
(4)为进一步探究 Fe3+和 Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
| 实验操作 | 实验现象 | 离子方程式 | 实验结论 |
| 向FeCl2溶液中添加新制氯水 | 溶液由浅绿色变为棕黄色 | ① | Fe2+具有还原性 |
| 向 FeCl3溶液加入足量的铁粉 | 铁粉逐渐溶解,溶液由棕黄色变为浅绿色 | Fe+2Fe3+=3Fe 2+ | ② |
(5)由
 和硫黄制取
和硫黄制取 的废水中含有一定量的
的废水中含有一定量的 ,Cr元素含量达标才能排放,可以加入
,Cr元素含量达标才能排放,可以加入 溶液去除酸性废水中的
溶液去除酸性废水中的 ,使
,使 转化为
转化为 而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程
而自身转化为三价铁,再放入沉淀池,达到指定标准后方可排放。上述过程 溶液与
溶液与 发生的反应中氧化剂与还原剂的物质的量之比为
发生的反应中氧化剂与还原剂的物质的量之比为(6)某兴趣小组同学想根据上述反应原理测出某酸性废水中残留的
 的物质的量浓度,采样后,经初步预算需要
的物质的量浓度,采样后,经初步预算需要 的
的 溶液240mL,配制该溶液时至少需称量
溶液240mL,配制该溶液时至少需称量 。下列操作会导致所配制的溶液物质的量浓度偏低的是
。下列操作会导致所配制的溶液物质的量浓度偏低的是A.配制前,容量瓶中有少量蒸馏水 B.定容时仰视容量瓶刻度线
C.向容量瓶转移溶液时有少量液体溅出 D.定容、摇匀后,发现液面低于刻度线
(7)往配制好的FeSO4溶液滴入少量的氢氧化钠溶液,出现的现象是
您最近一年使用:0次
10 . 废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是 、铝、炭黑及其他微量杂质,回收利用的流程如下:
、铝、炭黑及其他微量杂质,回收利用的流程如下:
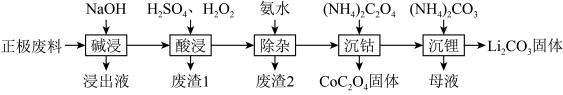
(1)“碱浸”步骤中铝溶解的离子方程式为________ ,“废渣1”的主要成分是_______ 。
(2)已知Li在化合物中显 价,
价, 中Co的化合价为
中Co的化合价为_____ ,“酸浸”步骤中 固体溶解的化学方程式为
固体溶解的化学方程式为_______ ,反应中 的作用为
的作用为_______ 。
(3)“酸浸”后的溶液中含有少量 、
、 、
、 ,滤渣2的主要成分是
,滤渣2的主要成分是______ 。
(4)沉钴过程发生的反应属于______ (填反应类型)。
(5)“母液”中的溶质成分是_______ ,生成 固体的离子方程式为
固体的离子方程式为________ 。
 、铝、炭黑及其他微量杂质,回收利用的流程如下:
、铝、炭黑及其他微量杂质,回收利用的流程如下:
(1)“碱浸”步骤中铝溶解的离子方程式为
(2)已知Li在化合物中显
 价,
价, 中Co的化合价为
中Co的化合价为 固体溶解的化学方程式为
固体溶解的化学方程式为 的作用为
的作用为(3)“酸浸”后的溶液中含有少量
 、
、 、
、 ,滤渣2的主要成分是
,滤渣2的主要成分是(4)沉钴过程发生的反应属于
(5)“母液”中的溶质成分是
 固体的离子方程式为
固体的离子方程式为
您最近一年使用:0次





