1 . 海水综合利用后的一种卤水中含NaCl、LiCl及少量的 、
、 、
、 等,利用该卤水制备
等,利用该卤水制备 的简要流程如图所示(第一次加入纯碱的量以不损失Li,其他离子尽量除去为标准):
的简要流程如图所示(第一次加入纯碱的量以不损失Li,其他离子尽量除去为标准):
①卤水中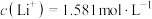 、
、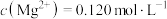 ;
;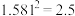 。
。
② 的溶解度随温度升高而降低。
的溶解度随温度升高而降低。
③常温下,几种难溶物质的溶度积数据如下表:
下列说法错误的是
 、
、 、
、 等,利用该卤水制备
等,利用该卤水制备 的简要流程如图所示(第一次加入纯碱的量以不损失Li,其他离子尽量除去为标准):
的简要流程如图所示(第一次加入纯碱的量以不损失Li,其他离子尽量除去为标准):
①卤水中
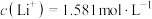 、
、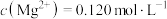 ;
;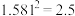 。
。②
 的溶解度随温度升高而降低。
的溶解度随温度升高而降低。③常温下,几种难溶物质的溶度积数据如下表:
物质 |
|
|
|
|
|
|
|
|
|
|
|
A.滤渣中含有 、 、 和 和 |
| B.在实验室中分离出滤渣需要的玻璃仪器主要为漏斗、玻璃棒和烧杯 |
C.“沉淀池Ⅱ”中滴加烧碱前, |
D.从“沉淀池Ⅲ”中析出的 需用热水洗涤 需用热水洗涤 |
您最近一年使用:0次
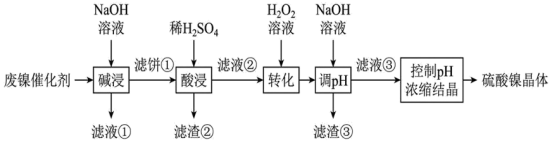
2 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属 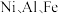 及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体 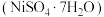 :
: 如表所示:
如表所示:
回答下列问题:
(1)“滤液②”中除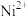 外还含有的金属离子
外还含有的金属离子___________ ;
(2)“转化”中可替代 的物质是
的物质是___________ (不能引入新的杂质离子);
由表格中的数据可求得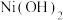 的
的 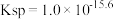 。如果“转化”后的溶液中
。如果“转化”后的溶液中 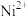 浓度为
浓度为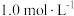 ,则除去杂质金属阳离子时“调
,则除去杂质金属阳离子时“调 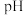 ”应控制的
”应控制的  范围是
范围是___________ 。
(3)硫酸镍在强碱溶液中用 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 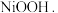 写出该反应的离子方程式
写出该反应的离子方程式___________ 。
(4)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。
(5)第Ⅷ族元素单质及其化合物在工业生产和科研领域有重要的用途。
①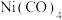 (该物质是配位化合物,且
(该物质是配位化合物,且  的结构式为
的结构式为  )常用作制备高纯镍粉,其熔点为
)常用作制备高纯镍粉,其熔点为 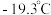 ,沸点为
,沸点为 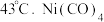 中
中  键和
键和  键的数目之比为
键的数目之比为___________ 。
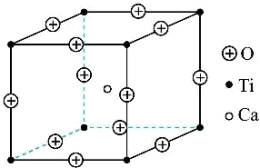
②在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示,在该晶胞中氧、钙、钛的粒子个数比是___________ 。
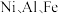 及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体 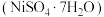 :
:
 如表所示:
如表所示:| 金属离子 | 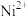 |  | 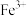 | 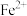 |
开始沉淀时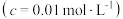 的  | 7.2 | 3.7 | 2.2 | 7.5 |
完全沉淀时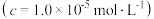 的  | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“滤液②”中除
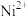 外还含有的金属离子
外还含有的金属离子(2)“转化”中可替代
 的物质是
的物质是由表格中的数据可求得
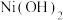 的
的 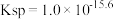 。如果“转化”后的溶液中
。如果“转化”后的溶液中 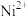 浓度为
浓度为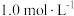 ,则除去杂质金属阳离子时“调
,则除去杂质金属阳离子时“调 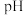 ”应控制的
”应控制的  范围是
范围是(3)硫酸镍在强碱溶液中用
 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 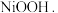 写出该反应的离子方程式
写出该反应的离子方程式(4)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
(5)第Ⅷ族元素单质及其化合物在工业生产和科研领域有重要的用途。
①
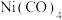 (该物质是配位化合物,且
(该物质是配位化合物,且  的结构式为
的结构式为  )常用作制备高纯镍粉,其熔点为
)常用作制备高纯镍粉,其熔点为 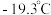 ,沸点为
,沸点为 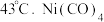 中
中  键和
键和  键的数目之比为
键的数目之比为②在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示,在该晶胞中氧、钙、钛的粒子个数比是
您最近一年使用:0次
名校
3 . 锌是一种重要的金属,锌及其化合物被广泛应用于汽车、建筑、船舶、电池等行业。现某科研小组以固体废锌催化剂(主要成分是 ,含少量
,含少量 、
、 、
、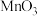 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。
②25℃时,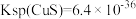 ,
,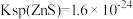
③深度除杂标准:溶液中 ≤2.0×10-6
≤2.0×10-6
(1)“浸取”温度为30℃,锌的浸出率可达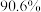 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为___________ 。
(2)“滤渣1”的主要成分为 、
、___________ 。
(3)“深度除锰”是将残留的 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式___________ 。
(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。 加入量最优选择
加入量最优选择___________ (填标号)
A.100% B.110% C.120% D.130%
②由图可知,当 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是___________ (用离子方程式解释)。
(5) 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:___________ 。
②键角③___________ 120°(填“<”或“=”)。
 ,含少量
,含少量 、
、 、
、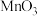 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: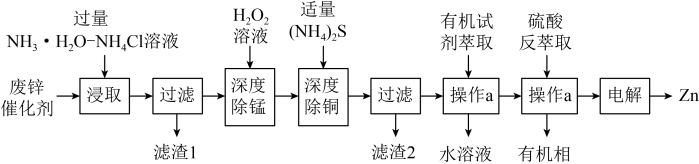
 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。②25℃时,
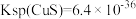 ,
,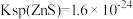
③深度除杂标准:溶液中
 ≤2.0×10-6
≤2.0×10-6(1)“浸取”温度为30℃,锌的浸出率可达
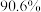 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为(2)“滤渣1”的主要成分为
 、
、(3)“深度除锰”是将残留的
 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比
 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。
 加入量最优选择
加入量最优选择A.100% B.110% C.120% D.130%
②由图可知,当
 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是(5)
 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图: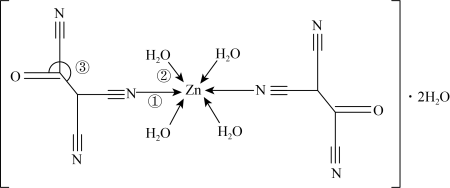
②键角③
您最近一年使用:0次
名校
4 . 二元有机酸( )的电离常数
)的电离常数 、
、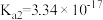 。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中
。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是 易溶于水。
易溶于水。
 )的电离常数
)的电离常数 、
、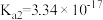 。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中
。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是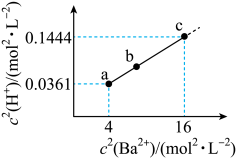
 易溶于水。
易溶于水。| A.NaHX溶液显碱性 |
B.溶度积 |
C.b点: |
D.若0.01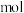 BaX溶于1L BaX溶于1L 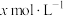 HY溶液中得到氢离子浓度与c点相等,则 HY溶液中得到氢离子浓度与c点相等,则 |
您最近一年使用:0次
5 . 25℃时,用NaOH溶液分别滴定HX、 、
、 三种溶液,
三种溶液, [M表示
[M表示 、
、 、
、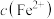 ]随pH变化关系如图所示,其中③的M代表
]随pH变化关系如图所示,其中③的M代表 。已知
。已知 ,下列有关分析不正确的是
,下列有关分析不正确的是
 、
、 三种溶液,
三种溶液, [M表示
[M表示 、
、 、
、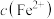 ]随pH变化关系如图所示,其中③的M代表
]随pH变化关系如图所示,其中③的M代表 。已知
。已知 ,下列有关分析不正确的是
,下列有关分析不正确的是
A.①代表滴定 溶液的变化关系 溶液的变化关系 |
B.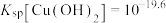 |
C.a点时,③中 与②中M的关系为 与②中M的关系为 |
D. 、 、 固体均易溶解于HX溶液 固体均易溶解于HX溶液 |
您最近一年使用:0次
名校
解题方法
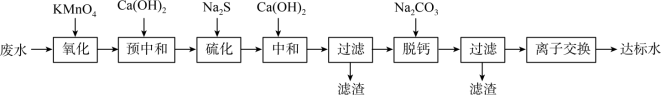
6 . 湿法炼锌的工业废水中主要阳离子有Zn2+、H+、Tl+、Tl3+,废水除铊的工艺流程如图。 能够在pH为0~14的范围内以离子态稳定存在,不易与
能够在pH为0~14的范围内以离子态稳定存在,不易与 形成沉淀。
形成沉淀。
②部分物质的 如表:
如表:
③排放标准:Tl的含量低于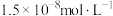 。
。
回答下列问题:
(1)Tl的原子序数为81,在元素周期表中的位置为___________ ,价电子排布式为___________ 。
(2)已知“氧化”步骤中 被还原为
被还原为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:___________ ,反应后仍存在少量的 。
。
(3)“预中和”步骤中加入 至溶液的pH约为7,可减少“硫化”步骤中
至溶液的pH约为7,可减少“硫化”步骤中 的使用量,还能减少
的使用量,还能减少___________ (填化学式)污染物的生成。
(4)“硫化”步骤的主要目的是除去___________ (填离子符号)。
(5)在“中和”步骤中,若要使溶液中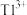 的含量低于排放标准,请根据
的含量低于排放标准,请根据 计算溶液的pH应大于
计算溶液的pH应大于___________ 。
(6)“离子交换”步骤中可用普鲁士蓝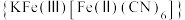 (其摩尔质量为
(其摩尔质量为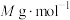 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[ 未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为
未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为___________ cm(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 能够在pH为0~14的范围内以离子态稳定存在,不易与
能够在pH为0~14的范围内以离子态稳定存在,不易与 形成沉淀。
形成沉淀。②部分物质的
 如表:
如表:| 物质 |  | 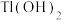 | ZnS |  |
 | 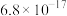 |  |  |  |
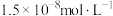 。
。回答下列问题:
(1)Tl的原子序数为81,在元素周期表中的位置为
(2)已知“氧化”步骤中
 被还原为
被还原为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式: 。
。(3)“预中和”步骤中加入
 至溶液的pH约为7,可减少“硫化”步骤中
至溶液的pH约为7,可减少“硫化”步骤中 的使用量,还能减少
的使用量,还能减少(4)“硫化”步骤的主要目的是除去
(5)在“中和”步骤中,若要使溶液中
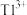 的含量低于排放标准,请根据
的含量低于排放标准,请根据 计算溶液的pH应大于
计算溶液的pH应大于(6)“离子交换”步骤中可用普鲁士蓝
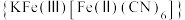 (其摩尔质量为
(其摩尔质量为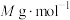 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[ 未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为
未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。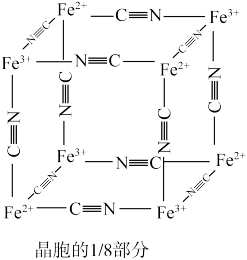
您最近一年使用:0次
解题方法
7 . 结合已有知识,根据下列实验操作,其对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将乙醇和浓硫酸混合溶液加热到170℃,并将产生的气体经过氢氧化钠溶液洗气,再通入溴水 | 溴水褪色 | 有乙烯生成 |
| B | 常温下将铁片分别插入稀硝酸和浓硝酸中 | 前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| C | 已知 : : 、 、 : :  ,向饱和溶液中滴加碳酸钠溶液 ,向饱和溶液中滴加碳酸钠溶液 | 无明显现象 |  与碳酸钠不反应 与碳酸钠不反应 |
| D | 向少量 悬浊液中加入足量饱和 悬浊液中加入足量饱和 溶液 溶液 | 沉淀颜色会由黑色变为浅红色( 为浅红色) 为浅红色) | Ksp(FeS)>Ksp(MnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 常温下,在烧杯中将0.025mol 粉末加水配成1L悬浊液,然后向烧杯中加入
粉末加水配成1L悬浊液,然后向烧杯中加入 固体并充分搅拌(忽略溶液体积的变化)。加入
固体并充分搅拌(忽略溶液体积的变化)。加入 固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法正确的是
固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法正确的是
 粉末加水配成1L悬浊液,然后向烧杯中加入
粉末加水配成1L悬浊液,然后向烧杯中加入 固体并充分搅拌(忽略溶液体积的变化)。加入
固体并充分搅拌(忽略溶液体积的变化)。加入 固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法正确的是
固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法正确的是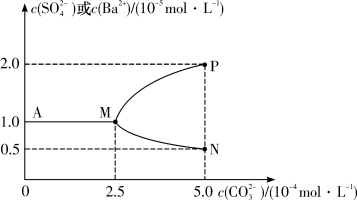
A.常温下, 在水中的溶解度、 在水中的溶解度、 均比在 均比在 溶液中的大 溶液中的大 |
B.常温下,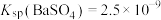 |
C.若要使 全部转化为 全部转化为 ,至少要加入0.625mol ,至少要加入0.625mol |
D. 恰好全部转化为 恰好全部转化为 时,离子浓度大小关系为 时,离子浓度大小关系为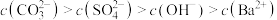 |
您最近一年使用:0次
解题方法
9 . 下列实验方案能达到实验目的的是

A.方案甲可制取无水 | B.方案乙可除去 溶液中部分的 溶液中部分的 |
C.方案丙可验证非金属性: | D.方案丁可判断溶度积: |
您最近一年使用:0次
名校
解题方法
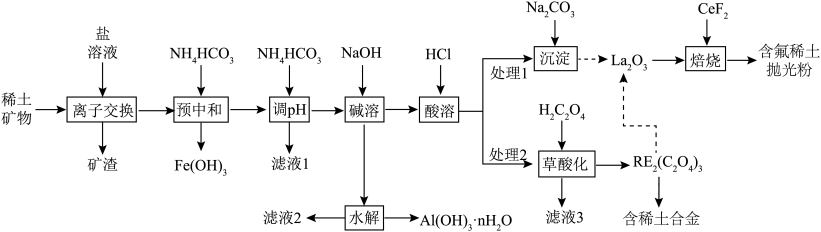
10 . 稀土(RE)包括镧(La)、铈(Ce)等元素,是重要的战略资源,从离子型稀土矿(含Fe、Al等元素)中提取稀土元素并获得高附加值产品的一种工艺流程如图所示。
回答下列问题:
(1)“预中和”工序中:
①该工序适宜的pH范围是________ 。
②胶状 的X射线衍射图谱中,
的X射线衍射图谱中,________ (填“能”或“不能”)观察到明锐的衍射峰。
(2)“调pH”工序中, 发生反应的离子方程式为
发生反应的离子方程式为________ 。
(3)滤液3可返回“________ ”工序循环使用。
(4)“沉淀”工序产物为________ [填“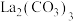 ”或“
”或“ ”],理由是
”],理由是________ {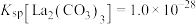 }。(当反应的
}。(当反应的 时可认为反应完全)
时可认为反应完全)
(5)含氟稀土抛光粉的主要成分为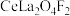 ,“焙烧”时发生反应的化学方程式为
,“焙烧”时发生反应的化学方程式为________ 。
(6)利用离子交换法浸出稀土的过程如图所示。已知离子半径越小、电荷数越大,离子交换能力越强。下列离子对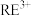 交换能力最强的是________。
交换能力最强的是________。
离子 |
|
|
|
开始沉淀时的pH | 1.5 | 4.3 | 5.6( |
沉淀完全时的pH | 3.2 | 5.5 | /( |
(1)“预中和”工序中:
①该工序适宜的pH范围是
②胶状
 的X射线衍射图谱中,
的X射线衍射图谱中,(2)“调pH”工序中,
 发生反应的离子方程式为
发生反应的离子方程式为(3)滤液3可返回“
(4)“沉淀”工序产物为
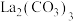 ”或“
”或“ ”],理由是
”],理由是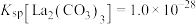 }。(当反应的
}。(当反应的 时可认为反应完全)
时可认为反应完全)(5)含氟稀土抛光粉的主要成分为
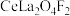 ,“焙烧”时发生反应的化学方程式为
,“焙烧”时发生反应的化学方程式为(6)利用离子交换法浸出稀土的过程如图所示。已知离子半径越小、电荷数越大,离子交换能力越强。下列离子对
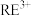 交换能力最强的是________。
交换能力最强的是________。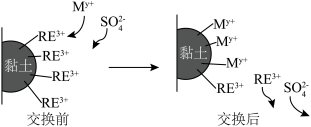
A. | B. | C. | D. |
您最近一年使用:0次
2024-04-16更新
|
242次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2023-2024学年高二下学期第一次大练习化学试题


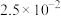
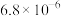
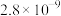
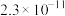


 为6.2)
为6.2)

