解题方法
1 . 由下列实验现象一定能得出相应结论的是
| 选项 | A | B | C | D |
| 装置或操作 | 在 饱和溶液中滴加稀硫酸,将产生的气体通入酸性 饱和溶液中滴加稀硫酸,将产生的气体通入酸性 溶液中 溶液中 | 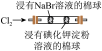 | 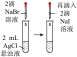 | 将带火星的木条伸入 与 与 的体积比为4∶1的混合气体中 的体积比为4∶1的混合气体中 |
| 现象 | 酸性 溶液褪色 溶液褪色 | 左边棉球变黄,右边棉球变蓝 | 试管中先出现淡黄色固体,后出现黄色固体 | 带火星的木条复燃 |
| 结论 | 该气体产物具有漂白性 | 氧化性: | 溶解度:AgCl>AgBr>AgI | 对于木条的燃烧, 比 比 的助燃效果更好 的助燃效果更好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 已知 为阿伏加德罗常数,下列关于
为阿伏加德罗常数,下列关于 说法正确的是
说法正确的是
 为阿伏加德罗常数,下列关于
为阿伏加德罗常数,下列关于 说法正确的是
说法正确的是A.标准状况下22.4L HF含有分子的个数为 |
B.1mol液态冰醋酸中含s-p  键的数目为4 键的数目为4 |
C.往 溶液中通入氯气,若有1mol 溶液中通入氯气,若有1mol  生成时,转移电子的数目可能为4 生成时,转移电子的数目可能为4 |
D.常温下已知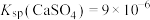 ,则该温度下 ,则该温度下 饱和溶液中含有 饱和溶液中含有 个 个 |
您最近一年使用:0次
3 . 湿法炼锌具有能耗低,生成产品纯度高等特点,其主要原料为锌精矿(主要成分为硫化锌,还含有铁、钴、铜、镉、铅等元素的杂质),获得较纯锌锭的工艺流程如图: 、
、 、CdO。
、CdO。
(1)铜原子的价层电子排布图为___________ 。
(2)“酸浸”中滤渣主要成分为___________ 。
(3)“一段沉积”和“二段沉积”刚开始加入锌粉时,反应速率较小,然后反应速率显著增大,请解释产生此现象的原因:___________ 。
(4)写出“赤铁矿除铁”过程中反应的离子方程式:___________ 。
(5)“ —萘酚净化除钴”先是
—萘酚净化除钴”先是 把
把 氧化成
氧化成 ,并生成NO,
,并生成NO, 与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出
与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出 被氧化的离子方程式:
被氧化的离子方程式:___________ 。
(6)“电解”工艺中,电解液常有较高浓度的 会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和
会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和 ,生成CuCl沉淀从而除去
,生成CuCl沉淀从而除去 。已知:
。已知: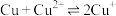
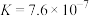 ;
;
 。请通过具体数据说明上述的反应能完全进行的原因:
。请通过具体数据说明上述的反应能完全进行的原因:___________ 。
(7)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中,发生合金化反应生成LiZn(合金相),同时负极材料晶胞的组成变化如图所示。 的电极方程式为
的电极方程式为___________ (x和y用具体数字表示)。
②若 的晶胞参数为a nm,则EF间的距离为
的晶胞参数为a nm,则EF间的距离为___________ nm。

 、
、 、CdO。
、CdO。(1)铜原子的价层电子排布图为
(2)“酸浸”中滤渣主要成分为
(3)“一段沉积”和“二段沉积”刚开始加入锌粉时,反应速率较小,然后反应速率显著增大,请解释产生此现象的原因:
(4)写出“赤铁矿除铁”过程中反应的离子方程式:
(5)“
 —萘酚净化除钴”先是
—萘酚净化除钴”先是 把
把 氧化成
氧化成 ,并生成NO,
,并生成NO, 与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出
与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出 被氧化的离子方程式:
被氧化的离子方程式:(6)“电解”工艺中,电解液常有较高浓度的
 会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和
会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和 ,生成CuCl沉淀从而除去
,生成CuCl沉淀从而除去 。已知:
。已知: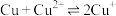
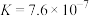 ;
;
 。请通过具体数据说明上述的反应能完全进行的原因:
。请通过具体数据说明上述的反应能完全进行的原因:(7)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中,发生合金化反应生成LiZn(合金相),同时负极材料晶胞的组成变化如图所示。
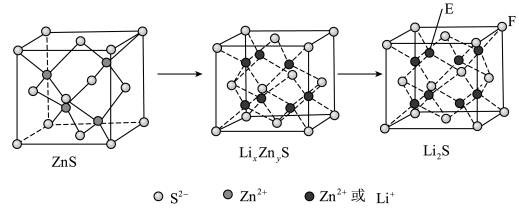
 的电极方程式为
的电极方程式为②若
 的晶胞参数为a nm,则EF间的距离为
的晶胞参数为a nm,则EF间的距离为
您最近一年使用:0次
名校
解题方法
4 . 常温下,在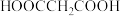 (简记为
(简记为 )和
)和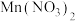 的混合溶液中滴加
的混合溶液中滴加 溶液,混合溶液中
溶液,混合溶液中 [
[ ,
, 、
、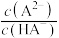 、
、 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
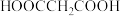 (简记为
(简记为 )和
)和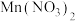 的混合溶液中滴加
的混合溶液中滴加 溶液,混合溶液中
溶液,混合溶液中 [
[ ,
, 、
、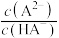 、
、 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
A. 代表 代表 与 与 的关系 的关系 |
B.直线 和 和 的交叉点坐标为 的交叉点坐标为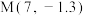 |
C.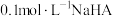 溶液中: 溶液中: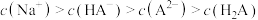 |
D.常温下,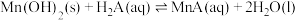 的 的 值为 值为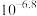 |
您最近一年使用:0次
2024-04-05更新
|
196次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高三下学期3月月考化学试题
5 . 向 溶液中滴加NaCl溶液,发生反应
溶液中滴加NaCl溶液,发生反应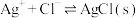 和
和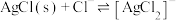 。
。 与
与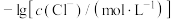 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 或
或 )。下列说法错误的是
)。下列说法错误的是

 溶液中滴加NaCl溶液,发生反应
溶液中滴加NaCl溶液,发生反应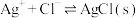 和
和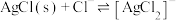 。
。 与
与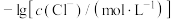 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 或
或 )。下列说法错误的是
)。下列说法错误的是
A. 时,溶液中 时,溶液中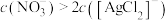 |
B.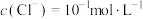 时,溶液中 时,溶液中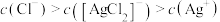 |
C.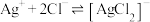 的平衡常数 的平衡常数 的值为 的值为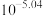 |
D.用 沉淀 沉淀 ,溶液中 ,溶液中 浓度过大时,沉淀效果不好 浓度过大时,沉淀效果不好 |
您最近一年使用:0次
6 . 以 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:
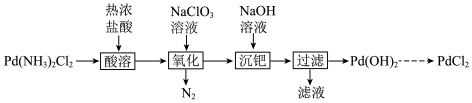
已知:① 具有顺反异构;
具有顺反异构;
②“酸溶”中生成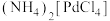 ;
;
③ 有两性,
有两性, ;
;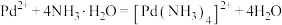
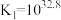 。
。
下列说法不正确的是
 固体为原料制备纯
固体为原料制备纯 ,其部分实验过程如下:
,其部分实验过程如下:
已知:①
 具有顺反异构;
具有顺反异构;②“酸溶”中生成
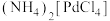 ;
;③
 有两性,
有两性, ;
;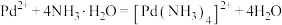
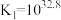 。
。下列说法不正确的是
A. 中的配位体为 中的配位体为 ,Pd的配位数为2 ,Pd的配位数为2 |
B.“氧化”过程中发生反应的离子方程式为: |
C. 的平衡常数 的平衡常数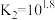 |
D.若氧化不充分,将会导致 的产率降低 的产率降低 |
您最近一年使用:0次
解题方法
7 . 氧化锌在橡胶、油漆涂料、化工、医疗及食品等行业有着广泛应用。一种以含锌烟灰(含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等)为原料制备氧化锌的工艺流程如图所示:
等)为原料制备氧化锌的工艺流程如图所示: 、
、 、
、 ;
;
ⅱ.25℃时相关物质的 如下表:
如下表:
(1) 态核外电子能级共
态核外电子能级共_____ 个。
(2)“氧化预处理”阶段得到的氧化产物有 、
、 ,“氧化预处理”的目的是
,“氧化预处理”的目的是_____ 。
(3)“氨浸”时生成多种配离子,其中生成 的离子方程式为
的离子方程式为_____ 。
(4)已知: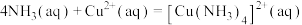
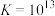 ,则
,则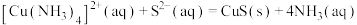 的化学平衡常数
的化学平衡常数 为
为_____ 。
(5)“蒸氨”时得到混合气体e和固体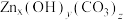 。
。
①混合气体e可返回至_____ 工序循环利用;
②取11.2g固体,经充分“煅烧”后得到氧化锌8.1g,同时产生的气体通入到足量 溶液中,可得沉淀9.85g,则固体
溶液中,可得沉淀9.85g,则固体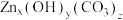 的化学式为
的化学式为_____ 。
(6)通过氢电极增压法可利用产品氧化锌进一步制得单质锌(如图),储罐内 溶解后形成
溶解后形成 离子,电解池中发生总反应的离子方程式为
离子,电解池中发生总反应的离子方程式为_____ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等)为原料制备氧化锌的工艺流程如图所示:
等)为原料制备氧化锌的工艺流程如图所示: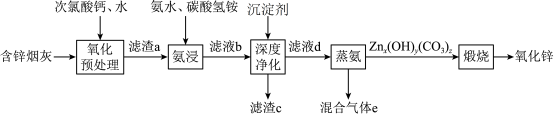
 、
、 、
、 ;
;ⅱ.25℃时相关物质的
 如下表:
如下表:| 物质 |  |  |  |  |  |  |
 | 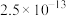 |  |  | 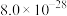 | 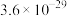 | 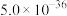 |
(1)
 态核外电子能级共
态核外电子能级共(2)“氧化预处理”阶段得到的氧化产物有
 、
、 ,“氧化预处理”的目的是
,“氧化预处理”的目的是(3)“氨浸”时生成多种配离子,其中生成
 的离子方程式为
的离子方程式为(4)已知:
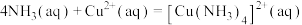
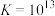 ,则
,则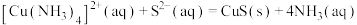 的化学平衡常数
的化学平衡常数 为
为(5)“蒸氨”时得到混合气体e和固体
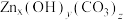 。
。①混合气体e可返回至
②取11.2g固体,经充分“煅烧”后得到氧化锌8.1g,同时产生的气体通入到足量
 溶液中,可得沉淀9.85g,则固体
溶液中,可得沉淀9.85g,则固体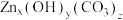 的化学式为
的化学式为(6)通过氢电极增压法可利用产品氧化锌进一步制得单质锌(如图),储罐内
 溶解后形成
溶解后形成 离子,电解池中发生总反应的离子方程式为
离子,电解池中发生总反应的离子方程式为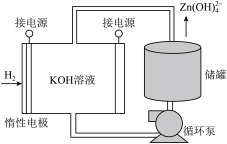
您最近一年使用:0次
名校
8 . 为了探究 的溶度积常数
的溶度积常数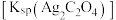 的测定,某兴趣小组设计如下步骤。
的测定,某兴趣小组设计如下步骤。

(1)步骤Ⅰ中需要配制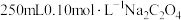 溶液、
溶液、 溶液、
溶液、 标准溶液。
标准溶液。
①配制 溶液时,选用棕色的容量瓶而不选用普通容量瓶的原因为
溶液时,选用棕色的容量瓶而不选用普通容量瓶的原因为_______ 。
②用 固体配制该溶液时,需要用电子天平称量
固体配制该溶液时,需要用电子天平称量_______ 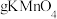 固体(该电子天平称量时可读数到
固体(该电子天平称量时可读数到 )。
)。
(2)用碱性滴定管量取 溶液于洁净的棕色锥形瓶中,然后用棕色滴定管量取一定体积的
溶液于洁净的棕色锥形瓶中,然后用棕色滴定管量取一定体积的 溶液注入到棕色锥形瓶中,摇动锥形瓶使沉淀完全,把沉淀陈化
溶液注入到棕色锥形瓶中,摇动锥形瓶使沉淀完全,把沉淀陈化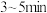 ,用过滤器过滤,滤液用干燥洁净的烧杯盛接。
,用过滤器过滤,滤液用干燥洁净的烧杯盛接。
①量取 溶液时选用碱式滴定管的主要原因为
溶液时选用碱式滴定管的主要原因为_______ (用离子方程式表示)。
②为方便数据处理,“一定体积”最好是_______  。
。
(3)准确量取 所得滤液注入锥形瓶中,加入足量的
所得滤液注入锥形瓶中,加入足量的 的硫酸,用所配
的硫酸,用所配 标准溶液滴定,实验三次,消耗
标准溶液滴定,实验三次,消耗 标准溶液的平均值为
标准溶液的平均值为 (已知:
(已知: )。
)。
①滴定终点现象为_______ 。
②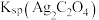 的溶度积测定值为
的溶度积测定值为_______ (用含b的计算式表示)。
③若步骤Ⅱ中烧杯盛接的滤液浑浊,会使测量值___ (填“偏高”“偏低”或“无影响”,下同);若锥形瓶有少量水存在,会使测量值__ 。
 的溶度积常数
的溶度积常数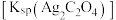 的测定,某兴趣小组设计如下步骤。
的测定,某兴趣小组设计如下步骤。
(1)步骤Ⅰ中需要配制
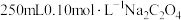 溶液、
溶液、 溶液、
溶液、 标准溶液。
标准溶液。①配制
 溶液时,选用棕色的容量瓶而不选用普通容量瓶的原因为
溶液时,选用棕色的容量瓶而不选用普通容量瓶的原因为②用
 固体配制该溶液时,需要用电子天平称量
固体配制该溶液时,需要用电子天平称量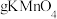 固体(该电子天平称量时可读数到
固体(该电子天平称量时可读数到 )。
)。(2)用碱性滴定管量取
 溶液于洁净的棕色锥形瓶中,然后用棕色滴定管量取一定体积的
溶液于洁净的棕色锥形瓶中,然后用棕色滴定管量取一定体积的 溶液注入到棕色锥形瓶中,摇动锥形瓶使沉淀完全,把沉淀陈化
溶液注入到棕色锥形瓶中,摇动锥形瓶使沉淀完全,把沉淀陈化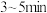 ,用过滤器过滤,滤液用干燥洁净的烧杯盛接。
,用过滤器过滤,滤液用干燥洁净的烧杯盛接。①量取
 溶液时选用碱式滴定管的主要原因为
溶液时选用碱式滴定管的主要原因为②为方便数据处理,“一定体积”最好是
 。
。(3)准确量取
 所得滤液注入锥形瓶中,加入足量的
所得滤液注入锥形瓶中,加入足量的 的硫酸,用所配
的硫酸,用所配 标准溶液滴定,实验三次,消耗
标准溶液滴定,实验三次,消耗 标准溶液的平均值为
标准溶液的平均值为 (已知:
(已知: )。
)。①滴定终点现象为
②
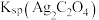 的溶度积测定值为
的溶度积测定值为③若步骤Ⅱ中烧杯盛接的滤液浑浊,会使测量值
您最近一年使用:0次
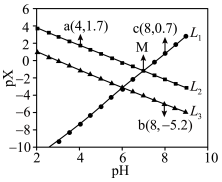
9 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

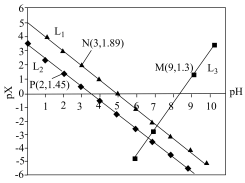
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的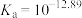 |
C.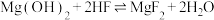 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近一年使用:0次
2024-04-01更新
|
452次组卷
|
5卷引用:湖南省邵阳市第二中学2023-2024学年高二下学期4月期中考试化学试题
解题方法
10 . 下列实验设计能达到对应实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 检验溶液中是否含 | 在待测液中滴加 溶液,观察是否出现特征蓝色沉淀 溶液,观察是否出现特征蓝色沉淀 |
| B | 检验含碘食盐中存在碘元素 | 在含碘食盐溶液中加入淀粉溶液,再滴加稀硝酸,观察溶液是否变蓝 |
| C | 验证溶度积: | 在2mL 0.1  溶液中先滴加5滴0.1 溶液中先滴加5滴0.1  溶液,再滴加5滴0.1 溶液,再滴加5滴0.1  溶液,观察是否出现沉淀 溶液,观察是否出现沉淀 |
| D | 探究 和 和 氧化性强弱 氧化性强弱 | 在 溶液中滴加酸化的过氧化氢溶液,观察溶液是否变为黄色 溶液中滴加酸化的过氧化氢溶液,观察溶液是否变为黄色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



