名校
1 .  (三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(1)探究三草酸合铁酸钾的热分解产物。
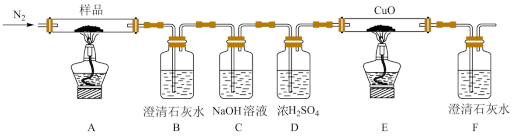
按如上图所示装置进行实验:观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色。
①装置C的作用是_______ 。
②装置E中发生反应的化学方程式为_______ 。
(2)测定三草酸合铁酸钾中铁的含量。
测定原理:

①配制溶液:实验中配制100 mL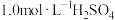 溶液,需要的仪器有烧杯、玻璃棒、量筒、
溶液,需要的仪器有烧杯、玻璃棒、量筒、_______ (从下图中选择,写出名称)。
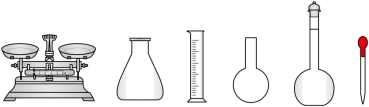
②测定:称量10.00g晶体样品,加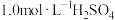 溶解后配成100mL溶液。
溶解后配成100mL溶液。
步骤Ⅰ:取20.00mL配制好的溶液于锥形瓶中,滴加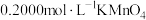 ,溶液至恰好完全反应。
,溶液至恰好完全反应。
步骤Ⅱ:向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀 酸化,用
酸化,用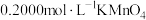 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液20.00mL。
溶液20.00mL。
该晶体样品中铁的质量分数为_______ (写出计算过程)。
 (三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:(1)探究三草酸合铁酸钾的热分解产物。

按如上图所示装置进行实验:观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色。
①装置C的作用是
②装置E中发生反应的化学方程式为
(2)测定三草酸合铁酸钾中铁的含量。
测定原理:


①配制溶液:实验中配制100 mL
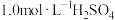 溶液,需要的仪器有烧杯、玻璃棒、量筒、
溶液,需要的仪器有烧杯、玻璃棒、量筒、
②测定:称量10.00g晶体样品,加
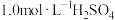 溶解后配成100mL溶液。
溶解后配成100mL溶液。步骤Ⅰ:取20.00mL配制好的溶液于锥形瓶中,滴加
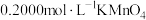 ,溶液至恰好完全反应。
,溶液至恰好完全反应。步骤Ⅱ:向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀
 酸化,用
酸化,用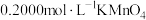 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液20.00mL。
溶液20.00mL。该晶体样品中铁的质量分数为
您最近一年使用:0次
名校
解题方法
2 .  是一种重要的P型半导体材料。以一种石膏渣[含
是一种重要的P型半导体材料。以一种石膏渣[含 及少量
及少量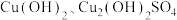 、
、 等]为原料制备
等]为原料制备 的实验流程如下:
的实验流程如下:
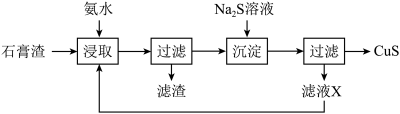
已知:常温下,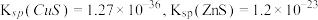 。
。
(1)“浸取”时,生成 与
与 等。
等。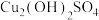 参加反应的离子方程式为
参加反应的离子方程式为_______ 。
(2)“沉淀”时 溶液的用量不宜过多,其原因是
溶液的用量不宜过多,其原因是_______ 。
(3)循环“浸取”多次后,“滤液X”中浓度增大的阳离子主要有_______ 。
(4)为测定“浸取”时 元素浸出率,需先测定石膏渣中
元素浸出率,需先测定石膏渣中 元素含量。称取
元素含量。称取 石膏渣,加入足量稀
石膏渣,加入足量稀 充分溶解,过滤并洗涤滤渣,将滤液转移至
充分溶解,过滤并洗涤滤渣,将滤液转移至 容量瓶中,加水稀释至刻度;准确量取
容量瓶中,加水稀释至刻度;准确量取 稀释后的溶液于锥形瓶中,加入足量KI溶液(
稀释后的溶液于锥形瓶中,加入足量KI溶液( ),用
),用 标准溶液滴定至终点(
标准溶液滴定至终点(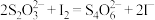 ),平行滴定3次,平均消耗
),平行滴定3次,平均消耗 标准溶液
标准溶液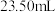 。计算石膏渣中
。计算石膏渣中 元素质量分数(写出计算过程)
元素质量分数(写出计算过程)_______ 。
 是一种重要的P型半导体材料。以一种石膏渣[含
是一种重要的P型半导体材料。以一种石膏渣[含 及少量
及少量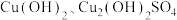 、
、 等]为原料制备
等]为原料制备 的实验流程如下:
的实验流程如下:
已知:常温下,
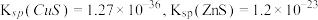 。
。(1)“浸取”时,生成
 与
与 等。
等。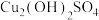 参加反应的离子方程式为
参加反应的离子方程式为(2)“沉淀”时
 溶液的用量不宜过多,其原因是
溶液的用量不宜过多,其原因是(3)循环“浸取”多次后,“滤液X”中浓度增大的阳离子主要有
(4)为测定“浸取”时
 元素浸出率,需先测定石膏渣中
元素浸出率,需先测定石膏渣中 元素含量。称取
元素含量。称取 石膏渣,加入足量稀
石膏渣,加入足量稀 充分溶解,过滤并洗涤滤渣,将滤液转移至
充分溶解,过滤并洗涤滤渣,将滤液转移至 容量瓶中,加水稀释至刻度;准确量取
容量瓶中,加水稀释至刻度;准确量取 稀释后的溶液于锥形瓶中,加入足量KI溶液(
稀释后的溶液于锥形瓶中,加入足量KI溶液( ),用
),用 标准溶液滴定至终点(
标准溶液滴定至终点(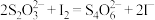 ),平行滴定3次,平均消耗
),平行滴定3次,平均消耗 标准溶液
标准溶液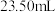 。计算石膏渣中
。计算石膏渣中 元素质量分数(写出计算过程)
元素质量分数(写出计算过程)
您最近一年使用:0次
名校
解题方法
3 . 轻质碳酸钙可用作橡胶的填料。以磷石膏(含 和少量
和少量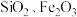 等)为原料制备轻质碳酸钙和铝铵矾的实验流程如图:
等)为原料制备轻质碳酸钙和铝铵矾的实验流程如图:
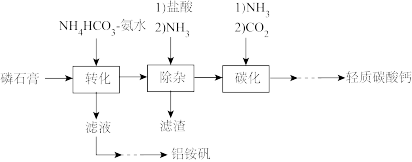
(1)检查图中所示装置气密性的操作为:用止水夹关闭左侧导管,_________ 。
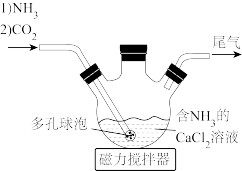
(2)“转化”步骤中 转化为
转化为 的化学方程式
的化学方程式_________ 。
(3)“除杂”时通入NH3的目的是_________ 。
(4)通过下列方法测定产品中碳酸钙的含量:准确称取0.5000g产品用盐酸充分溶解,过滤,将滤液和洗涤液转移至250mL容量瓶中定容、摇匀,记为试液A。取25.00mL试液 ,加入指示剂,调节pH>12,用0.02000mol/LNa2H2Y标准溶液滴定
,加入指示剂,调节pH>12,用0.02000mol/LNa2H2Y标准溶液滴定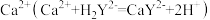 ,至终点时消耗Na2H2Y溶液24.60mL。计算产品中碳酸钙的质量分数
,至终点时消耗Na2H2Y溶液24.60mL。计算产品中碳酸钙的质量分数_________ 。(写出计算过程)。
(5)铝铵矾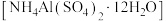 是一种水絮凝剂。请补充由“转化”后的滤液制取铝铵矾的实验方案:
是一种水絮凝剂。请补充由“转化”后的滤液制取铝铵矾的实验方案:
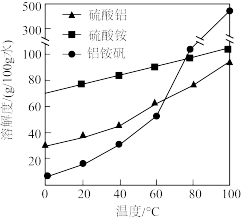
①_________ ,将所得溶液蒸发浓缩至有大量晶体析出,过滤,用无水乙醇洗涤、干燥,得 固体;②
固体;②_________ ,用无水乙醇洗涤,干燥,得到铝铵矾。(部分物质的溶解度随温度的变化如图所示,实验须用的试剂: 的
的 溶液、
溶液、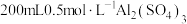 溶液)
溶液)
 和少量
和少量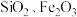 等)为原料制备轻质碳酸钙和铝铵矾的实验流程如图:
等)为原料制备轻质碳酸钙和铝铵矾的实验流程如图:
(1)检查图中所示装置气密性的操作为:用止水夹关闭左侧导管,

(2)“转化”步骤中
 转化为
转化为 的化学方程式
的化学方程式(3)“除杂”时通入NH3的目的是
(4)通过下列方法测定产品中碳酸钙的含量:准确称取0.5000g产品用盐酸充分溶解,过滤,将滤液和洗涤液转移至250mL容量瓶中定容、摇匀,记为试液A。取25.00mL试液
 ,加入指示剂,调节pH>12,用0.02000mol/LNa2H2Y标准溶液滴定
,加入指示剂,调节pH>12,用0.02000mol/LNa2H2Y标准溶液滴定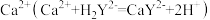 ,至终点时消耗Na2H2Y溶液24.60mL。计算产品中碳酸钙的质量分数
,至终点时消耗Na2H2Y溶液24.60mL。计算产品中碳酸钙的质量分数(5)铝铵矾
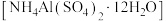 是一种水絮凝剂。请补充由“转化”后的滤液制取铝铵矾的实验方案:
是一种水絮凝剂。请补充由“转化”后的滤液制取铝铵矾的实验方案:①
 固体;②
固体;② 的
的 溶液、
溶液、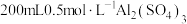 溶液)
溶液)
您最近一年使用:0次
解题方法
4 . 碱式次氯酸镁[化学式为Mg2ClO(OH)3·H2O]是一种白色粉末,难溶于水,也是新一代无机抗菌剂。可由Cl2、NaOH及MgCl2为原料制取。
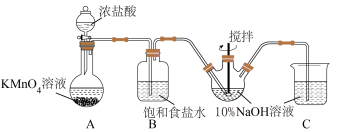
(1)甲同学拟利用如图装置制备质量分数约为5%的次氯酸钠溶液。___________ 。
②Cl2和NaOH在较高的温度下反应生成NaClO3,写出该反应的离子反应方程式___________ ,因此控制反应在0~5℃范围内进行,实验中适宜的措施是___________ 。
(2)乙同学拟利用甲同学制得的NaClO溶液制取碱式次氯酸镁,步骤如下:
步骤2:逐滴滴入NaClO溶液;
步骤3:调节溶液pH=10,回流反应4h;
步骤4:过滤,烘干。
①上图中,冷凝水从仪器A___________ (填"上口"或“下口"”) 进入。
②过滤时,需用到的玻璃仪器除烧杯外,还需___________ 。
③写出MgCl2、NaOH、Cl2反应制取Mg2ClO(OH)3·H2O的化学方程式:___________ 。
④通过测定Mg2ClO(OH)3·H2O产品有效氯的含量来衡量产品品质。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,有效氯含量=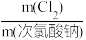 ×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2
×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2 =2I-+
=2I-+ )恰好完全反应,测得有效氯含量为
)恰好完全反应,测得有效氯含量为___________ 。(写出计算过程)
(1)甲同学拟利用如图装置制备质量分数约为5%的次氯酸钠溶液。
②Cl2和NaOH在较高的温度下反应生成NaClO3,写出该反应的离子反应方程式
(2)乙同学拟利用甲同学制得的NaClO溶液制取碱式次氯酸镁,步骤如下:
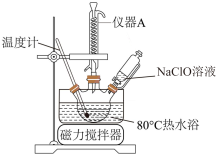
步骤2:逐滴滴入NaClO溶液;
步骤3:调节溶液pH=10,回流反应4h;
步骤4:过滤,烘干。
①上图中,冷凝水从仪器A
②过滤时,需用到的玻璃仪器除烧杯外,还需
③写出MgCl2、NaOH、Cl2反应制取Mg2ClO(OH)3·H2O的化学方程式:
④通过测定Mg2ClO(OH)3·H2O产品有效氯的含量来衡量产品品质。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,有效氯含量=
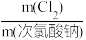 ×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2
×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2 =2I-+
=2I-+ )恰好完全反应,测得有效氯含量为
)恰好完全反应,测得有效氯含量为
您最近一年使用:0次
名校
5 . 某种胃药的有效成分为碳酸钙.某实验小组为测定其中碳酸钙的含量.取10粒药片(0.1g/粒)研碎后溶解.加入25.00mL NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
(1)配制500mL 的NaOH溶液,需要NaOH的质量是
的NaOH溶液,需要NaOH的质量是____________ 。
(2)药片中碳酸钙的质量分数_________ 。(写出计算过程)
 NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
 的NaOH溶液,需要NaOH的质量是
的NaOH溶液,需要NaOH的质量是(2)药片中碳酸钙的质量分数
您最近一年使用:0次
解题方法
6 . 回收再利用金属冶炼厂的酸性废水(主要含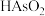 、
、 、
、 、
、 、
、 ),制备亚砷酸铜
),制备亚砷酸铜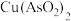 的流程如下。
的流程如下。
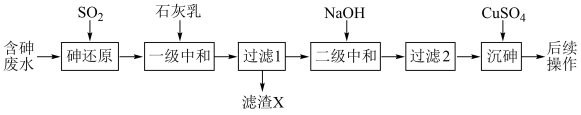
(1)基态砷原子的电子排布式为_______ 。
(2)砷的还原。常温下,五价砷溶液中各种微粒的物质的量分数随pH的变化曲线如图所示。向酸性废水中通入 ,能把五价砷转化为三价砷。
,能把五价砷转化为三价砷。
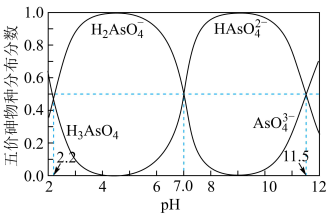
① 的二级电离平衡常数
的二级电离平衡常数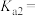
_______ 。
②pH为1时“还原”的主要反应的离子方程式为_______ 。
(3)中和除杂。当溶液中离子浓度小于 ,可认为已经完全除去。
,可认为已经完全除去。
已知: 在
在 时开始转化为
时开始转化为 ,
,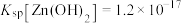 ,
, ,
, 。
。
①一级中和控制pH为2左右,滤渣X的主要成分有_______ 。
②二级中和沉淀重金属离子应控制pH范围为_______ 。
(4)应用碘量法可测定亚砷酸铜中的铜含量。称取2.000g试样溶于稀 搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成
搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成 溶液,取
溶液,取 所配溶液于碘量瓶中加入过量的碘化钾溶液,用
所配溶液于碘量瓶中加入过量的碘化钾溶液,用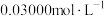
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。
①计算样品中铜元素的质量分数_______ 。(写出计算过程)
②已知纯亚砷酸铜中铜元素的质量分数为23.02%,实际测得样品中铜元素的质量分数有偏差(操作步骤均正确)的原因为_______ 。(已知: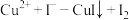 ;
;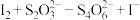 ,未配平)
,未配平)
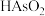 、
、 、
、 、
、 、
、 ),制备亚砷酸铜
),制备亚砷酸铜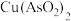 的流程如下。
的流程如下。
(1)基态砷原子的电子排布式为
(2)砷的还原。常温下,五价砷溶液中各种微粒的物质的量分数随pH的变化曲线如图所示。向酸性废水中通入
 ,能把五价砷转化为三价砷。
,能把五价砷转化为三价砷。
①
 的二级电离平衡常数
的二级电离平衡常数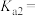
②pH为1时“还原”的主要反应的离子方程式为
(3)中和除杂。当溶液中离子浓度小于
 ,可认为已经完全除去。
,可认为已经完全除去。已知:
 在
在 时开始转化为
时开始转化为 ,
,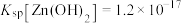 ,
, ,
, 。
。①一级中和控制pH为2左右,滤渣X的主要成分有
②二级中和沉淀重金属离子应控制pH范围为
(4)应用碘量法可测定亚砷酸铜中的铜含量。称取2.000g试样溶于稀
 搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成
搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成 溶液,取
溶液,取 所配溶液于碘量瓶中加入过量的碘化钾溶液,用
所配溶液于碘量瓶中加入过量的碘化钾溶液,用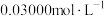
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 。
。①计算样品中铜元素的质量分数
②已知纯亚砷酸铜中铜元素的质量分数为23.02%,实际测得样品中铜元素的质量分数有偏差(操作步骤均正确)的原因为
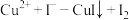 ;
;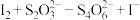 ,未配平)
,未配平)
您最近一年使用:0次
解题方法
7 .  常用于制备易吸收的高效铁制剂。
常用于制备易吸收的高效铁制剂。
(1)制备 。一种利用铁矿烧渣(主要成分是
。一种利用铁矿烧渣(主要成分是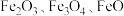 和
和 )制取
)制取 的流程如下:
的流程如下:
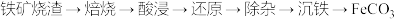
①“焙烧”过程是将铁矿烧渣和煤粉按一定比例投入焙烧炉中,利用生成的 将铁的高价氧化物转化为
将铁的高价氧化物转化为 。
。 参与反应的化学方程式为
参与反应的化学方程式为___________ 。
②“酸浸”是在一定温度下,用一定浓度的 溶液浸取焙烧后固体中的铁元素。酸浸时间对铁浸出率的影响如题图所示。
溶液浸取焙烧后固体中的铁元素。酸浸时间对铁浸出率的影响如题图所示。 后铁浸出率整体呈下降趋势的可能原因是
后铁浸出率整体呈下降趋势的可能原因是___________ 。 完全转化为
完全转化为 。检验
。检验 是否还原完全的实验操作是
是否还原完全的实验操作是___________
④“沉铁”是将“除杂”后的 溶液与
溶液与 溶液反应,生成
溶液反应,生成 沉淀。设计以
沉淀。设计以 溶液、
溶液、 溶液为原料,制备
溶液为原料,制备 的实验方案:
的实验方案:___________ 。
[ 沉淀需“洗涤完全”,
沉淀需“洗涤完全”, 开始沉淀的
开始沉淀的 ]。(可选用试剂:蒸馏水、
]。(可选用试剂:蒸馏水、 溶液、稀
溶液、稀 )
)
⑤将制得的 加入足量乳酸溶液
加入足量乳酸溶液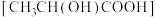 中,再加入少量铁粉,
中,再加入少量铁粉,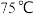 下搅拌反应,过滤。将所得滤液经加热浓缩、冷却结晶、过滤、洗涤、干燥,获得乳酸亚铁晶体
下搅拌反应,过滤。将所得滤液经加热浓缩、冷却结晶、过滤、洗涤、干燥,获得乳酸亚铁晶体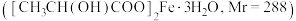 。用铈
。用铈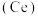 量法测定产品中
量法测定产品中 的含量。取
的含量。取 产品配成
产品配成 溶液,每次取
溶液,每次取 ,进行必要处理,用
,进行必要处理,用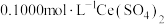 标准溶液滴定至终点,平均消耗
标准溶液滴定至终点,平均消耗 溶液的体积为
溶液的体积为 。滴定反应为
。滴定反应为 ,则产品中乳酸亚铁晶体的质量分数为
,则产品中乳酸亚铁晶体的质量分数为___________ 。(写出计算过程)
(2)若用酸性 代替
代替 测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于
测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于 ,其原因可能是
,其原因可能是___________ 。
 常用于制备易吸收的高效铁制剂。
常用于制备易吸收的高效铁制剂。(1)制备
 。一种利用铁矿烧渣(主要成分是
。一种利用铁矿烧渣(主要成分是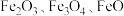 和
和 )制取
)制取 的流程如下:
的流程如下: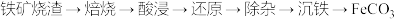
①“焙烧”过程是将铁矿烧渣和煤粉按一定比例投入焙烧炉中,利用生成的
 将铁的高价氧化物转化为
将铁的高价氧化物转化为 。
。 参与反应的化学方程式为
参与反应的化学方程式为②“酸浸”是在一定温度下,用一定浓度的
 溶液浸取焙烧后固体中的铁元素。酸浸时间对铁浸出率的影响如题图所示。
溶液浸取焙烧后固体中的铁元素。酸浸时间对铁浸出率的影响如题图所示。 后铁浸出率整体呈下降趋势的可能原因是
后铁浸出率整体呈下降趋势的可能原因是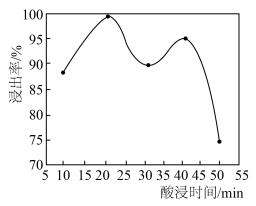
 完全转化为
完全转化为 。检验
。检验 是否还原完全的实验操作是
是否还原完全的实验操作是④“沉铁”是将“除杂”后的
 溶液与
溶液与 溶液反应,生成
溶液反应,生成 沉淀。设计以
沉淀。设计以 溶液、
溶液、 溶液为原料,制备
溶液为原料,制备 的实验方案:
的实验方案:[
 沉淀需“洗涤完全”,
沉淀需“洗涤完全”, 开始沉淀的
开始沉淀的 ]。(可选用试剂:蒸馏水、
]。(可选用试剂:蒸馏水、 溶液、稀
溶液、稀 )
)⑤将制得的
 加入足量乳酸溶液
加入足量乳酸溶液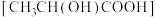 中,再加入少量铁粉,
中,再加入少量铁粉,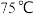 下搅拌反应,过滤。将所得滤液经加热浓缩、冷却结晶、过滤、洗涤、干燥,获得乳酸亚铁晶体
下搅拌反应,过滤。将所得滤液经加热浓缩、冷却结晶、过滤、洗涤、干燥,获得乳酸亚铁晶体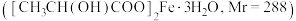 。用铈
。用铈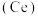 量法测定产品中
量法测定产品中 的含量。取
的含量。取 产品配成
产品配成 溶液,每次取
溶液,每次取 ,进行必要处理,用
,进行必要处理,用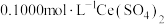 标准溶液滴定至终点,平均消耗
标准溶液滴定至终点,平均消耗 溶液的体积为
溶液的体积为 。滴定反应为
。滴定反应为 ,则产品中乳酸亚铁晶体的质量分数为
,则产品中乳酸亚铁晶体的质量分数为(2)若用酸性
 代替
代替 测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于
测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于 ,其原因可能是
,其原因可能是
您最近一年使用:0次
2023-06-28更新
|
172次组卷
|
3卷引用:江苏省连云港市2022-2023学年高二下学期6月期末考试化学试题
江苏省连云港市2022-2023学年高二下学期6月期末考试化学试题(已下线)专题07 化工流程综合题-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(江苏专用)江苏省部分学校2023-2024学年高二下学期期末考前演练化学试题(二)
名校
解题方法
8 . I.现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量。可供选用的反应物:CaCO3固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
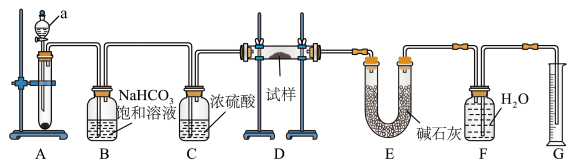
(1)装置a的名称为_____ 。
(2)装置B中除杂反应的离子方程式为_________ 。
(3)装置D中反应的化学方程式为_______ 。
(4)装置E中碱石灰的主要作用是________ 。
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数___________ 。
Ⅱ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
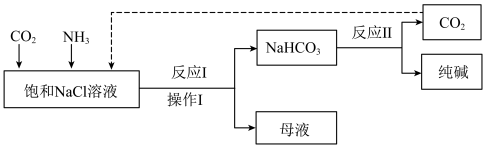
(6)为提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为_____ 。
A.先通CO2再通NH3 B.先通NH3再通CO2

(1)装置a的名称为
(2)装置B中除杂反应的离子方程式为
(3)装置D中反应的化学方程式为
(4)装置E中碱石灰的主要作用是
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数
Ⅱ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

(6)为提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为
A.先通CO2再通NH3 B.先通NH3再通CO2
您最近一年使用:0次
名校
9 . 三氯化六氨合钴(Ⅲ){[Co(NH3)6]Cl3}是制备其它三价钴配合物的重要试剂。
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3•6H2O在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
制备[Co(NH3)6]Cl3•6H2O的实验操作步骤如下:
第一步:混合。取研细的CoCl2•6H2O和NH4Cl溶解后转入三颈烧瓶,加入活性炭作催化剂。
第二步:配合、氧化。如图装置,先向三颈烧瓶滴加过量氨水,充分反应,再向混合溶液中滴加H2O2,水浴加热温度控制在50~60℃,充分搅拌,生成的[Co(NH3)6]Cl3吸附在活性炭上。
回答下列问题:
(1)加入的NH4Cl溶液有利于后续Co2+与NH3的配合反应,其原理是_______ 。
(2)加入H2O2溶液时发生反应的离子方程式为_________ 。
(3)向三颈烧瓶中先滴加氨水后滴加H2O2的原因是_________ 。
(4)已知:稀盐酸可将吸附在活性炭上的[Co(NH3)6]Cl3溶解。请补充完整第三步实验方案:将三颈烧瓶中所得混合物充分搅拌、趁热过滤,________ ,低温干燥。(实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。)
(5)为测定产品中钴的含量,进行下列实验:
称取3.5400g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液12.00mL。(反应原理:Co3++I-→Co2++I2、I2+S2O →I-+S4O
→I-+S4O 未配平),计算产品中钴元素的质量分数
未配平),计算产品中钴元素的质量分数________ (写出计算过程)。
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3•6H2O在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
制备[Co(NH3)6]Cl3•6H2O的实验操作步骤如下:
第一步:混合。取研细的CoCl2•6H2O和NH4Cl溶解后转入三颈烧瓶,加入活性炭作催化剂。
第二步:配合、氧化。如图装置,先向三颈烧瓶滴加过量氨水,充分反应,再向混合溶液中滴加H2O2,水浴加热温度控制在50~60℃,充分搅拌,生成的[Co(NH3)6]Cl3吸附在活性炭上。

回答下列问题:
(1)加入的NH4Cl溶液有利于后续Co2+与NH3的配合反应,其原理是
(2)加入H2O2溶液时发生反应的离子方程式为
(3)向三颈烧瓶中先滴加氨水后滴加H2O2的原因是
(4)已知:稀盐酸可将吸附在活性炭上的[Co(NH3)6]Cl3溶解。请补充完整第三步实验方案:将三颈烧瓶中所得混合物充分搅拌、趁热过滤,
(5)为测定产品中钴的含量,进行下列实验:
称取3.5400g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液12.00mL。(反应原理:Co3++I-→Co2++I2、I2+S2O
 →I-+S4O
→I-+S4O 未配平),计算产品中钴元素的质量分数
未配平),计算产品中钴元素的质量分数
您最近一年使用:0次
2023-10-19更新
|
310次组卷
|
3卷引用:江苏省常熟中学2023-2024学年高三上学期阶段性抽测一化学试题
名校
解题方法
10 . 抗原检测盒中T线处使用的是胶体金(Au)标记物。一种从被 包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去
包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去 而露出金矿物,再加入
而露出金矿物,再加入 溶液和
溶液和 溶液对金矿物进行浸取,得到含金的溶液,然后加入
溶液对金矿物进行浸取,得到含金的溶液,然后加入 置换出
置换出 。其工艺流程如下:
。其工艺流程如下:
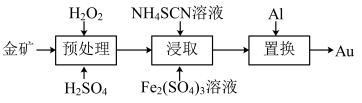
(1)①“预处理”时,用 将
将 直接氧化为
直接氧化为 和硫酸,写出该反应的化学方程式
和硫酸,写出该反应的化学方程式______ 。
②研究发现:在 的催化作用下,
的催化作用下, 产生具有强氧化能力的中间体
产生具有强氧化能力的中间体 ,
, 将金表面的
将金表面的 氧化溶出,
氧化溶出, 越多,
越多, 溶出率越高.
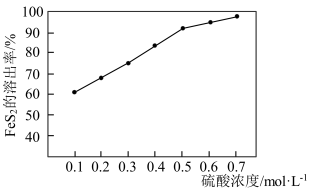
溶出率越高. 溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,
溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大, 溶出率逐渐提高的主要原因是
溶出率逐渐提高的主要原因是________ 。
(2)“置换”时需维持无氧环境,其主要原因是_________ 。
(3)测定样品中 的含量:准确称取
的含量:准确称取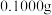 试样,加入王水,将样品中的
试样,加入王水,将样品中的 完全转化成具有强氧化性的氯金酸
完全转化成具有强氧化性的氯金酸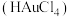 ,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量
,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量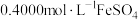 溶液
溶液 ,将
,将 完全还原为
完全还原为 ,滴加二苯胺磺酸钠作指示剂,用
,滴加二苯胺磺酸钠作指示剂,用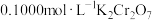 标准溶液滴定至终点(将剩余的
标准溶液滴定至终点(将剩余的 恰好完全氧化),消耗
恰好完全氧化),消耗 溶液
溶液 。
。
已知: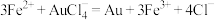

计算样品中金的质量分数(写出计算过程)_____________ 。
 包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去
包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去 而露出金矿物,再加入
而露出金矿物,再加入 溶液和
溶液和 溶液对金矿物进行浸取,得到含金的溶液,然后加入
溶液对金矿物进行浸取,得到含金的溶液,然后加入 置换出
置换出 。其工艺流程如下:
。其工艺流程如下:

(1)①“预处理”时,用
 将
将 直接氧化为
直接氧化为 和硫酸,写出该反应的化学方程式
和硫酸,写出该反应的化学方程式②研究发现:在
 的催化作用下,
的催化作用下, 产生具有强氧化能力的中间体
产生具有强氧化能力的中间体 ,
, 将金表面的
将金表面的 氧化溶出,
氧化溶出, 越多,
越多, 溶出率越高.
溶出率越高. 溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,
溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大, 溶出率逐渐提高的主要原因是
溶出率逐渐提高的主要原因是
(2)“置换”时需维持无氧环境,其主要原因是
(3)测定样品中
 的含量:准确称取
的含量:准确称取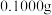 试样,加入王水,将样品中的
试样,加入王水,将样品中的 完全转化成具有强氧化性的氯金酸
完全转化成具有强氧化性的氯金酸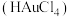 ,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量
,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量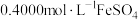 溶液
溶液 ,将
,将 完全还原为
完全还原为 ,滴加二苯胺磺酸钠作指示剂,用
,滴加二苯胺磺酸钠作指示剂,用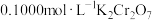 标准溶液滴定至终点(将剩余的
标准溶液滴定至终点(将剩余的 恰好完全氧化),消耗
恰好完全氧化),消耗 溶液
溶液 。
。已知:
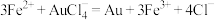

计算样品中金的质量分数(写出计算过程)
您最近一年使用:0次
2023-04-25更新
|
1052次组卷
|
2卷引用:江苏省泰州中学2022-2023学年高一上学期期末考试化学试题



