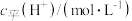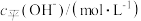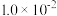解题方法
1 . 室温条件下,测得强碱NaOH溶液的浓度为1.0×10-3mol·L-1,计算该溶液的pH。_________ 。
您最近一年使用:0次
解题方法
2 . 室温下测得某酸溶液中的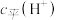 为
为 ,根据
,根据 ,则该酸溶液中的
,则该酸溶液中的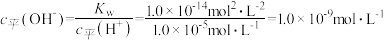 。
。
下表列出了室温下一些溶液的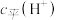 或
或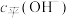 ,请填上空缺的数据。
,请填上空缺的数据。
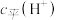 为
为 ,根据
,根据 ,则该酸溶液中的
,则该酸溶液中的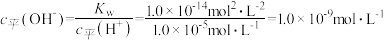 。
。下表列出了室温下一些溶液的
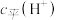 或
或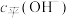 ,请填上空缺的数据。
,请填上空缺的数据。化合物 |
|
|
|
|
|
| |
|
|
| |
|
|
| |
|
|
|
您最近一年使用:0次
解题方法
3 . 将等物质的量的A、B充入容积为 的密闭容器中,发生反应
的密闭容器中,发生反应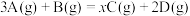 。
。 后,测得D的浓度为
后,测得D的浓度为 ,
,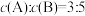 ,C的反应速率是
,C的反应速率是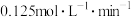 ,此时A的物质的量浓度为
,此时A的物质的量浓度为_________ ,B的反应速率为__________ ,x的值是_________ 。
 的密闭容器中,发生反应
的密闭容器中,发生反应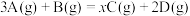 。
。 后,测得D的浓度为
后,测得D的浓度为 ,
,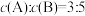 ,C的反应速率是
,C的反应速率是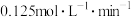 ,此时A的物质的量浓度为
,此时A的物质的量浓度为
您最近一年使用:0次
2020-09-17更新
|
367次组卷
|
3卷引用:鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率
解题方法
4 . 反应 在一容积为
在一容积为 的密闭容器中进行,试回答下列问题:
的密闭容器中进行,试回答下列问题:
(1)若要加快该反应的反应速率,可采取的措施有___________________ 。
(2)开始时, 的浓度是
的浓度是 ,
, 的浓度是
的浓度是 ,
, 内,
内, 的浓度减少
的浓度减少 ,则
,则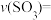
_____________ 。在 末,
末, 的浓度是
的浓度是__________ , 的浓度是
的浓度是________ 。
 在一容积为
在一容积为 的密闭容器中进行,试回答下列问题:
的密闭容器中进行,试回答下列问题:(1)若要加快该反应的反应速率,可采取的措施有
(2)开始时,
 的浓度是
的浓度是 ,
, 的浓度是
的浓度是 ,
, 内,
内, 的浓度减少
的浓度减少 ,则
,则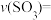
 末,
末, 的浓度是
的浓度是 的浓度是
的浓度是
您最近一年使用:0次
5 . 近20年来,科学工作者对氢能源的研究取得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列制氢气的方法中既经济又符合资源可持续利用的是___________ (填标号)。
A.电解水 B.锌和稀硫酸反应 C.光解海水 D.分解天然气
(2)氢气燃烧时耗氧量小,放出的热量多。已知:
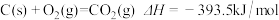
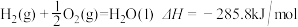
等质量的氢气和碳完全燃烧时放出的热量之比约是__________ 。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列制氢气的方法中既经济又符合资源可持续利用的是
A.电解水 B.锌和稀硫酸反应 C.光解海水 D.分解天然气
(2)氢气燃烧时耗氧量小,放出的热量多。已知:
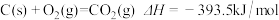
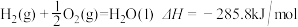
等质量的氢气和碳完全燃烧时放出的热量之比约是
您最近一年使用:0次
2020-09-17更新
|
359次组卷
|
2卷引用:鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第1节 化学反应的热效应
6 . 图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。热化学硫碘循环水分解制氢系统(Ⅰ)
H2SO4(aq)=SO2(g)+H2O(l)+ O2(g) △H1=+327 kJ/mol
O2(g) △H1=+327 kJ/mol
SO2(g)+I2(s)+2H2O(l)=2HI(aq)+H2SO4(aq) △H2=-151 kJ/mol
2HI(aq)= H2(g)+ I2(s) △H3=+110 kJ/mol
H2S(g)+H2SO4(aq)=S(s)+SO2(g)+2H2O(l) △H4=+61 kJ/mol
热化学硫碘循环硫化氢分解联产氢气、硫黄系统(Ⅱ),通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为_______ 、_________ ,制得等量 所需能量较少的是
所需能量较少的是______________ 。
H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g) △H1=+327 kJ/mol
O2(g) △H1=+327 kJ/molSO2(g)+I2(s)+2H2O(l)=2HI(aq)+H2SO4(aq) △H2=-151 kJ/mol
2HI(aq)= H2(g)+ I2(s) △H3=+110 kJ/mol
H2S(g)+H2SO4(aq)=S(s)+SO2(g)+2H2O(l) △H4=+61 kJ/mol
热化学硫碘循环硫化氢分解联产氢气、硫黄系统(Ⅱ),通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为
 所需能量较少的是
所需能量较少的是
您最近一年使用:0次
解题方法
7 . (1)已知:

则反应 的
的
_____  。
。
(2) 催化重整反应为
催化重整反应为 。
。
已知:


该催化重整反应的
_____  。
。
(3) 在催化剂作用下发生反应:
在催化剂作用下发生反应:


则反应 的
的 为
为______  。
。
(4)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:


反应 的
的
______ 


则反应
 的
的
 。
。(2)
 催化重整反应为
催化重整反应为 。
。已知:



该催化重整反应的

 。
。(3)
 在催化剂作用下发生反应:
在催化剂作用下发生反应:

则反应
 的
的 为
为 。
。(4)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下:

反应
 的
的

您最近一年使用:0次
解题方法
8 . (1)已知在 、
、 时,反应
时,反应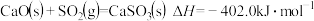 ,
,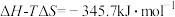 ,若该反应的
,若该反应的 和
和 不随温度变化而变化,则保持该反应能自发进行的温度应低于
不随温度变化而变化,则保持该反应能自发进行的温度应低于_______ (结果保留整数)。
(2)已知: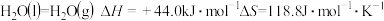 ,则水的沸点是
,则水的沸点是_______ (结果保留1位小数)。
(3)已知在 时,由石墨转化为金刚石的反应的
时,由石墨转化为金刚石的反应的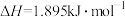 ,
,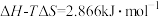 ,石墨的熵S石
,石墨的熵S石 ,则金刚石的熵S金=
,则金刚石的熵S金=________ ,这两种碳的同素异形体中更有序的是________ 。
 、
、 时,反应
时,反应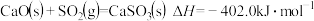 ,
,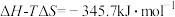 ,若该反应的
,若该反应的 和
和 不随温度变化而变化,则保持该反应能自发进行的温度应低于
不随温度变化而变化,则保持该反应能自发进行的温度应低于(2)已知:
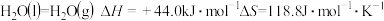 ,则水的沸点是
,则水的沸点是(3)已知在
 时,由石墨转化为金刚石的反应的
时,由石墨转化为金刚石的反应的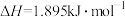 ,
,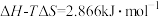 ,石墨的熵S石
,石墨的熵S石 ,则金刚石的熵S金=
,则金刚石的熵S金=
您最近一年使用:0次
2020-09-16更新
|
348次组卷
|
3卷引用:鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向
鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向(已下线)第2章能力提升测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)上海市嘉定区安亭高级中学2022-2023学年高二上学期期中考试化学试题
解题方法
9 . 如图所示A为直流电源,B为电解槽,c、d为石墨电极,B中盛有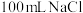 和
和 的混合溶液,其中
的混合溶液,其中 的物质的量浓度为
的物质的量浓度为 ,闭合S,d极收集到标准状况下的气体甲
,闭合S,d极收集到标准状况下的气体甲 ,该气体能使湿润的淀粉碘化钾试纸变蓝。假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收。请回答下列问题:
,该气体能使湿润的淀粉碘化钾试纸变蓝。假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收。请回答下列问题:
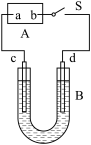
(1)电源的a极是______ ,d极发生的电极反应为_________________ 。
(2)c极理论上收集到的气体的体积是___________ (标准状况) 。
。
(3)假设 溶液中,
溶液中,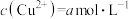 ,
,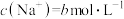 ,
, 完全放电后,理论上d极共产生甲气体的体积V(标准状况)的范围是
完全放电后,理论上d极共产生甲气体的体积V(标准状况)的范围是______ (用含a、b的代数式表示)。
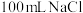 和
和 的混合溶液,其中
的混合溶液,其中 的物质的量浓度为
的物质的量浓度为 ,闭合S,d极收集到标准状况下的气体甲
,闭合S,d极收集到标准状况下的气体甲 ,该气体能使湿润的淀粉碘化钾试纸变蓝。假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收。请回答下列问题:
,该气体能使湿润的淀粉碘化钾试纸变蓝。假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收。请回答下列问题:
(1)电源的a极是
(2)c极理论上收集到的气体的体积是
 。
。(3)假设
 溶液中,
溶液中,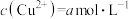 ,
,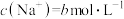 ,
, 完全放电后,理论上d极共产生甲气体的体积V(标准状况)的范围是
完全放电后,理论上d极共产生甲气体的体积V(标准状况)的范围是
您最近一年使用:0次
2020-09-16更新
|
618次组卷
|
2卷引用:鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第3节 电能转化为化学能——电解
解题方法
10 . 在某化学反应中,反应混合物A、B、C的物质的量浓度(mol·L-1)与时间t(s)的关系如下表所示。
(1)该反应的化学方程式为____________ 。
(2)用A的浓度变化表示200~800 s内反应的平均反应速率为_______ mol/(L·min)。
(3)用C的浓度变化表示400~800 s内反应的平均反应速率为________ mol/(L·s)。
t/s | 200 | 400 | 800 |
c(A)/mol·L-1 | 1.45 | 1.28 | 1.00 |
c(B)/mol·L-1 | 0.38 | 0.72 | 1.28 |
c(C)/mol·L-1 | 0.095 | 0.18 | 0.32 |
(2)用A的浓度变化表示200~800 s内反应的平均反应速率为
(3)用C的浓度变化表示400~800 s内反应的平均反应速率为
您最近一年使用:0次