名校
解题方法
1 . 已知 时,部分电解质的电离常数如下表所示:
时,部分电解质的电离常数如下表所示:
(1)根据在 时,用蒸馏水稀释
时,用蒸馏水稀释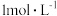 的醋酸溶液至
的醋酸溶液至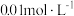 ,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
(2)常温下,同浓度的下列物质的水溶液 最小的是_____。(单选)
最小的是_____。(单选)
(3)常温下,下列操作(忽略过程中温度变化)可以使亚硫酸稀溶液中的 增大的是_____。(单选)
增大的是_____。(单选)
(4)下列关于 溶液中微粒关系错误的是_____。(不定项)
溶液中微粒关系错误的是_____。(不定项)
(5)向 溶液中通入少量
溶液中通入少量 ,写出反应的离子方程式
,写出反应的离子方程式_____ 。
(6)含镉 废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下,
废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下, 、
、 。若用
。若用 处理
处理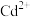 实现沉淀转化,写出反应的离子方程式:
实现沉淀转化,写出反应的离子方程式:_____ ,此时该反应的化学平衡常数为_____ 。
 时,部分电解质的电离常数如下表所示:
时,部分电解质的电离常数如下表所示:| 电解质 |  | 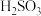 |
| 电离常数 | 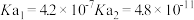 | 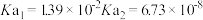 |
| 电解质 | 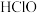 |  |
| 电离常数 |  | 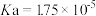 |
 时,用蒸馏水稀释
时,用蒸馏水稀释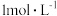 的醋酸溶液至
的醋酸溶液至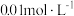 ,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)A. | B.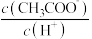 |
C.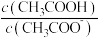 | D. |
 最小的是_____。(单选)
最小的是_____。(单选)A.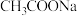 | B. | C. | D. |
 增大的是_____。(单选)
增大的是_____。(单选)A.通入 气体 气体 | B.通入 气体 气体 | C.加入 固体 固体 | D.加入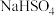 固体 固体 |
 溶液中微粒关系错误的是_____。(不定项)
溶液中微粒关系错误的是_____。(不定项)A.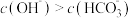 |
B.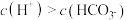 |
C. |
D.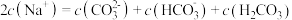 |
 溶液中通入少量
溶液中通入少量 ,写出反应的离子方程式
,写出反应的离子方程式(6)含镉
 废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下,
废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下, 、
、 。若用
。若用 处理
处理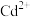 实现沉淀转化,写出反应的离子方程式:
实现沉淀转化,写出反应的离子方程式:
您最近一年使用:0次
2 . 烟气中的SO2可以用钠碱循环法加以处理,用Na2SO3溶液作为吸收液,当吸收液与SO2反应至pH为6左右时,可将吸收液通入电解槽进行再生,吸收液pH随微粒组成的变化关系见表:
| 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
回答下列问题:
(1)吸收液pH由8.2下降至6.2过程中发生反应的离子方程式为
(2)当吸收液呈中性时,溶液中

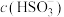 (填“>”“<”或“=”,下同);pH=7.2时,
(填“>”“<”或“=”,下同);pH=7.2时,
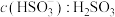 第二步电离平衡常数
第二步电离平衡常数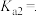
(3)NaHSO3﹣Na2SO3、H2CO3﹣NaHCO3,Na2HPO4﹣NaH2PO4都可组成缓冲溶液,缓冲溶液中lgx[x表示
 或
或 ]与pH的关系如图,当lgx数值在﹣1~1之间时具有可实用价值的缓冲能力,曲线
]与pH的关系如图,当lgx数值在﹣1~1之间时具有可实用价值的缓冲能力,曲线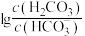 与pH的变化关系,应控制Na2HPO4﹣NaH2PO4缓冲溶液的pH范围为
与pH的变化关系,应控制Na2HPO4﹣NaH2PO4缓冲溶液的pH范围为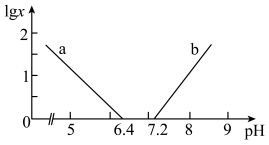
您最近一年使用:0次
名校
3 . NOx、SO2是大气的主要污染物。研究消除NOx、SO2的方法和机理一直是环境专家不断追求的目标。
I.南京大学某教授研究团队以CO同时还原NOx和SO2过程为研究对象,发现在一定温度下,平衡体系中发生的反应为:
①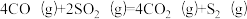
②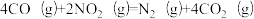
在该温度下,总压为4MPa条件下,以n(CO):n(SO2):n(NO2)=2:1:1通入,t1s后达到平衡,CO2的分压为aMPa,N2的分压为bMPa。
(1)当t1s达平衡时,以CO表示的反应速率为______________________ MPa/s。
(2)反应①在该温度下的Kp=_________________ (MPa)-1。(列出计算式即可,无需化简)
Ⅱ.东南大学化工团队在酸性的条件下,以电化学原理消除NOx、SO2,同时又变废为宝。
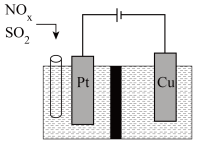
(3)写出NOx转化的电极反应方程式:________________ 。
(4)电解生成的硫酸,电离方程式可表示为: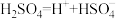 ,
, 。
。
①25°C时,Na2SO4溶液的pH________________ (填“>”“<”或“=”)7。
②0.100mol.L-1的稀硫酸中,c(H+)=0.109mol.L-1,求硫酸第二步电离的电离常数:________________ (写出计算过程,结果保留三位有效数字)。
I.南京大学某教授研究团队以CO同时还原NOx和SO2过程为研究对象,发现在一定温度下,平衡体系中发生的反应为:
①
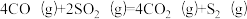
②
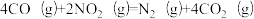
在该温度下,总压为4MPa条件下,以n(CO):n(SO2):n(NO2)=2:1:1通入,t1s后达到平衡,CO2的分压为aMPa,N2的分压为bMPa。
(1)当t1s达平衡时,以CO表示的反应速率为
(2)反应①在该温度下的Kp=
Ⅱ.东南大学化工团队在酸性的条件下,以电化学原理消除NOx、SO2,同时又变废为宝。

(3)写出NOx转化的电极反应方程式:
(4)电解生成的硫酸,电离方程式可表示为:
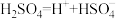 ,
, 。
。①25°C时,Na2SO4溶液的pH
②0.100mol.L-1的稀硫酸中,c(H+)=0.109mol.L-1,求硫酸第二步电离的电离常数:
您最近一年使用:0次
解题方法
4 . 乙酸俗称醋酸,因是醋的主要成分而得名,是一种重要的化工原料。
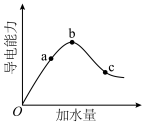
(1)纯的无水乙酸常温下是无色液体,低于16.6℃凝结为类似冰一样的晶体,又称为冰醋酸。一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,加水前导电能力接近零的原因是________ ;a、b、c三点对应的溶液中, 由大到小的顺序是
由大到小的顺序是________ 。
(2)t℃时, 的
的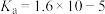 ,0.010mol/L的醋酸溶液中
,0.010mol/L的醋酸溶液中
________ ,pH=________ 。(lg2=0.3)
(3)为了测定某醋酸中 的浓度,某学习小组进行了如下实验:取20.00mL待测溶液,用0.1000mol/LNaOH标准溶液滴定。
的浓度,某学习小组进行了如下实验:取20.00mL待测溶液,用0.1000mol/LNaOH标准溶液滴定。
①滴定加入的指示剂应是________ (选填“甲基橙”或“酚酞”)。滴定终点的颜色变化为________ 。
②滴定操作测得数据记录如下:
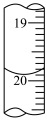
 的读数如上图所示,则
的读数如上图所示,则
________ mL,根据以上实验数据,所测醋酸的浓度是________ mol/L。
③上述实验中,当其它操作正确时,下列操作一定会造成测定结果偏高的是________ (填字母)。
A.待装NaOH标准溶液的滴定管用蒸馏水洗净后,未用标准溶液润洗
B.锥形瓶用蒸馏水洗净后,直接盛装待测液
C.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛NaOH标准溶液的滴定管,滴定前尖嘴部分有气泡,滴定后无气泡
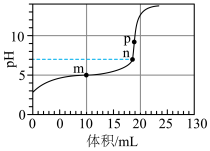
④25℃下,用酸式滴定管量取25.00mL未知浓度的醋酸溶液,放入烧杯中,并放入磁力搅拌子,开启磁力搅拌器,往滴数传感器的滴定管中注入一定量的1.00mol/LNaOH溶液,通过数字化实验,计算机绘制出溶液pH随NaOH溶液体积变化的曲线如图。酸碱刚好完全反应时对应曲线上的________ 点。
(1)纯的无水乙酸常温下是无色液体,低于16.6℃凝结为类似冰一样的晶体,又称为冰醋酸。一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,加水前导电能力接近零的原因是
 由大到小的顺序是
由大到小的顺序是
(2)t℃时,
 的
的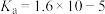 ,0.010mol/L的醋酸溶液中
,0.010mol/L的醋酸溶液中
(3)为了测定某醋酸中
 的浓度,某学习小组进行了如下实验:取20.00mL待测溶液,用0.1000mol/LNaOH标准溶液滴定。
的浓度,某学习小组进行了如下实验:取20.00mL待测溶液,用0.1000mol/LNaOH标准溶液滴定。①滴定加入的指示剂应是
②滴定操作测得数据记录如下:
测定次数 | 滴定前读数/mL | 滴定后读数/mL |
第1次 | 0.20 | 20.14 |
第2次 | 0.12 | 19.98 |
第3次 | 0.00 | 18.30 |
第4次 | 0.00 |
|

 的读数如上图所示,则
的读数如上图所示,则
③上述实验中,当其它操作正确时,下列操作一定会造成测定结果偏高的是
A.待装NaOH标准溶液的滴定管用蒸馏水洗净后,未用标准溶液润洗
B.锥形瓶用蒸馏水洗净后,直接盛装待测液
C.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛NaOH标准溶液的滴定管,滴定前尖嘴部分有气泡,滴定后无气泡
④25℃下,用酸式滴定管量取25.00mL未知浓度的醋酸溶液,放入烧杯中,并放入磁力搅拌子,开启磁力搅拌器,往滴数传感器的滴定管中注入一定量的1.00mol/LNaOH溶液,通过数字化实验,计算机绘制出溶液pH随NaOH溶液体积变化的曲线如图。酸碱刚好完全反应时对应曲线上的

您最近一年使用:0次
名校
5 . 资源化利用二氧化硫,一方面能保护环境,另一方面能提高经济效益,具有深远意义。钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)常温下进行“钠碱法”的模拟实验。用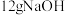 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________ L(折算成标准状况)。若实验时只吸收了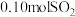 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为___________ 。
(2)当钠碱法的吸收液 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是___________ (填写化学式)。
(3)将 通入
通入 溶液时,得到一组
溶液时,得到一组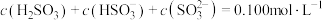 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
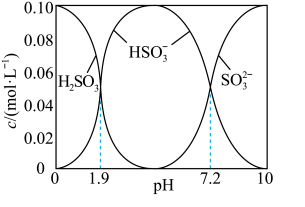
若溶液的 ,溶液中
,溶液中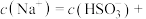
___________ 此时溶液中
___________  。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)
(4)亚硫酸为二元弱酸, 时,其电离常数
时,其电离常数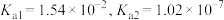 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。___________ 。
(5)工业中可用含 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了___________ (选填编号)。
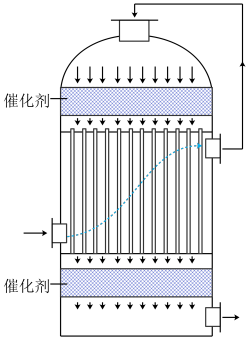
a.充分利用热能 b.防止形成酸雾 c.加速转化 d.获取纯净
d.获取纯净
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)常温下进行“钠碱法”的模拟实验。用
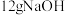 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为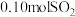 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为(2)当钠碱法的吸收液
 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是(3)将
 通入
通入 溶液时,得到一组
溶液时,得到一组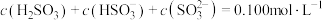 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
若溶液的
 ,溶液中
,溶液中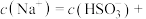

 。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)(4)亚硫酸为二元弱酸,
 时,其电离常数
时,其电离常数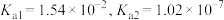 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。(5)工业中可用含
 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了
a.充分利用热能 b.防止形成酸雾 c.加速转化
 d.获取纯净
d.获取纯净
您最近一年使用:0次
名校
6 . 已知常见的酸的电离平衡常数如下(均为常温下的数据):
回答下列问题。
(1)下列事实能证明草酸是弱电解质的是______(填标号)。
(2)同浓度的 、
、 、
、 、
、 中结合
中结合 的能力最强的是
的能力最强的是______ 。
(3)常温下 的
的 溶液在加水稀释过程中,下列表达式的数据一定变小的是______(填标号)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是______(填标号)。
(4)向 溶液中加入少量
溶液中加入少量 溶液,反应
溶液,反应 离子方程式为
离子方程式为____________ 。
(5)常温下,向 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至 ,溶液中
,溶液中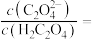
______ 。
(6) 的
的 溶液和
溶液和 的
的 溶液等体积混合,写出混合后溶液中离子浓度由大到小的排序:
溶液等体积混合,写出混合后溶液中离子浓度由大到小的排序:____________ 。
| 化学式 |  | HClO |  |  |
| 电离平衡常数 |  |  | 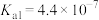  | 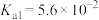 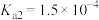 |
(1)下列事实能证明草酸是弱电解质的是______(填标号)。
A.草酸能使酸性 溶液褪色 溶液褪色 |
B.常温下, 的 的 溶液的 溶液的 |
C.相同条件下,浓度均为 的 的 溶液的导电能力比硫酸的导电能力弱 溶液的导电能力比硫酸的导电能力弱 |
D. 溶液中存在 溶液中存在 分子,呈酸性 分子,呈酸性 |
 、
、 、
、 、
、 中结合
中结合 的能力最强的是
的能力最强的是(3)常温下
 的
的 溶液在加水稀释过程中,下列表达式的数据一定变小的是______(填标号)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是______(填标号)。A. | B. | C. | D. |
 溶液中加入少量
溶液中加入少量 溶液,反应
溶液,反应 离子方程式为
离子方程式为(5)常温下,向
 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至 ,溶液中
,溶液中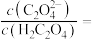
(6)
 的
的 溶液和
溶液和 的
的 溶液等体积混合,写出混合后溶液中离子浓度由大到小的排序:
溶液等体积混合,写出混合后溶液中离子浓度由大到小的排序:
您最近一年使用:0次
名校
7 . 化学反应原理在生产、生活及科学研究中有着广泛的应用。25℃时,部分物质的电离平衡常数如表所示,请结合所提供的数据回答下列问题(注:本题所涉及的选择题,选项不唯一)。
化学式 电离平衡常数(25℃)
HCN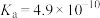
CH3COOH
H2CO3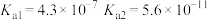
HClO
NH3·H2O
(1)根据上表数据,判断下列反应不能发生的是_______ (填字母)。
A.
B.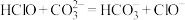
C.
D.
E.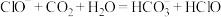
(2)氨水可以吸收CO2.常温下,某氨水的浓度为2mol/L,则溶液中
_______  。将CO2通入氨水中使溶液恰好呈中性,则此时
。将CO2通入氨水中使溶液恰好呈中性,则此时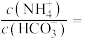
_______ 保留小数点后4位数字)
(3)25℃时,在浓度均为 的①
的① 、②
、② 、③
、③ 的溶液中,
的溶液中, 由大到小的顺序为
由大到小的顺序为_______ (用序号表示)。
(4)25℃时,将 HCN溶液与
HCN溶液与 NaOH溶液等体积混合,混合溶液中①c(Na+)、②c(CN-)、③c(HCN)由大到小的顺序为
NaOH溶液等体积混合,混合溶液中①c(Na+)、②c(CN-)、③c(HCN)由大到小的顺序为_______ (用序号表示)。
(5)25℃时,用 的NaOH溶液滴定20mL
的NaOH溶液滴定20mL 的HCN溶液,当滴加VmLNaOH溶液时,混合溶液的pH=7.HCN的电离常数以
的HCN溶液,当滴加VmLNaOH溶液时,混合溶液的pH=7.HCN的电离常数以 表示,忽略混合时引起的溶液体积的变化,下列叙述不正确的是_______(填写字母)。
表示,忽略混合时引起的溶液体积的变化,下列叙述不正确的是_______(填写字母)。
化学式 电离平衡常数(25℃)
HCN
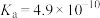
CH3COOH

H2CO3
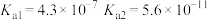
HClO

NH3·H2O

(1)根据上表数据,判断下列反应不能发生的是
A.

B.
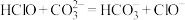
C.

D.

E.
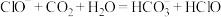
(2)氨水可以吸收CO2.常温下,某氨水的浓度为2mol/L,则溶液中

 。将CO2通入氨水中使溶液恰好呈中性,则此时
。将CO2通入氨水中使溶液恰好呈中性,则此时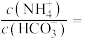
(3)25℃时,在浓度均为
 的①
的① 、②
、② 、③
、③ 的溶液中,
的溶液中, 由大到小的顺序为
由大到小的顺序为(4)25℃时,将
 HCN溶液与
HCN溶液与 NaOH溶液等体积混合,混合溶液中①c(Na+)、②c(CN-)、③c(HCN)由大到小的顺序为
NaOH溶液等体积混合,混合溶液中①c(Na+)、②c(CN-)、③c(HCN)由大到小的顺序为(5)25℃时,用
 的NaOH溶液滴定20mL
的NaOH溶液滴定20mL 的HCN溶液,当滴加VmLNaOH溶液时,混合溶液的pH=7.HCN的电离常数以
的HCN溶液,当滴加VmLNaOH溶液时,混合溶液的pH=7.HCN的电离常数以 表示,忽略混合时引起的溶液体积的变化,下列叙述不正确的是_______(填写字母)。
表示,忽略混合时引起的溶液体积的变化,下列叙述不正确的是_______(填写字母)。| A.V>20 | B.混合溶液的pH=7时: |
C.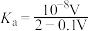 | D.滴定过程中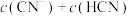 始终不变 始终不变 |
您最近一年使用:0次
8 . 电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
已知部分弱酸的电离常数如下表:
(1)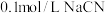 溶液和
溶液和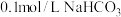 溶液中,
溶液中,
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)常温下,pH相同的三种溶液a. ,b.
,b. ,c.
,c. ,其物质的量浓度由大到小的顺序是
,其物质的量浓度由大到小的顺序是___________ (填编号)。
(3)向 溶液中通入少量
溶液中通入少量 时反应的离子方程式:
时反应的离子方程式:___________ 。
(4)室温下,—定浓度的 溶液
溶液 ,溶液中
,溶液中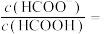
___________ 。
(5)若向 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将___________ (填“增大”、“减小”或“不变”)。
(6)工业废水中的亚硫酸盐过量排放和不恰当的处理方法会引发严重的环境问题,如水体富营养化、水生生物死亡等。工厂废水排放前,可以先用氧化性工业废水(以含酸性 溶液为例)进行处理。常温处理后,再调节pH使
溶液为例)进行处理。常温处理后,再调节pH使 浓度不高于
浓度不高于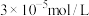 即可排放,调节pH应不低于
即可排放,调节pH应不低于___________ 。[已知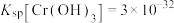 ]
]
(7)常温下, 醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
(8)25℃时,在 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中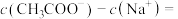
___________  (填精确值)。
(填精确值)。
已知部分弱酸的电离常数如下表:
| 弱酸 |  |  |  |  |  |
| 电离常数(25℃) | 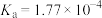 | 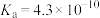 | 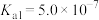  |  | 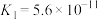 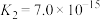 |
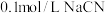 溶液和
溶液和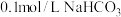 溶液中,
溶液中,
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)常温下,pH相同的三种溶液a.
 ,b.
,b. ,c.
,c. ,其物质的量浓度由大到小的顺序是
,其物质的量浓度由大到小的顺序是(3)向
 溶液中通入少量
溶液中通入少量 时反应的离子方程式:
时反应的离子方程式:(4)室温下,—定浓度的
 溶液
溶液 ,溶液中
,溶液中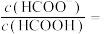
(5)若向
 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将(6)工业废水中的亚硫酸盐过量排放和不恰当的处理方法会引发严重的环境问题,如水体富营养化、水生生物死亡等。工厂废水排放前,可以先用氧化性工业废水(以含酸性
 溶液为例)进行处理。常温处理后,再调节pH使
溶液为例)进行处理。常温处理后,再调节pH使 浓度不高于
浓度不高于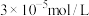 即可排放,调节pH应不低于
即可排放,调节pH应不低于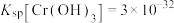 ]
](7)常温下,
 醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。A. | B. |
C. | D.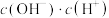 |
 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中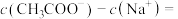
 (填精确值)。
(填精确值)。
您最近一年使用:0次
名校
解题方法
9 . 活性炭载钯(Pd/C)催化剂被广泛应用于医药和化工行业,某废钯催化剂(钯碳)的杂质主要含炭、有机物及少量Fe、Zn等。如图是利用钯碳制备氧化钯( )和Pd的流程。
)和Pd的流程。______ (填仪器名称)中模拟“焚烧”过程。 为二元弱碱,常温下
为二元弱碱,常温下 的电离常数
的电离常数 、
、 ,则常温下0.1mol/L
,则常温下0.1mol/L  水溶液pH=
水溶液pH=______ 。
(2)“溶浸”步骤中钯与王水发生反应生成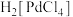 和一种有毒的无色气体A,A为
和一种有毒的无色气体A,A为______ (填化学式),钯的浸出率与反应的时间、温度的关系如图所示,则最佳的浸取时间和温度为______ ,写出“除锌铁”步骤中钯的化合物与试剂Ⅰ反应的化学方程式______ 。______ (填名称),加入该试剂的目的是______ 。
(4)海绵钯具有优良的储氢功能。假设海绵钯的密度为 ,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
______ mol(氢气的浓度r为1mol Pd吸附氢气的物质的量,用含 、n的分数式表示)。
、n的分数式表示)。
 )和Pd的流程。
)和Pd的流程。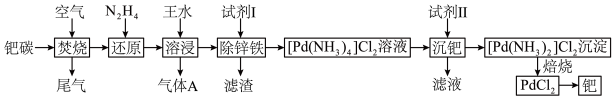
 为二元弱碱,常温下
为二元弱碱,常温下 的电离常数
的电离常数 、
、 ,则常温下0.1mol/L
,则常温下0.1mol/L  水溶液pH=
水溶液pH=(2)“溶浸”步骤中钯与王水发生反应生成
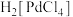 和一种有毒的无色气体A,A为
和一种有毒的无色气体A,A为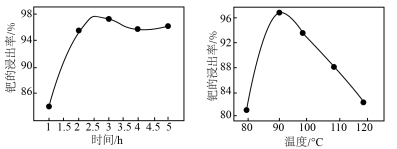
(4)海绵钯具有优良的储氢功能。假设海绵钯的密度为
 ,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
 、n的分数式表示)。
、n的分数式表示)。
您最近一年使用:0次
2024-03-15更新
|
503次组卷
|
4卷引用:山东省聊城市2023-2024学年高三下学期一模化学试题
山东省聊城市2023-2024学年高三下学期一模化学试题 (已下线)化学(山东卷02)-2024年高考押题预测卷2024届四川省绵阳南山中学高三下学期高考仿真演练(一) 理科综合试题-高中化学山东省聊城市2024年高考模拟试题(一) 化学
10 . 雪碧、可乐是深受全球青睐的碳酸型饮料。
Ⅰ.雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,苯甲酸和柠檬酸的电离常数如表所示:
(1)酸性强弱比较:苯甲酸______ 柠檬酸(填“>”“<”或“=”)。
(2)欲使纯水中平衡 向右移动,且溶液显碱性,下列方法可行的是______(填标号)。
向右移动,且溶液显碱性,下列方法可行的是______(填标号)。
Ⅱ.某兴趣小组在实验室测定某可乐中磷酸的含量的实验步骤如下(不考虑白砂糖、咖啡因的影响)。
ⅰ.将50.00mL可乐注入圆底烧瓶,搅拌2~3min,加入6g活性炭,吸附色素。
ⅱ.将可乐回流加热10min,冷却至室温,过滤。
ⅲ.取滤液,用百里香酚酞作指示剂,用 NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液4.60mL。(已知磷酸为三元中强酸。)
NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液4.60mL。(已知磷酸为三元中强酸。)
(3)加热的目的是______ 。
(4)该可乐样品中磷酸的含量为______  (计算结果保留两位小数)。
(计算结果保留两位小数)。
Ⅲ.已知某溶洞水体中lgc(X)(X为H2CO3、、或Ca2+)与pH的关系如图所示。______ (填“ ”“
”“ ”或“Ca2+”)。
”或“Ca2+”)。
②利用上图数据计算,
______ 。
③d=______ (填具体数值)。
Ⅰ.雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,苯甲酸和柠檬酸的电离常数如表所示:
| 化学式 | 苯甲酸(C6H5COOH) | 柠檬酸 |
| 电离常数 | 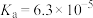 |  |
(1)酸性强弱比较:苯甲酸
(2)欲使纯水中平衡
 向右移动,且溶液显碱性,下列方法可行的是______(填标号)。
向右移动,且溶液显碱性,下列方法可行的是______(填标号)。| A.通入氨气 | B.加入Na |
| C.加入苯甲酸钠固体 | D.加热至90℃ |
Ⅱ.某兴趣小组在实验室测定某可乐中磷酸的含量的实验步骤如下(不考虑白砂糖、咖啡因的影响)。
ⅰ.将50.00mL可乐注入圆底烧瓶,搅拌2~3min,加入6g活性炭,吸附色素。
ⅱ.将可乐回流加热10min,冷却至室温,过滤。
ⅲ.取滤液,用百里香酚酞作指示剂,用
 NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液4.60mL。(已知磷酸为三元中强酸。)
NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液4.60mL。(已知磷酸为三元中强酸。)(3)加热的目的是
(4)该可乐样品中磷酸的含量为
 (计算结果保留两位小数)。
(计算结果保留两位小数)。Ⅲ.已知某溶洞水体中lgc(X)(X为H2CO3、、或Ca2+)与pH的关系如图所示。

 ”“
”“ ”或“Ca2+”)。
”或“Ca2+”)。②利用上图数据计算,

③d=
您最近一年使用:0次