1 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼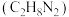 ,
, 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热。
,并放出大量热。
已知:①

②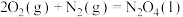

③

请写出上述反应的热化学方程式:______ 。
(2)碘蒸气存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。
下列表述正确的是______。
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中 和
和 发生反应
发生反应

 。实验测得:
。实验测得: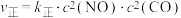 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。
①达到平衡后,仅升高温度, 增大的倍数
增大的倍数______ (填“大于”“小于”或“等于”) 增大的倍数
增大的倍数
②若在 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则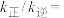
______ 。(保留小数点后两位)
(4)实验室用 溶液处理
溶液处理 ,已知
,已知 ,某吸收液中溶质只含
,某吸收液中溶质只含 ,溶液中
,溶液中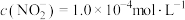 ,取该溶液
,取该溶液 ,加1滴
,加1滴 的
的 溶液混合均匀(20滴约为
溶液混合均匀(20滴约为 ),估算
),估算______ (填“能”或“不能”)产生 沉淀。
沉淀。
(5)一种以液态肼 为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达
为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:______ 。
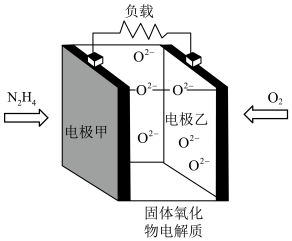
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼
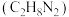 ,
, 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热。
,并放出大量热。已知:①


②
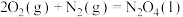

③


请写出上述反应的热化学方程式:
(2)碘蒸气存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。下列表述正确的是______。
A. 分解反应中,k值与碘蒸气浓度大小有关 分解反应中,k值与碘蒸气浓度大小有关 |
| B.第二步对总反应速率起决定作用 |
| C.第二步活化能比第三步大 |
| D.IO为反应的催化剂 |
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中
 和
和 发生反应
发生反应

 。实验测得:
。实验测得: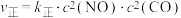 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。①达到平衡后,仅升高温度,
 增大的倍数
增大的倍数 增大的倍数
增大的倍数②若在
 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则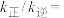
(4)实验室用
 溶液处理
溶液处理 ,已知
,已知 ,某吸收液中溶质只含
,某吸收液中溶质只含 ,溶液中
,溶液中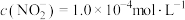 ,取该溶液
,取该溶液 ,加1滴
,加1滴 的
的 溶液混合均匀(20滴约为
溶液混合均匀(20滴约为 ),估算
),估算 沉淀。
沉淀。(5)一种以液态肼
 为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达
为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
您最近一年使用:0次
名校
2 . 直接排放含 的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关 性质的探究活动。
性质的探究活动。
(1)写出证明 弱氧化性的化学方程式
弱氧化性的化学方程式________ 。
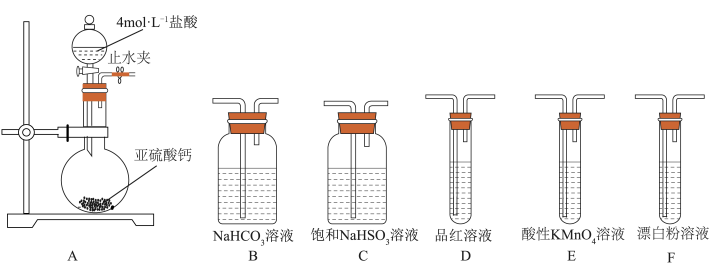
(2)写出下图装置A中滴加盐酸仪器的名称:________ 。
①甲同学认为按照A→C→F顺序连接装置可以比较亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是________ 。
②丙同学设计的合理实验方案为A→________ →尾气处理(填字母)。其中装置C的作用是________ 。证明亚硫酸酸性强于次氯酸的实验现象是________ 。
(4)利用下图的装置可测定装置A残液中 的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使
的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
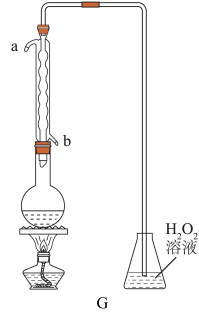
残液中 的含量为
的含量为________  。
。
 的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关 性质的探究活动。
性质的探究活动。(1)写出证明
 弱氧化性的化学方程式
弱氧化性的化学方程式(2)写出下图装置A中滴加盐酸仪器的名称:
①甲同学认为按照A→C→F顺序连接装置可以比较亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是
②丙同学设计的合理实验方案为A→
(4)利用下图的装置可测定装置A残液中
 的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使
的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
残液中
 的含量为
的含量为 。
。
您最近一年使用:0次
2024-03-14更新
|
238次组卷
|
2卷引用:广东省深圳市高级中学2021-2022学年高一下学期期中考试化学试卷
名校
解题方法
3 . I.已知:金属钠和空气可以制备纯度较高的 ,反应原理是:
,反应原理是: ,并且
,并且 易与空气中
易与空气中 、水蒸气反应。现用金属钠和空气制备纯度较高的
、水蒸气反应。现用金属钠和空气制备纯度较高的 ,可利用的装置如图所示。回答下列问题:
,可利用的装置如图所示。回答下列问题:
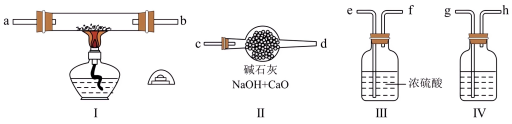
(1)装置Ⅳ中盛放的试剂是_______ ,其作用是_________ 。
(2)若规定气体的气流方向从左到右,则组合实验装置时各接口的连接顺序为:______ →d。
(3)装置Ⅱ的作用是___________ 。
(4)操作中通空气和加热的先后顺序为___________ 。
Ⅱ.为了探究过氧化钠的强氧化性,某小组设计了如图所示的实验装置。
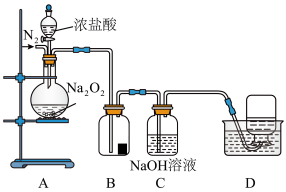
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的 后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有气体产生。
后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭活塞,再通一段时间N₂,直至装置中气体变为无色。
回答下列问题:
(5)装置A中盛装浓盐酸的仪器名称是______ 。
(6)实验中观察到B中湿润的红色纸条褪色,说明在浓盐酸和 的反应中有
的反应中有______ (填化学式)生成。
(7)实验中,在D的集气瓶中收集到能使带火星木条复燃的无色气体,有同学认为该气体是 被浓盐酸还原所得,从氧化还原角度分析该推断是否合理并说明理由?
被浓盐酸还原所得,从氧化还原角度分析该推断是否合理并说明理由?___________ 。
(8)还有同学认为D的集气瓶中收集到的气体是 与浓盐酸中的水反应得到。通过实验证实
与浓盐酸中的水反应得到。通过实验证实 与干燥的
与干燥的 能反应,请完成并配平该化学方程式:
能反应,请完成并配平该化学方程式:________ ,___ +____
+____
 ____
____ +____
+____ +_____。当有0.1mol电子发生转移时,生成的
+_____。当有0.1mol电子发生转移时,生成的 在标况下的体积为
在标况下的体积为______ 。
 ,反应原理是:
,反应原理是: ,并且
,并且 易与空气中
易与空气中 、水蒸气反应。现用金属钠和空气制备纯度较高的
、水蒸气反应。现用金属钠和空气制备纯度较高的 ,可利用的装置如图所示。回答下列问题:
,可利用的装置如图所示。回答下列问题:
(1)装置Ⅳ中盛放的试剂是
(2)若规定气体的气流方向从左到右,则组合实验装置时各接口的连接顺序为:
(3)装置Ⅱ的作用是
(4)操作中通空气和加热的先后顺序为
Ⅱ.为了探究过氧化钠的强氧化性,某小组设计了如图所示的实验装置。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的
 后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有气体产生。
后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有气体产生。③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭活塞,再通一段时间N₂,直至装置中气体变为无色。
回答下列问题:
(5)装置A中盛装浓盐酸的仪器名称是
(6)实验中观察到B中湿润的红色纸条褪色,说明在浓盐酸和
 的反应中有
的反应中有(7)实验中,在D的集气瓶中收集到能使带火星木条复燃的无色气体,有同学认为该气体是
 被浓盐酸还原所得,从氧化还原角度分析该推断是否合理并说明理由?
被浓盐酸还原所得,从氧化还原角度分析该推断是否合理并说明理由?(8)还有同学认为D的集气瓶中收集到的气体是
 与浓盐酸中的水反应得到。通过实验证实
与浓盐酸中的水反应得到。通过实验证实 与干燥的
与干燥的 能反应,请完成并配平该化学方程式:
能反应,请完成并配平该化学方程式: +____
+____
 ____
____ +____
+____ +_____。当有0.1mol电子发生转移时,生成的
+_____。当有0.1mol电子发生转移时,生成的 在标况下的体积为
在标况下的体积为
您最近一年使用:0次
解题方法
4 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有 、
、 、FeO、
、FeO、 等)来制备绿矾(
等)来制备绿矾( )和氧化铝,其工艺流程如图:
)和氧化铝,其工艺流程如图:
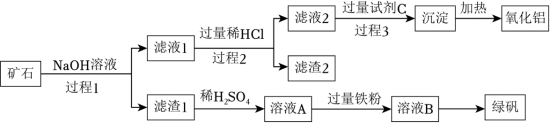
回答下列问题:
(1)过程1中能加快矿石与NaOH溶液反应速率的措施是___________ 。(答一条)
(2)滤渣1的主要成分是___________ ,举例说明滤渣2的用途___________ 。
(3)向溶液A中加入过量铁粉发生反应的离子方程式为:___________ 。
(4)写出由滤液1生成滤液2的离子方程式___________ 。
(5)用来配制试剂C的物质的电子式为:___________ 。
(6)绿矾晶体易被空气中的氧气氧化变质,宜密封保存放置。为探究制备的绿矾样品是否变质,具体的实验操作为___________ 。
 、
、 、FeO、
、FeO、 等)来制备绿矾(
等)来制备绿矾( )和氧化铝,其工艺流程如图:
)和氧化铝,其工艺流程如图:
回答下列问题:
(1)过程1中能加快矿石与NaOH溶液反应速率的措施是
(2)滤渣1的主要成分是
(3)向溶液A中加入过量铁粉发生反应的离子方程式为:
(4)写出由滤液1生成滤液2的离子方程式
(5)用来配制试剂C的物质的电子式为:
(6)绿矾晶体易被空气中的氧气氧化变质,宜密封保存放置。为探究制备的绿矾样品是否变质,具体的实验操作为
您最近一年使用:0次
名校
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中含有碳碳三键的数目一定为 中含有碳碳三键的数目一定为 |
B. 乙烯和丙烯的混合气体中碳原子数目为 乙烯和丙烯的混合气体中碳原子数目为 |
C.常温常压下,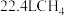 所含电子数目为 所含电子数目为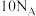 |
D. 时, 时, 完全燃烧所得气体分子数为 完全燃烧所得气体分子数为 |
您最近一年使用:0次
6 . 卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)拟卤素 与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。
与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。 对应的酸有两种,测得硫氰酸
对应的酸有两种,测得硫氰酸 的沸点低于异硫氰酸(
的沸点低于异硫氰酸(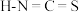 ),其原因是
),其原因是___________ 。
(2) 可与
可与 互溶,从微观角度解释其原因为
互溶,从微观角度解释其原因为___________ ; 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为___________ 。
(3)卤素互化物如 等与卤素单质结构和性质相似。
等与卤素单质结构和性质相似。 沸点由高到低的顺序为
沸点由高到低的顺序为___________ 。
(4)请推测① 、②
、②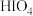 、③
、③ 三种物质的酸性由强到弱的顺序为
三种物质的酸性由强到弱的顺序为___________ (填序号)。
(5) 晶体的晶胞结构与
晶体的晶胞结构与 晶体的相似(如图所示),
晶体的相似(如图所示), 晶体中的哑铃形
晶体中的哑铃形 的存在,使晶胞沿一个方向拉长。此晶体中1个
的存在,使晶胞沿一个方向拉长。此晶体中1个 周围距离最近的
周围距离最近的 为
为___________ 个;若该晶胞的边长为 ,则该晶体的密度为
,则该晶体的密度为___________  (写出表达式)。
(写出表达式)。

(1)拟卤素
 与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。
与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。 对应的酸有两种,测得硫氰酸
对应的酸有两种,测得硫氰酸 的沸点低于异硫氰酸(
的沸点低于异硫氰酸(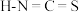 ),其原因是
),其原因是(2)
 可与
可与 互溶,从微观角度解释其原因为
互溶,从微观角度解释其原因为 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为(3)卤素互化物如
 等与卤素单质结构和性质相似。
等与卤素单质结构和性质相似。 沸点由高到低的顺序为
沸点由高到低的顺序为(4)请推测①
 、②
、②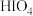 、③
、③ 三种物质的酸性由强到弱的顺序为
三种物质的酸性由强到弱的顺序为(5)
 晶体的晶胞结构与
晶体的晶胞结构与 晶体的相似(如图所示),
晶体的相似(如图所示), 晶体中的哑铃形
晶体中的哑铃形 的存在,使晶胞沿一个方向拉长。此晶体中1个
的存在,使晶胞沿一个方向拉长。此晶体中1个 周围距离最近的
周围距离最近的 为
为 ,则该晶体的密度为
,则该晶体的密度为 (写出表达式)。
(写出表达式)。
您最近一年使用:0次
名校
解题方法
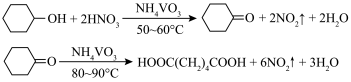
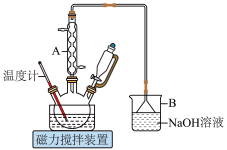
7 . 1,6己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6己二酸。反应原理为:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入0.03 g NH4VO3固体和18 mL浓HNO3(略过量),向恒压滴液漏斗中加入6 mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60 ℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90 ℃水浴中加热10 min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100 mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)仪器A的名称为___________ ,其作用是___________ 。
(2)B中发生反应的离子方程式为___________ (其中一种产物为亚硝酸盐)
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为___________ ,滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60 ℃,说明该反应的ΔH___________ 0(填“>”或“<”)。
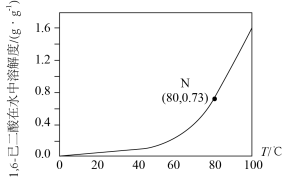
(4)将步骤Ⅲ补充完整:___________ 。步骤Ⅳ提纯方法的名称为___________ 。如图为1,6己二酸在水中的溶解度曲线,80 ℃时1,6-己二酸水溶液的密度为ρ g·mL-1;该溶液的物质的量浓度为___________ 。
| 试剂 | 相对分子质量 | 密度/(g·mL-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 210(分解) | — | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入0.03 g NH4VO3固体和18 mL浓HNO3(略过量),向恒压滴液漏斗中加入6 mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60 ℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90 ℃水浴中加热10 min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100 mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)仪器A的名称为
(2)B中发生反应的离子方程式为
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为
(4)将步骤Ⅲ补充完整:
| A.46.07% | B.57.08% | C.63.03% | D.74.61% |
您最近一年使用:0次
2024-02-29更新
|
361次组卷
|
8卷引用:3.5.2 有机合成路线的设计与实施-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)
(已下线)3.5.2 有机合成路线的设计与实施-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)东北三省三校(哈师大附中、东北师大附中、辽宁省实验中学)2021届高三第一次联合模拟考试(3月)理综化学试题(已下线)重点7 化学实验综合题-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)(已下线)05 以分离提纯为主线的有机制备类综合实验 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型三 以分离提纯为主的有机制备类实验-备战2024年高考化学答题技巧与模板构建河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题四川省成都市第七中学林荫校区2023-2024学年高三下学期4月月考理科综合试卷-高中化学
名校
8 . 某有机物X(分子组成可表示为CxHyOz)是生物体的一种代谢产物,在不同的生命体中发挥不同的功能。现对X进行相关实验:
①取纯净的X固体9.0g(不含结晶水),控制在125℃~150℃缓慢加热,将其完全转化为蒸气,所得X气体所占体积为2.24L(已折算成标准状况);
②取纯净的X固体18.0g(不含结晶水),迅速加热到190℃以上,使其完全分解,得到三种气体产物;
③将分解产物依次通过足量浓硫酸和无水硫酸铜固体,浓硫酸增重3.6g,无水硫酸铜不显蓝色;
④将剩余的气体8.96L(已折算成标准状况)通过足量澄清石灰水,有白色沉淀生成,最后剩余的气体在装置末端可以被点燃;
⑤被点燃的尾气产生蓝色火焰,用干冷的烧杯罩在火焰上方没有水雾产生,用涂有澄清石灰水的烧杯罩在火焰上方有浑浊。
回答下列问题:
(1)有机物X的摩尔质量为___________ ;X分解产物的化学式为___________ 。
(2)通过计算推导出X的分子式(写出计算过程)___________ 。
(3)取0.5g含有杂质的X固体,溶于水配成25.00mL溶液,取所配溶液于锥形瓶中,加入少量硫酸酸化,用KMnO4溶液滴定至X恰好全部氧化成二氧化碳,共消耗0.002mol 的KMnO4.(MnO 转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为___________ 。
①取纯净的X固体9.0g(不含结晶水),控制在125℃~150℃缓慢加热,将其完全转化为蒸气,所得X气体所占体积为2.24L(已折算成标准状况);
②取纯净的X固体18.0g(不含结晶水),迅速加热到190℃以上,使其完全分解,得到三种气体产物;
③将分解产物依次通过足量浓硫酸和无水硫酸铜固体,浓硫酸增重3.6g,无水硫酸铜不显蓝色;
④将剩余的气体8.96L(已折算成标准状况)通过足量澄清石灰水,有白色沉淀生成,最后剩余的气体在装置末端可以被点燃;
⑤被点燃的尾气产生蓝色火焰,用干冷的烧杯罩在火焰上方没有水雾产生,用涂有澄清石灰水的烧杯罩在火焰上方有浑浊。
回答下列问题:
(1)有机物X的摩尔质量为
(2)通过计算推导出X的分子式(写出计算过程)
(3)取0.5g含有杂质的X固体,溶于水配成25.00mL溶液,取所配溶液于锥形瓶中,加入少量硫酸酸化,用KMnO4溶液滴定至X恰好全部氧化成二氧化碳,共消耗0.002mol 的KMnO4.(MnO
 转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
您最近一年使用:0次
2024-02-24更新
|
151次组卷
|
2卷引用:江苏省无锡市第一中学2022-2023学年高一上学期阶段性质量检测化学试题
9 . 回答下列问题。
I.智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O。
(1)反应中___________ 元素被氧化,___________ (填化学式)是氧化剂。
(2)用单线桥标出电子转移方向和数目___________ 。
(3)反应产物中,所得氧化产物与还原产物微粒个数之比为___________ 。
Ⅱ.有一种“地康法”制取氯气的反应原理如图所示:
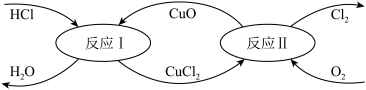
(4)反应Ⅱ的化学方程式为___________ 。
(5)在肉制品加工中,使用发色剂-亚硝酸钠时必须严格控制用量,确保使用安全。某一反应体系中反应物和生成物共有六种:NaNO2、H2O、NO、I2、NaI、HI。已知该反应中NaNO2只发生了如下过程:NaNO2→NO;写出该反应的化学方程式___________ 。
(6)ClO2是一种黄绿色的气体。铬(Cr)的一种固体氧化物Cr2O3与KClO3固体在高温条件下反应,只生成ClO2、Cl2和铬酸钾(K2CrO4)固体三种产物。若该反应中转移24mol电子,生成气体共___________ mol。
I.智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O。
(1)反应中
(2)用单线桥标出电子转移方向和数目
(3)反应产物中,所得氧化产物与还原产物微粒个数之比为
Ⅱ.有一种“地康法”制取氯气的反应原理如图所示:

(4)反应Ⅱ的化学方程式为
(5)在肉制品加工中,使用发色剂-亚硝酸钠时必须严格控制用量,确保使用安全。某一反应体系中反应物和生成物共有六种:NaNO2、H2O、NO、I2、NaI、HI。已知该反应中NaNO2只发生了如下过程:NaNO2→NO;写出该反应的化学方程式
(6)ClO2是一种黄绿色的气体。铬(Cr)的一种固体氧化物Cr2O3与KClO3固体在高温条件下反应,只生成ClO2、Cl2和铬酸钾(K2CrO4)固体三种产物。若该反应中转移24mol电子,生成气体共
您最近一年使用:0次
名校
10 . 黄铁矿的主要成分是FeS2 (Fe为 价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO
价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO +16H+。下列说法中正确的是
+16H+。下列说法中正确的是
 价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO
价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO +16H+。下列说法中正确的是
+16H+。下列说法中正确的是| A.反应中氧化产物和还原产物的物质的量之比为2∶15 |
| B.FeS2是反应中的氧化剂,发生还原反应 |
C.由反应可知氧化性:SO >Fe3+ >Fe3+ |
D.每生成1mol SO ,反应中转移的电子是7mol ,反应中转移的电子是7mol |
您最近一年使用:0次
2024-02-24更新
|
294次组卷
|
3卷引用:江苏省无锡市第一中学2022-2023学年高一上学期阶段性质量检测化学试题



