名校
1 . 下列实验操作合理的是
|
|
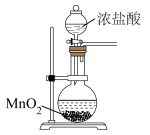
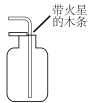
| A.制备氯气 | B.检验氧气是否集满 |
|
|
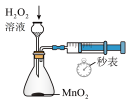
| C.乙炔除杂 | D.测定化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 甲硫醇(CH3SH)是重要的有机化工中间体,可用于合成维生素。通过CH3OH和H2S合成CH3SH的主要反应为:
Ⅰ.
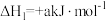
Ⅱ.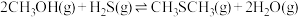
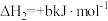
回答下列问题:
(1)计算反应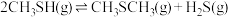 的△H=
的△H=________ kJ/mol。
(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是________ (填选项字母);若按相同比例再充入一定量CH3OH(g)和H2S(g),CH3OH(g)的平衡转化率将________ (填“变大”“变小”或“不变”)。
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为________ (CH3SH的选择性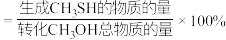 )。
)。
②反应Ⅰ的平衡常数Kp=________ (Kp是用分压表示的平衡常数,结果保留两位小数)。
(4)在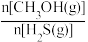 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。________ Mpa/min(结果保留两位有效数字)。
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为________ 。
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:________ 。
Ⅰ.

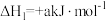
Ⅱ.
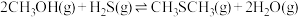
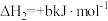
回答下列问题:
(1)计算反应
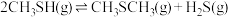 的△H=
的△H=(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为
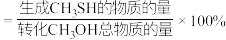 )。
)。②反应Ⅰ的平衡常数Kp=
(4)在
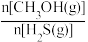 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。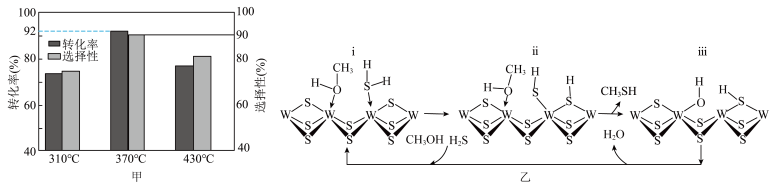
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:
您最近半年使用:0次
3 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
Ⅰ.工业合成氨反应N2(g)+3H2(g) 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
(1)已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量___________ (填“大于”小于或“等于”)920kJ。
(2)工业合成氨选择高温(400-500℃)、高压(10MPa~30MPa)和催化剂的原因是___________ 。
Ⅱ.实验室模拟工业合成氨时,在容积为2L的密闭容器内,开始时加入3molN2(g)和6molH2(g),在10min末,测得NH3(g)的物质的量是2mol。
(3)用N2表示的化学反应速率为___________ mol/(L·min)。
(4)在10min末,H2(g)的转化率为___________ 。
(5)保持容器体积不变,充入惰性气体Ar,化学反应速率___________ (填“增大“减小”或“不变”)。
(6)一定条件下,能说明该反应进行到最大限度的是_______ (填字母)。
a.正、逆反应速率都为零
b.单位时间内消耗3amnolH2(g),同时生成2amolNH3(g)
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
Ⅰ.工业合成氨反应N2(g)+3H2(g)
 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。(1)已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量
(2)工业合成氨选择高温(400-500℃)、高压(10MPa~30MPa)和催化剂的原因是
Ⅱ.实验室模拟工业合成氨时,在容积为2L的密闭容器内,开始时加入3molN2(g)和6molH2(g),在10min末,测得NH3(g)的物质的量是2mol。
(3)用N2表示的化学反应速率为
(4)在10min末,H2(g)的转化率为
(5)保持容器体积不变,充入惰性气体Ar,化学反应速率
(6)一定条件下,能说明该反应进行到最大限度的是
a.正、逆反应速率都为零
b.单位时间内消耗3amnolH2(g),同时生成2amolNH3(g)
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
您最近半年使用:0次
解题方法
4 . 关于2A(g)+B(g) 3C(g)的化学反应,下列表示的反应速率最快的是
3C(g)的化学反应,下列表示的反应速率最快的是
 3C(g)的化学反应,下列表示的反应速率最快的是
3C(g)的化学反应,下列表示的反应速率最快的是| A.v(A)=0.5 mol/(L·min) | B.v(B)=0.4 mol/(L·min) |
| C.v(C)=0.01 mol/(L·s) | D.v(C)=1.1mol/(L·min) |
您最近半年使用:0次
5 . 对反应 来说,同一段时间内,用不同物质表示的化学反应速率(单位相同)的关系正确的是
来说,同一段时间内,用不同物质表示的化学反应速率(单位相同)的关系正确的是
 来说,同一段时间内,用不同物质表示的化学反应速率(单位相同)的关系正确的是
来说,同一段时间内,用不同物质表示的化学反应速率(单位相同)的关系正确的是A.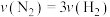 | B.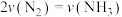 |
C.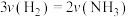 | D. |
您最近半年使用:0次
6 . 根据要求,回答下列问题:
(1)为比较 、
、 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察
分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察______ (填实验现象),即可得出 、
、 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是______  和
和 (草酸)反应速率的影响,设计实验方案如下:
(草酸)反应速率的影响,设计实验方案如下:
上述反应的离子方程式为______ ,该实验是探究______ 对反应速率的影响。
(3)工业制硫酸的反应之一为 ,在2L恒温恒容密闭容器中投入2mol
,在2L恒温恒容密闭容器中投入2mol 和1mol
和1mol 在一定条件下充分反应,下图是
在一定条件下充分反应,下图是 和
和 随时间的变化曲线。
随时间的变化曲线。 的平均反应速率为
的平均反应速率为______ 。
(2)A点的
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)为比较
 、
、 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察
分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察 、
、 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是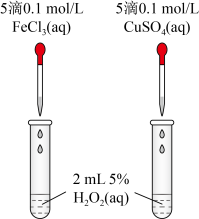
 和
和 (草酸)反应速率的影响,设计实验方案如下:
(草酸)反应速率的影响,设计实验方案如下:实验序号 | 草酸溶液 | 酸性高锰酸钾溶液 |
① |
|
|
② |
|
|
(3)工业制硫酸的反应之一为
 ,在2L恒温恒容密闭容器中投入2mol
,在2L恒温恒容密闭容器中投入2mol 和1mol
和1mol 在一定条件下充分反应,下图是
在一定条件下充分反应,下图是 和
和 随时间的变化曲线。
随时间的变化曲线。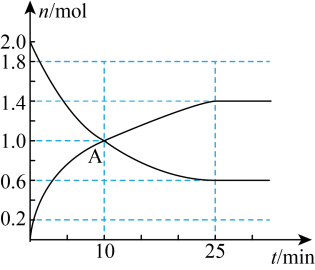
 的平均反应速率为
的平均反应速率为(2)A点的

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近半年使用:0次
7 . 在2L恒容密闭容器中,通入1mol X、0.6mol Y,发生反应: ,2min末,测得Z、W的浓度分别为
,2min末,测得Z、W的浓度分别为 、
、 ,则下列说法错误的是
,则下列说法错误的是
 ,2min末,测得Z、W的浓度分别为
,2min末,测得Z、W的浓度分别为 、
、 ,则下列说法错误的是
,则下列说法错误的是A. | B.反应过程中混合气体的平均相对分子质量不变 |
C.0~2min内,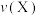 为 为 | D.2min末,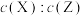 等于8∶3 等于8∶3 |
您最近半年使用:0次
8 . 一定温度下,向2.0L恒容密闭容器中充入1.0mol ,发生反应:
,发生反应: 。反应中测定的部分数据见下表:
。反应中测定的部分数据见下表:
下列说法错误的是
 ,发生反应:
,发生反应: 。反应中测定的部分数据见下表:
。反应中测定的部分数据见下表:t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 时,正反应速率最大,逆反应速率为0 时,正反应速率最大,逆反应速率为0 |
| B.150s时,正反应速率大于逆反应速率 |
C.250s时,反应恰好达到平衡, 的转化率为20% 的转化率为20% |
D.当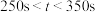 时,反应处于停止状态 时,反应处于停止状态 |
您最近半年使用:0次
9 . 对于可逆反应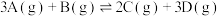 ,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是
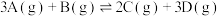 ,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是A. | B.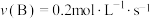 |
C. | D.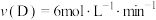 |
您最近半年使用:0次
10 . 某温度时,在一定体积的密闭容器中,某一可逆反应中气体X、Y的物质的量随时间变化的曲线如图所示,则该反应的化学方程式为
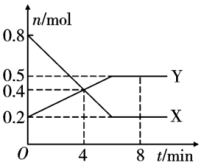
A. | B. | C.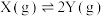 | D.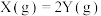 |
您最近半年使用:0次


 、20mL
、20mL 、30mL
、30mL 、20mL
、20mL /mol
/mol

