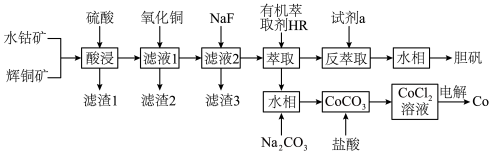
1 . 以水钴矿(Co2O3·H2O,含Fe2O3、MgO、CaO)和辉铜矿(Cu2S,含SiO2、Fe2O3)为原料制取胆矾和单质钴。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
③萃取Cu2+的反应原理;Cu2++2HR CuR2+2H+;
CuR2+2H+;
④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:___________ 。
(2)“滤渣1”的主要成分为___________ 。
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于___________ 。
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为___________ g(忽略溶液体积的变化)。
(5)“反萃取”步骤中加入的“试剂a”为___________ 。
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是___________ 。
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶4∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为___________ 。
①常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaSO4)=7.1×10-7,Ksp(CoCO3)=2.4×10-7;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Cu2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 2.7 | 7.5 | 7.6 | 4.7 |
| 完全沉淀时(c=10-5mol/L)的pH | 3.7 | 9.0 | 9.1 | 6.2 |
 CuR2+2H+;
CuR2+2H+;④Mg、Ca、Fe、Co均能与强酸反应产生H2。
回答下列问题:
(1)“酸浸”过程硫元素价态变为+6价,写出“酸浸”过程中主要反应的化学方程式:
(2)“滤渣1”的主要成分为
(3)常温下,“滤液1”中(Fe元素都以Fe3+形式存在)加“氧化铜”调pH不小于
(4)常温下,若“滤液2”中c(Mg2+)=0.015mol/L(忽略溶液中极少量的Ca2+),除去2L“滤液2”中的Mg2+,至少需加入NaF固体的质量为
(5)“反萃取”步骤中加入的“试剂a”为
(6)采用惰性电极电解CoCl2溶液﹑在无离子交换膜的条件下,不能用CoSO4溶液代替CoCl2溶液的理由是
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入SO2至弱酸性,生成白色沉淀。经仪器分析:白色沉淀含H、N,O、S、Cu五种元素,且Cu∶N∶S=1∶4∶l;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为三角锥形和正四面体形。则白色沉淀的化学式为
您最近一年使用:0次
2 . 实验室以废铜屑(含少量Fe、不溶性杂质)为原料制取 晶体和
晶体和 晶体,其实验流程如下:
晶体,其实验流程如下:
(1)基态Cu原子核外电子排布式为______ 。
(2) 中,中心离子为
中,中心离子为_____ ,其配位数为_____ ,配体是_____ 。
(3) 中,存在的化学键有
中,存在的化学键有______ (填字母)。
a.离子键 b.非极性共价键 c.极性共价键 d.配位键 e.氢键
(4)“氧化”时,在如图所示的装置中进行。从长导管中通入氧气的作用是_______ 。保持试剂的用量不变,实验中提高反应速率的操作有______ (写一种)。该步骤首先加入一定量 的
的 溶液,再调节浓
溶液,再调节浓 的用量至
的用量至 为2.0左右时,铜粉和浓
为2.0左右时,铜粉和浓 完全反应,主要反应的化学方程式为
完全反应,主要反应的化学方程式为_______ 。硝酸过量对产品的影响为______ 。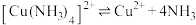 ;
; 、
、 难溶于乙醇。结合下图,
难溶于乙醇。结合下图, 在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的
在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的 溶液制备
溶液制备 晶体的实验方案补充完整:将
晶体的实验方案补充完整:将 溶液加入
溶液加入______ ,所得沉淀先用乙醇—水混合液洗涤,向最后的洗涤滤液中滴加_______ (填试剂)无沉淀生成,再将晶体用无水乙醇洗涤,放入真空干燥箱中干燥。
 晶体和
晶体和 晶体,其实验流程如下:
晶体,其实验流程如下: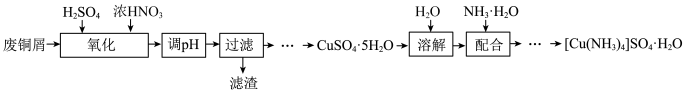
(1)基态Cu原子核外电子排布式为
(2)
 中,中心离子为
中,中心离子为(3)
 中,存在的化学键有
中,存在的化学键有a.离子键 b.非极性共价键 c.极性共价键 d.配位键 e.氢键
(4)“氧化”时,在如图所示的装置中进行。从长导管中通入氧气的作用是
 的
的 溶液,再调节浓
溶液,再调节浓 的用量至
的用量至 为2.0左右时,铜粉和浓
为2.0左右时,铜粉和浓 完全反应,主要反应的化学方程式为
完全反应,主要反应的化学方程式为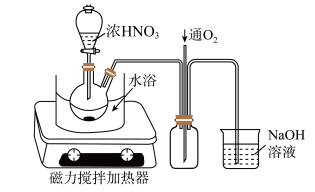
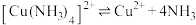 ;
; 、
、 难溶于乙醇。结合下图,
难溶于乙醇。结合下图, 在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的
在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的 溶液制备
溶液制备 晶体的实验方案补充完整:将
晶体的实验方案补充完整:将 溶液加入
溶液加入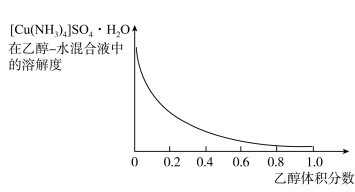
您最近一年使用:0次
名校
3 . 铜、钛、钴及其化合物在生产中有重要作用,回答下列问题
(1)钴元素基态原子的价电子轨道表示式为___________ ,未成对电子数为___________ 。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。与 互为等电子体的阳离子的化学式为
互为等电子体的阳离子的化学式为___________ 。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。___________ (填碳原子旁标的序号)。
(4)配合物[Co(NH3)4(H2O)2]Cl3是钴重要化合物[Co(NH3)4(H2O)2]Cl3中的Co3+配位数为___________ 。根据价电子对互斥理论,预测[Co(NH3)4(H2O)2]2+的立体构型为___________ 体(填相关的立体构型)。
(5)我们通过学习,已经了解到Fe3+溶液在不同溶液中会显示不同的颜色,例如:[Fe(H2O)6]3+溶液显浅紫色(接近无色,肉眼几乎看不见浅紫色);[FeCl4(H2O)2]-溶液显黄色,[Fe(H2O)6-n(OH)n]3-n溶液显黄色。
已知Fe3+溶液存在以下平衡:
[Fe(H2O)6]3++nH2O⇌[Fe(H2O)6-n(OH)n]3-n+nH3O+(正向为Fe3+水解)
[Fe(H2O)6]3++4Cl-⇌[FeCl4(H2O)2]-+4H2O请用上述平衡预测:
若两只盛有等量的Fe(NO3)3固体的试管,向第一只试管加1mL水,向第二只试管加1mL1mol/L稀硝酸,第一只试管发生的现象是___________ ,第二只试管发生的现象是___________ 。
(6)铜与类卤素(SCN)2反应生成Cu(SCN)2,HSCN结构有两种,分别是硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),沸点高的是___________ ,沸点高的原因是:___________ 。
(7)NH4HF2中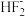 的结构为F-H…F-,则NH4HF2中含有的化学键有
的结构为F-H…F-,则NH4HF2中含有的化学键有___________ (填标号)。
A.氢键 B.价键 C.金属键 D.离子键 E.配位键
(1)钴元素基态原子的价电子轨道表示式为
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。与
 互为等电子体的阳离子的化学式为
互为等电子体的阳离子的化学式为(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。

(4)配合物[Co(NH3)4(H2O)2]Cl3是钴重要化合物[Co(NH3)4(H2O)2]Cl3中的Co3+配位数为
(5)我们通过学习,已经了解到Fe3+溶液在不同溶液中会显示不同的颜色,例如:[Fe(H2O)6]3+溶液显浅紫色(接近无色,肉眼几乎看不见浅紫色);[FeCl4(H2O)2]-溶液显黄色,[Fe(H2O)6-n(OH)n]3-n溶液显黄色。
已知Fe3+溶液存在以下平衡:
[Fe(H2O)6]3++nH2O⇌[Fe(H2O)6-n(OH)n]3-n+nH3O+(正向为Fe3+水解)
[Fe(H2O)6]3++4Cl-⇌[FeCl4(H2O)2]-+4H2O请用上述平衡预测:
若两只盛有等量的Fe(NO3)3固体的试管,向第一只试管加1mL水,向第二只试管加1mL1mol/L稀硝酸,第一只试管发生的现象是
(6)铜与类卤素(SCN)2反应生成Cu(SCN)2,HSCN结构有两种,分别是硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),沸点高的是
(7)NH4HF2中
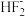 的结构为F-H…F-,则NH4HF2中含有的化学键有
的结构为F-H…F-,则NH4HF2中含有的化学键有A.氢键 B.价键 C.金属键 D.离子键 E.配位键
您最近一年使用:0次
解题方法
4 . 原子序数依次增大的前四周期元素X、Y、Z、W中,X和Y的价电子层中未成对电子均只有1个,并且 和
和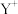 的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
(1)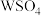 溶于氨水形成
溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中
中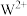 与
与 之间形成的化学键称为
之间形成的化学键称为______ ,提供孤电子对的成键原子是______ (填元素符号)。
②氨气溶于水时,大部分 与
与 以氢键(用“…”表示)结合形成
以氢键(用“…”表示)结合形成 分子。根据氨水的性质可推知
分子。根据氨水的性质可推知 的结构式为
的结构式为______ 。
③往 蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为
蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为____________ 。
(2) 中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的
中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的 的结构式为
的结构式为______ ,其中Z的配位数为______ 。
(3)反应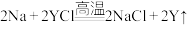 能够发生的原因为
能够发生的原因为____________ 。
 和
和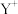 的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:(1)
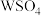 溶于氨水形成
溶于氨水形成 蓝色溶液。
蓝色溶液。①
 中
中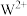 与
与 之间形成的化学键称为
之间形成的化学键称为②氨气溶于水时,大部分
 与
与 以氢键(用“…”表示)结合形成
以氢键(用“…”表示)结合形成 分子。根据氨水的性质可推知
分子。根据氨水的性质可推知 的结构式为
的结构式为③往
 蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为
蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为(2)
 中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的
中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的 的结构式为
的结构式为(3)反应
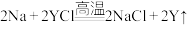 能够发生的原因为
能够发生的原因为
您最近一年使用:0次
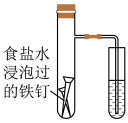
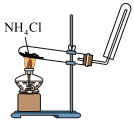
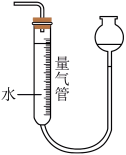
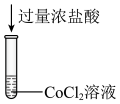
5 . 下列装置可以实现对应实验目的的是
|
|
| A.验证吸氧腐蚀 | B.分离乙醇和 |
|
|
C.制备 | D.测量 体积 体积 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列现象与形成配合物无关的是
| A.向FeCl3溶液中滴入KSCN溶液呈红色 |
B.向Cu与 反应后的集气瓶中加少量水,呈绿色,再加水,呈蓝色 反应后的集气瓶中加少量水,呈绿色,再加水,呈蓝色 |
C.Cu与浓 反应后,溶液呈绿色;Cu与稀 反应后,溶液呈绿色;Cu与稀 反应后,溶液呈蓝色 反应后,溶液呈蓝色 |
| D.向AgNO3溶液中逐滴滴加氨水至过量,先出现白色沉淀,继而沉淀消失 |
您最近一年使用:0次
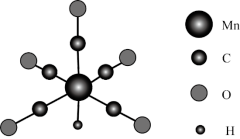
7 . 金属羰基配位化合物在催化反应中有着重要应用。HMn(CO)5是锰的一种简单羰基配位化合物,其结构示意图如下。
(1)基态锰原子的简化电子排布式为___________ 。
(2)配位化合物中的中心原子配位数是指和中心原子直接成键的原子的数目。HMn(CO)5中锰原子的配位数为___________ 。
(3)CH3Mn(CO)5可看作是HMn(CO)5中的氢原子被甲基取代的产物。CH3Mn(CO)5与I2反应可用于制备CH3I,反应前后锰的配位数不变,CH3Mn(CO)5与I2反应的化学方程式为___________ 。
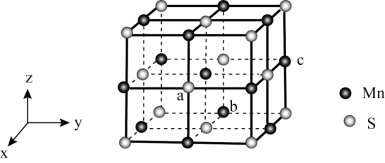
(4)MnS晶胞与NaCl晶胞属于同种类型,如图所示。前者的熔点明显高于后者,其主要原因是___________ 。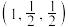 ,b点锰原子坐标为
,b点锰原子坐标为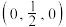 ,则c点锰原子坐标为
,则c点锰原子坐标为___________ 。
(1)基态锰原子的简化电子排布式为
(2)配位化合物中的中心原子配位数是指和中心原子直接成键的原子的数目。HMn(CO)5中锰原子的配位数为
(3)CH3Mn(CO)5可看作是HMn(CO)5中的氢原子被甲基取代的产物。CH3Mn(CO)5与I2反应可用于制备CH3I,反应前后锰的配位数不变,CH3Mn(CO)5与I2反应的化学方程式为
(4)MnS晶胞与NaCl晶胞属于同种类型,如图所示。前者的熔点明显高于后者,其主要原因是
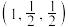 ,b点锰原子坐标为
,b点锰原子坐标为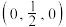 ,则c点锰原子坐标为
,则c点锰原子坐标为
您最近一年使用:0次
8 . 氯化亚铜可用作有机合成的催化剂。以黄铜矿(主要成分为 ,还含杂质
,还含杂质 )为主要原料制备
)为主要原料制备 的流程如下。已知:
的流程如下。已知: 可以溶解在氯离子浓度较大的溶液中,生成
可以溶解在氯离子浓度较大的溶液中,生成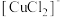 ,
,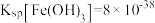 ,
,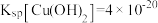 ,
, 。
。___________ (填“大于”或“小于”)锌的第二电离能,其主要原因是___________ 。
(2)“滤渣1”的主要成分为___________ 。
(3)用 溶液调节溶液的
溶液调节溶液的 的值应大于
的值应大于___________ 。
(4)“还原”过程中发生的主要反应的离子方程式为___________ ;该过程中若 的用量过多,造成的后果是
的用量过多,造成的后果是___________ 。
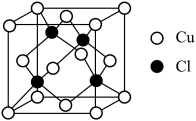
(5)氯化亚铜的立方晶胞如图所示,已知其密度为 ,
, 为阿伏加德罗常数的值,晶胞中
为阿伏加德罗常数的值,晶胞中 的配位数为
的配位数为___________ ,该晶胞参数为___________  。
。
 ,还含杂质
,还含杂质 )为主要原料制备
)为主要原料制备 的流程如下。已知:
的流程如下。已知: 可以溶解在氯离子浓度较大的溶液中,生成
可以溶解在氯离子浓度较大的溶液中,生成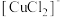 ,
,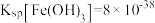 ,
,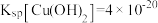 ,
, 。
。
(2)“滤渣1”的主要成分为
(3)用
 溶液调节溶液的
溶液调节溶液的 的值应大于
的值应大于(4)“还原”过程中发生的主要反应的离子方程式为
 的用量过多,造成的后果是
的用量过多,造成的后果是(5)氯化亚铜的立方晶胞如图所示,已知其密度为
 ,
, 为阿伏加德罗常数的值,晶胞中
为阿伏加德罗常数的值,晶胞中 的配位数为
的配位数为 。
。
您最近一年使用:0次
名校
9 . 蓝色的无水 在吸水后会变成粉红色的水合物
在吸水后会变成粉红色的水合物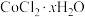 ,该水合物受热后又变成无水
,该水合物受热后又变成无水 ,所以
,所以 常用作吸湿剂和空气湿度指示剂。现有65g无水
常用作吸湿剂和空气湿度指示剂。现有65g无水 ,吸水后变成119g
,吸水后变成119g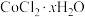 (假设该水合物为配合物),下列说法正确的是
(假设该水合物为配合物),下列说法正确的是
 在吸水后会变成粉红色的水合物
在吸水后会变成粉红色的水合物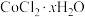 ,该水合物受热后又变成无水
,该水合物受热后又变成无水 ,所以
,所以 常用作吸湿剂和空气湿度指示剂。现有65g无水
常用作吸湿剂和空气湿度指示剂。现有65g无水 ,吸水后变成119g
,吸水后变成119g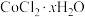 (假设该水合物为配合物),下列说法正确的是
(假设该水合物为配合物),下列说法正确的是| A.Co是第四周期第ⅢB族元素 |
| B.基态氯原子核外电子的空间运动状态有17种 |
C.上述119g 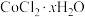 配合物中,所含σ键的物质的量的最大值一定不为20mol 配合物中,所含σ键的物质的量的最大值一定不为20mol |
D.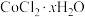 配合物中,所含的化学键为氢键、离子键、共价键和配位键 配合物中,所含的化学键为氢键、离子键、共价键和配位键 |
您最近一年使用:0次
10 . 某小组对 的性质进行探究,实验操作及现象如下,下列说法不正确的是
的性质进行探究,实验操作及现象如下,下列说法不正确的是
资料:
 的性质进行探究,实验操作及现象如下,下列说法不正确的是
的性质进行探究,实验操作及现象如下,下列说法不正确的是资料:
| 物质 |  |  |  | ||||
| 溶液中的颜色 | 粉红色 | 蓝色 | 无色 | ||||
| 操作 |
| 将a中得到的蓝色溶液均分为3份,分别倒入试管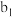 、 、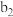 、 、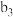 中 中 | |||||
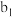 |
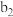 |
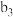 | |||||
| 现象 | a中现象:加入浓盐酸后,溶液由粉红色变为蓝色 | 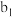 中现象:溶液变为粉红色 中现象:溶液变为粉红色 | 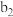 中现象 中现象 | 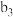 中现象 中现象 | |||
A.试管a中存在平衡: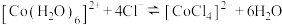 |
B.由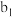 中现象可推测稳定性: 中现象可推测稳定性: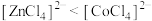 |
C.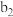 中现象可能为产生白色沉淀 中现象可能为产生白色沉淀 |
D.推测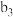 中现象为溶液变为粉红色,因为加入水使各组分离子浓度变化,平衡移动 中现象为溶液变为粉红色,因为加入水使各组分离子浓度变化,平衡移动 |
您最近一年使用:0次