名校
1 . 反应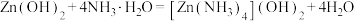 中的有关物质的说法不正确的是
中的有关物质的说法不正确的是
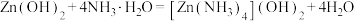 中的有关物质的说法不正确的是
中的有关物质的说法不正确的是A.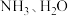 固态时均属于分子晶体 固态时均属于分子晶体 |
B.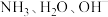 均为 均为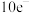 微粒 微粒 |
C. 分子中的键角 分子中的键角 比 比 中的键角 中的键角 大 大 |
D. 中存在离子键、配位键、极性键 中存在离子键、配位键、极性键 |
您最近一年使用:0次
解题方法
2 . 下列实验探究方案能达到探究目的的是
选项 | 探究方案 | |
A | 向 溶液中加入少量 溶液中加入少量 固体,振荡,溶液由蓝色变为黄绿色 固体,振荡,溶液由蓝色变为黄绿色 |  中的配位键稳定性大于 中的配位键稳定性大于 中的配位键 中的配位键 |
B | 向 溶液中滴加淀粉溶液,再通入 溶液中滴加淀粉溶液,再通入 气体,观察现象 气体,观察现象 | 比较 与 与 氧化性的强弱 氧化性的强弱 |
C | 向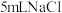 和 和 的混合溶液中,滴加12滴 的混合溶液中,滴加12滴 溶液,观察沉淀颜色 溶液,观察沉淀颜色 | 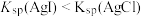 |
D | 向2支分别盛有 不同浓度 不同浓度 溶液的试管中,同时加入 溶液的试管中,同时加入 溶液 溶液 | 探究反应物㳖度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
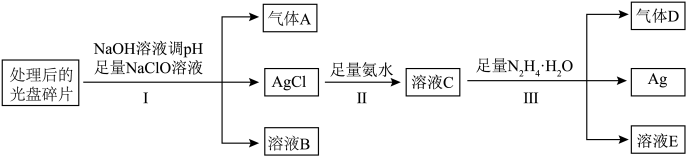
3 . 光盘金属层含有Ag(其它金属微量忽略不计),可以进行资源回收利用,下图为从光盘中提取Ag的工业流程:
②配离子的形成是分步进行的: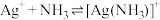
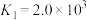 。
。
③AgCl的 ,
,
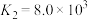 。
。
请回答:
(1)已知Ag位于周期表的第五周期IB族,Ag的原子序数为___________ ;气体A的化学式为___________ ,写出溶液C中所有的阳离子___________ 。
(2)反应Ⅲ的离子方程式为___________ 。
(3)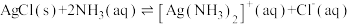 是一个可逆反应。
是一个可逆反应。
①结合相关数据说明上述反应是可逆反应___________ ;
②设计实验验证上述反应是可逆反应___________ 。
②配离子的形成是分步进行的:
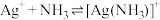
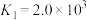 。
。③AgCl的
 ,
,
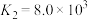 。
。请回答:
(1)已知Ag位于周期表的第五周期IB族,Ag的原子序数为
(2)反应Ⅲ的离子方程式为
(3)
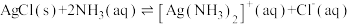 是一个可逆反应。
是一个可逆反应。①结合相关数据说明上述反应是可逆反应
②设计实验验证上述反应是可逆反应
您最近一年使用:0次
解题方法
4 . 胆矾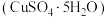 可写为
可写为 ,其结构示意图如图所示:
,其结构示意图如图所示:
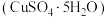 可写为
可写为 ,其结构示意图如图所示:
,其结构示意图如图所示: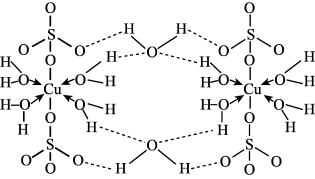
A.胆矾晶体中存在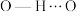 氢键 氢键 | B.胆矾晶体中 的配位数是4 的配位数是4 |
C.基态 的价层电子排布式为 的价层电子排布式为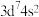 | D.五水硫酸铜晶体是一种含水混合物 |
您最近一年使用:0次
5 . 为测定 中
中 配位数
配位数 ,将浓度均为
,将浓度均为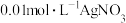 和
和 溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知:
溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知: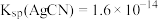 。
。
 中
中 配位数
配位数 ,将浓度均为
,将浓度均为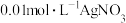 和
和 溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知:
溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知: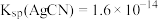 。
。
A.b点对应的 |
B. 中 中 配位数 配位数 |
C.当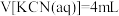 时, 时, |
D.当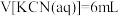 时, 时,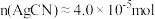 |
您最近一年使用:0次
6 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 固体中含 固体中含 个阴离子 个阴离子 |
B. 分子式为 分子式为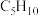 的烃可能含 的烃可能含 个 个 键 键 |
C.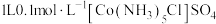 溶液中含 溶液中含 个 个 |
D.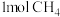 与 与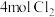 混合光照反应可生成 混合光照反应可生成 个 个 |
您最近一年使用:0次
7 . 由辉铜矿(含 ,少量
,少量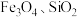 )合成
)合成 的流程如下。
的流程如下。 时,
时, ,
,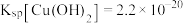 ,离子浓度
,离子浓度 时可认为离子完全沉淀。下列说法正确的是
时可认为离子完全沉淀。下列说法正确的是
 ,少量
,少量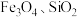 )合成
)合成 的流程如下。
的流程如下。
 时,
时, ,
,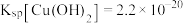 ,离子浓度
,离子浓度 时可认为离子完全沉淀。下列说法正确的是
时可认为离子完全沉淀。下列说法正确的是A.煅烧时只有 两种元素被氧化 两种元素被氧化 |
B.酸浸后,滤液的主要成分为 和 和 |
C.调 为 为 时,可实现铜、铁的分离 时,可实现铜、铁的分离 |
D. 乙醇的作用为增大 乙醇的作用为增大 的溶解度 的溶解度 |
您最近一年使用:0次
解题方法
8 . 副族元素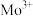 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液_______ ;锰在周期表中的_______ 区。
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为_______ 。
(3)副族元素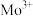 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是_______ ; 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是_______ (填元素符号),其中配体中C原子的杂化方式为_______ , 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为_______ 。
(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是_______ 。
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。_______ ;
② 的熔点
的熔点_______ (填“>”、“<”或“=”) ;
;
③若该八面体边长为 ,则晶胞的密度为
,则晶胞的密度为
_______  (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
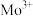 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液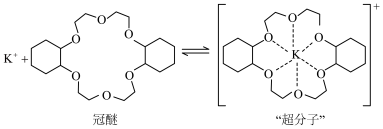
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为
(3)副族元素
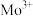 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。

②
 的熔点
的熔点 ;
;③若该八面体边长为
 ,则晶胞的密度为
,则晶胞的密度为
 (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
您最近一年使用:0次
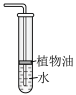
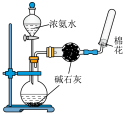
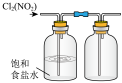
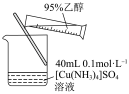
9 . 下列能达到实验目的的是
|
|
| A.吸收氨气 | B.制取并收集氨气 |
|
|
C.除去 中的 中的 | D.析出硫酸四氨合铜晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 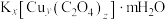 是一种重要的化工原料,其制备及各微粒的测定原理如下:
是一种重要的化工原料,其制备及各微粒的测定原理如下:
 .实验方法:称取
.实验方法:称取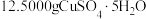 和
和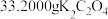 分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
 .重量法测定配合物中结晶水含量
.重量法测定配合物中结晶水含量
将 配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
 .配合物中
.配合物中 及
及 含量
含量
将 中的剩余固体先用1mol/L的
中的剩余固体先用1mol/L的 将其溶解配成250ml溶液,取25ml用酸性
将其溶解配成250ml溶液,取25ml用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,消耗
,消耗 0.0048mol;滴定后的溶液中铜以
0.0048mol;滴定后的溶液中铜以 形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
回答下列问题:
(1)该配合物的配体及配位原子分别是___________ 、___________ 。
(2)本实验减压过滤所需的主要仪器有抽气泵、吸滤瓶及___________ 、___________ 。
(3)根据题干信息分析步骤 使用的洗涤剂为
使用的洗涤剂为___________ 。
(4)酸性滴定的离子反应方程式为___________ 。
(5)已知: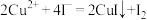 向滴定后的溶液加入足量的KI溶液,用0.6
向滴定后的溶液加入足量的KI溶液,用0.6
 溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为
溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为___________ ;若消耗 溶液的体积为10.00mL。
溶液的体积为10.00mL。 ,步骤
,步骤 中配合物铜的物质的量
中配合物铜的物质的量___________ mol。
(6)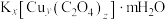 的化学式为:
的化学式为:___________ 。
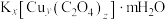 是一种重要的化工原料,其制备及各微粒的测定原理如下:
是一种重要的化工原料,其制备及各微粒的测定原理如下: .实验方法:称取
.实验方法:称取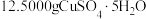 和
和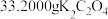 分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。 .重量法测定配合物中结晶水含量
.重量法测定配合物中结晶水含量将
 配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。 .配合物中
.配合物中 及
及 含量
含量将
 中的剩余固体先用1mol/L的
中的剩余固体先用1mol/L的 将其溶解配成250ml溶液,取25ml用酸性
将其溶解配成250ml溶液,取25ml用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,消耗
,消耗 0.0048mol;滴定后的溶液中铜以
0.0048mol;滴定后的溶液中铜以 形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量回答下列问题:
(1)该配合物的配体及配位原子分别是
(2)本实验减压过滤所需的主要仪器有抽气泵、吸滤瓶及
(3)根据题干信息分析步骤
 使用的洗涤剂为
使用的洗涤剂为(4)酸性滴定的离子反应方程式为
(5)已知:
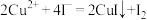 向滴定后的溶液加入足量的KI溶液,用0.6
向滴定后的溶液加入足量的KI溶液,用0.6
 溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为
溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为 溶液的体积为10.00mL。
溶液的体积为10.00mL。 ,步骤
,步骤 中配合物铜的物质的量
中配合物铜的物质的量(6)
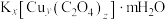 的化学式为:
的化学式为:
您最近一年使用:0次