解题方法
1 . 几种元素在周期表中的位置如图所示,用化学用语(特殊标记的除外)回答下列问题:
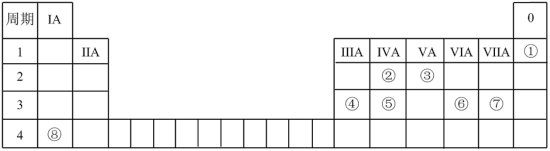
(1)表中所列元素中,①的元素符号是_______ ;金属性最强的是_______ ,该元素在周期表中的位置是_______ 。
(2)②有多种同素异形体,例如足球烯和_______ (填名称)
(3)元素③单质的化学式为_______ ;④的单质与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
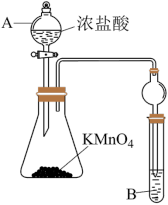
(4)已知 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为_______ ,仪器B中盛放淀粉-碘化钾溶液,所发生的离子反应方程式为_______ ,当观察到_______ 现象时,即可证明非金属性: 。
。

(1)表中所列元素中,①的元素符号是
(2)②有多种同素异形体,例如足球烯和

(3)元素③单质的化学式为
 溶液反应的化学方程式为
溶液反应的化学方程式为(4)已知
 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为 。
。
您最近一年使用:0次
名校
2 . 下表是元素周期表前20号元素的有关信息:
已知:Li的半径为0.152nm,Be的半径为0.111nm。回答下列问题:
(1)元素c在周期表中的位置为________ ,用电子式表示a2e的形成过程:________ 。
(2)f、h、b简单离子半径由大到小的顺序为________ (用离子符号表示)。
(3)BaCl2溶液中先通入eb2,再加入h的单质,可观察到的现象是________ ,发生反应的离子方程式为________ 。
(4)化合物A、B均由a、b、e、f四种元素组成,则A和B相互反应的离子方程式:________ 。
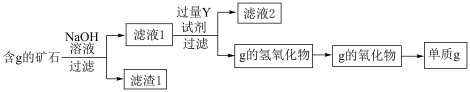
(5)工业上用含g元素的矿石(主要成分为g的氧化物,还含有杂质FeO、Fe2O3)提纯g的氧化物并冶炼单质g,流程如下,滤渣1的成分为:________ (填写化学式),滤液1中通入过量Y试剂反应的离子方程式为:________ 。
| 元素 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.030 | 0.066 | 0.117 | 0.232 | 0.106 | 0.186 | 0.143 | 0.099 |
| 最高正化合价 | +1 | +4 | +1 | +6 | +1 | +3 | +7 | |
| 最低负化合价 | -2 | -4 | -2 | -1 |
(1)元素c在周期表中的位置为
(2)f、h、b简单离子半径由大到小的顺序为
(3)BaCl2溶液中先通入eb2,再加入h的单质,可观察到的现象是
(4)化合物A、B均由a、b、e、f四种元素组成,则A和B相互反应的离子方程式:
(5)工业上用含g元素的矿石(主要成分为g的氧化物,还含有杂质FeO、Fe2O3)提纯g的氧化物并冶炼单质g,流程如下,滤渣1的成分为:

您最近一年使用:0次
解题方法
3 . 下表为长式元素周期表的主要部分。①~⑬代表13种元素,⑭表示元素周期表中某一区域。
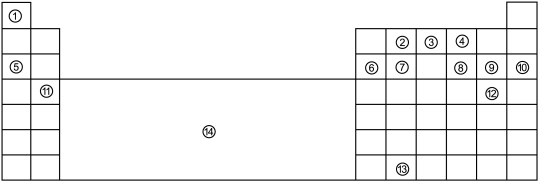
请回答:
(1)①、②、④的原子半径从大到小排列的顺序是______ 。(填化学式)
(2)①与③组成的含10个电子的阳离子的化学式是______ 。
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做______ 元素。
(4)⑩的元素符号是______ 。
(5)⑪的元素名称是______ 。
(6)⑫的原子结构示意图是______ 。
(7)⑬在元素周期表中的位置是______ 。
(8)下列说法不正确 的是______ 。
A. ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数
B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与 溶液反应的化学方程式是
溶液反应的化学方程式是______ 。

请回答:
(1)①、②、④的原子半径从大到小排列的顺序是
(2)①与③组成的含10个电子的阳离子的化学式是
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做
(4)⑩的元素符号是
(5)⑪的元素名称是
(6)⑫的原子结构示意图是
(7)⑬在元素周期表中的位置是
(8)下列说法
A.
 ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与
 溶液反应的化学方程式是
溶液反应的化学方程式是
您最近一年使用:0次
名校
解题方法
4 . 几种主族元素在周期表中的位置如下:
(1)①⑨形成的化合物属于___________ (填“离子化合物”或“共价化合物”),用电子式表示其形成过程___________ 。
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为___________ 。
(3)比较⑦、⑧简单氢化物的还原性:___________ (填化学式);比较①、⑥、⑦三种简单离子的半径大小,其由大到小的顺序___________ (填离子符号)。
(4)下列可以判断①和③金属性强弱的是___________(填字母)。
(5)金属镓 常用作光学玻璃、真空管、半导体的原料。
常用作光学玻璃、真空管、半导体的原料。
预测 的化学性质并填写表格:
的化学性质并填写表格:
以上预测都是依据___________ 。
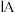 | 0 | |||||||
| 1 | ④ | 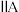 | 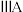 | 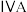 | 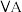 | 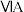 | 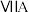 | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑨ | ⑦ | ||||
| 4 | ② |  | ⑧ | |||||
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为
(3)比较⑦、⑧简单氢化物的还原性:
(4)下列可以判断①和③金属性强弱的是___________(填字母)。
A.单质的熔点: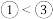 | B.化合价: |
| C.单质与水反应的剧烈程度:①>③ | D.最高价氧化物对应水化物的碱性:①>③ |
 常用作光学玻璃、真空管、半导体的原料。
常用作光学玻璃、真空管、半导体的原料。预测
 的化学性质并填写表格:
的化学性质并填写表格:| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
 能与 能与 | 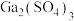 、 、 |
 能与 能与 | 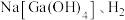 |
您最近一年使用:0次
名校
5 . 如表所示为元素周期表的前四周期部分,根据图示结合所学知识回答下列问题:
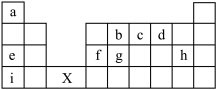
(1)h、i的简单离子半径由大到小的顺序为_______ (填离子符号)。
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______ (填化学式)。
(3)用电子式表示e和h形成离子化合物的过程:________ 。
(4)非金属性:b_______ g(填“>”或“<”);以如图装置进行实验比较b、g对应的最高价氧化物对应水化物的酸性,则试剂A为_______ (填试剂名称),试剂B为_______ 。
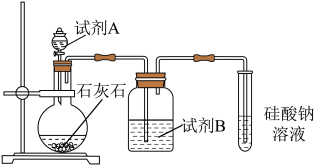
(5)X处包含_______ 纵列,_______ 个族。
(6)i单质与d的简单氢化物反应的离子方程式为_______ 。

(1)h、i的简单离子半径由大到小的顺序为
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)用电子式表示e和h形成离子化合物的过程:
(4)非金属性:b

(5)X处包含
(6)i单质与d的简单氢化物反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答以下问题。
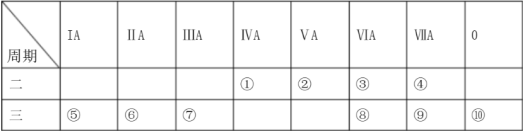
(1)非金属性最强的元素是___________ (填元素符号,下同),最外层电子数是次外层电子数2倍的元素是___________ ,这种元素的一种同位素可用于测定文物年代,这种同位素的符号是___________ 。
(2)与⑥同主族的下一周期的元素是___________ (填元素符号),它在元素周期表中的位置是___________ ,请写出它的原子结构示意图___________ 。
(3)请写出⑦的单质与碱液反应的离子方程式___________ 。

(1)非金属性最强的元素是
(2)与⑥同主族的下一周期的元素是
(3)请写出⑦的单质与碱液反应的离子方程式
您最近一年使用:0次
2024-04-03更新
|
78次组卷
|
2卷引用:四川省雅安市名山区第三中学2023-2024学年高一12月月考化学试题
7 . 下表是元素周期表的一部分。请按要求回答下列问题:
(1)氧元素在周期表中的位置是___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)已知X为第四周期第IIIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIA族元素,写出Y的原子序数b=___________ (用含a的代数式表示)。
(5)下列说法不正确的是___________。
(6)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ | ||||||
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)已知X为第四周期第IIIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIA族元素,写出Y的原子序数b=
(5)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第IVA族 |
| C.第5周期第VIIA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
您最近一年使用:0次
8 . X、Y、Z、W、M、R、T七种短周期元素,周期表中位置如图:
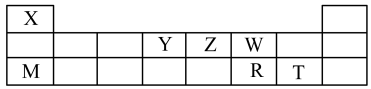
试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是______ (用元素符号表示)。
(2)W的简单氢化物的电子式为_______ 。
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为______ 。
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是______ (用化学式表示)。
(5)M和R最高价氧化物对应水化物反应的离子方程式为______ 。

试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是
(2)W的简单氢化物的电子式为
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是
(5)M和R最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
名校
9 . 元素周期表反映了元素之间的内在联系,是研究物质性质的重要工具。下图是元素周期表的一部分,请结合推断回答下列问题:________ (填元素符号);简单离子半径最小的元素是:________ (填离子符号)。
(2)由这些元素中原子半径最大与最小的两种元素形成的化合物X的电子式为________ ;画出X中阴离子的离子结构示意图:________ 。
(3)⑦⑧两种元素的最高价氧化物的水化物酸性较强的是________ (填化学式)。
(4)⑥的单质与强碱反应的离子方程式为________ 。
(5)根据周期表的结构特点,推断在第四周期中与⑤和⑥同族的元素原子序数相差________ 。
(6)查阅资料可知:⑤的单质可以在①的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:________ 。
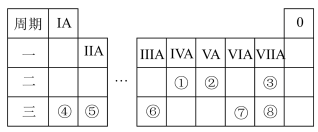
(2)由这些元素中原子半径最大与最小的两种元素形成的化合物X的电子式为
(3)⑦⑧两种元素的最高价氧化物的水化物酸性较强的是
(4)⑥的单质与强碱反应的离子方程式为
(5)根据周期表的结构特点,推断在第四周期中与⑤和⑥同族的元素原子序数相差
(6)查阅资料可知:⑤的单质可以在①的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:
您最近一年使用:0次
2024-04-03更新
|
224次组卷
|
2卷引用:辽宁省名校联盟2023-2024学年高一下学期3月联合考试化学试题
名校
解题方法
10 . 下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素,回答下列问题:
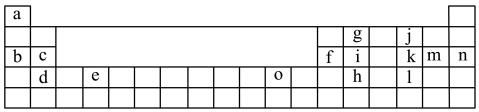
(1)表中所列元素中:属于短周期主族元素的有___________ 种,化学性质最稳定的元素是___________ (填元素符号),h元素在周期表中的位置是___________ 。
(2)下列___________元素的单质可能都是电的良导体。
(3)1元素的最高正化合价为___________ ,b与f两元素的最高价氧化物对应水化物间相互反应的离子方程式为___________ 。
(4)b、c、k三种元素原子半径由大到小的顺序是___________ (用元素符号作答)。
(5)比较c和d两元素原子的失电子能力的强弱,并从原子结构角度进行论证___________ 。
(6)比较元素i、k、m的最高价氧化物对应水化物,按酸性从强到弱的顺序排列为___________ 。

(1)表中所列元素中:属于短周期主族元素的有
(2)下列___________元素的单质可能都是电的良导体。
| A.b、c、i | B.a、g、k | C.c、g、o | D.d、e、f |
(3)1元素的最高正化合价为
(4)b、c、k三种元素原子半径由大到小的顺序是
(5)比较c和d两元素原子的失电子能力的强弱,并从原子结构角度进行论证
(6)比较元素i、k、m的最高价氧化物对应水化物,按酸性从强到弱的顺序排列为
您最近一年使用:0次



