名校
解题方法
1 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~g7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是_______ 。
(3)非金属性e强于g,用原子结构解释原因:_______ ,得电子能力e大于g。
(4)下列对f及其化合物的推断中,正确的是_______ (填序号)。
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | a | |||||||
| 3 | b | c | d | e | ||||
| 4 | f | g |
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是
(3)非金属性e强于g,用原子结构解释原因:
(4)下列对f及其化合物的推断中,正确的是
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
您最近一年使用:0次
解题方法
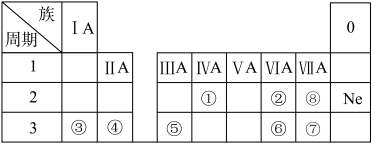
2 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
①___________ ;⑤___________ ;⑦___________ ;⑧___________ 。
(2)②和③元素所组成的化合物中可做供氧剂的是___________ (写化学式)。
(3)⑥元素的原子结构示意图为___________ 。②元素的原子结构示意图为___________ 。
(4)①元素的氧化物中是酸性氧化物的是___________ (写化学式)。
①
(2)②和③元素所组成的化合物中可做供氧剂的是
(3)⑥元素的原子结构示意图为
(4)①元素的氧化物中是酸性氧化物的是
您最近一年使用:0次
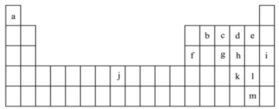
3 . 结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
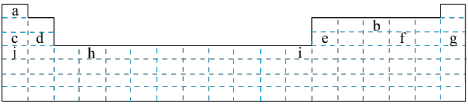
(2)f元素位于第
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
| A.比较四种元素形成的最高价氧化物对应的水化物碱性强弱:j>c>d>e |
| B.比较四种元素形成氢化物的难易程度以及氢化物的热稳定性:j<c<d<e |
| C.比较四种元素形成的单质分别与非氧化性酸反应置换氢气的剧烈程度:c>j>d>e |
| D.将空气中久置的四种元素的块状单质分别放入水中,比较与水反应的剧烈程度:j>c>d>e |
您最近一年使用:0次
名校
解题方法
4 . 1869年俄国化学家门捷列夫制出第一张元素周期表元素,下图是元素周期表的一部分。回答下列问题:
(1)Ga的原子结构示意图为________ 。
(2)Ge位于金属元素和非金属元素的分界处,可以做________ 材料,其最高正价为________ 。
(3)Cl元素的最高价氧化物对应的水化物为________ (填化学式),设计实验方案证明Cl的得电子能力强于S。
(4)Bi的最高价氧化物为________ (填化学式), ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的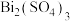 ,该反应的离子方程式为
,该反应的离子方程式为________ 。
(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为________ (填名称),该物质的电子式为________ 。
②氢化物的还原性:
________  (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。
③ 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为________ 。
④ 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为________ (用离子符号表示)。
B | C | N | O | F |
Al | Si | P | S | Cl |
Ga | Ge | As | Se | Br |
In | Sn | Sb | Te | I |
Tl | Pb | Bi | Po | At |
(2)Ge位于金属元素和非金属元素的分界处,可以做
(3)Cl元素的最高价氧化物对应的水化物为
(4)Bi的最高价氧化物为
 ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的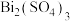 ,该反应的离子方程式为
,该反应的离子方程式为(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为
②氢化物的还原性:

 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。③
 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为④
 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为
您最近一年使用:0次
名校
5 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:________ (用元素符号填空,下同)。
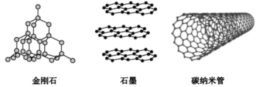
(2)下图为b元素的三种单质,它们互为________ 。________ 。
(4)c的一种氢化物因极易溶于水的性质,可用作喷泉实验,请从物质结构的角度解释溶解度大的原因________ 。
(5)由b、c、h构成的一种阴离子,常用于检验补血剂是否变质,此阴离子的结构可能与________ (请填“ ”、“
”、“ ”或“
”或“ ”)相同。
”)相同。
(6)k常用作光敏材料,基态k原子价层电子占据的最高能级符号为________ ;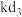 的空间构型为
的空间构型为________ ;熔沸点大小比较: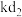
________ 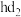 (填“>”、“<”获“=”)。
(填“>”、“<”获“=”)。
(2)下图为b元素的三种单质,它们互为
(4)c的一种氢化物因极易溶于水的性质,可用作喷泉实验,请从物质结构的角度解释溶解度大的原因
(5)由b、c、h构成的一种阴离子,常用于检验补血剂是否变质,此阴离子的结构可能与
 ”、“
”、“ ”或“
”或“ ”)相同。
”)相同。(6)k常用作光敏材料,基态k原子价层电子占据的最高能级符号为
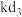 的空间构型为
的空间构型为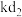
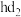 (填“>”、“<”获“=”)。
(填“>”、“<”获“=”)。
您最近一年使用:0次
名校
6 . Ⅰ、已知电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
(1)估计O元素的电负性数值范围________ <X<________
(2)下列物质属于离子化合物的是________ ,属于共价化合物的有________ 。
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
Ⅱ、下表列出了①~⑨九种元素在周期表中的位置:
(3)基态②原子的核外电子有___________ 种空间运动状态。
(4)元素⑦的基态原子价层电子轨道表示式为___________________________ 。
(5)按气态氢化物的稳定性由弱到强的顺序排列,④⑥⑦的简单氢化物稳定性:________ (写氢化物的化学式)。
(6)写出元素⑤形成的单质在氧气中燃烧的化学方程式:___________________ 。
(7)③的简单氢化物与其最高价氧化物的水化物反应的离子方程式:___________________________________ 。
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | X | 2.1 | 2.5 | 1.8 |
(2)下列物质属于离子化合物的是
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
Ⅱ、下表列出了①~⑨九种元素在周期表中的位置:
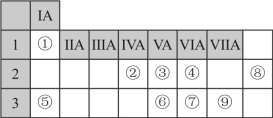
(3)基态②原子的核外电子有
(4)元素⑦的基态原子价层电子轨道表示式为
(5)按气态氢化物的稳定性由弱到强的顺序排列,④⑥⑦的简单氢化物稳定性:
(6)写出元素⑤形成的单质在氧气中燃烧的化学方程式:
(7)③的简单氢化物与其最高价氧化物的水化物反应的离子方程式:
您最近一年使用:0次
7 . Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为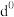 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
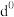 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次
8 . 写出基态Ti原子的下列表示方法。
(1)电子排布式___________ 。
(2)简化电子排布式___________ 。
(3)价层电子排布式___________ 。
(4)价层电子轨道表示式___________ 。
(5)周期表中的位置(周期、族、区)___________ 。
(1)电子排布式
(2)简化电子排布式
(3)价层电子排布式
(4)价层电子轨道表示式
(5)周期表中的位置(周期、族、区)
您最近一年使用:0次
解题方法
9 . 表为元素周期表的一部分,a、b、c……为其中几种元素。回答下列问题:
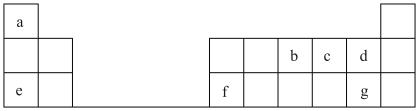
(1)写出b在元素周期表中的位置_______ 。
(2)元素d和g的气态氢化物中,更稳定的是_______ (写化学式)。
(3)元素d、e、g中原子半径由大到小的顺序为_______ (用元素符号表示)。
(4)元素e、g形成的化合物的电子式为_______ ,所含化学键类型为_______ 。
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:_______ 。

(1)写出b在元素周期表中的位置
(2)元素d和g的气态氢化物中,更稳定的是
(3)元素d、e、g中原子半径由大到小的顺序为
(4)元素e、g形成的化合物的电子式为
(5)a、c、e三种元素形成化合物的水溶液与g的最高价氧化物对应水化物反应的离子方程式:
您最近一年使用:0次
解题方法
10 . 几种元素在周期表中的位置如图所示,用化学用语(特殊标记的除外)回答下列问题:
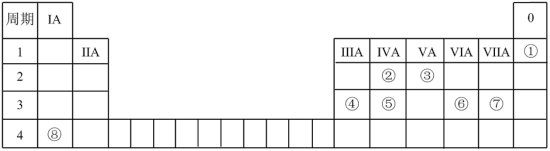
(1)表中所列元素中,①的元素符号是_______ ;金属性最强的是_______ ,该元素在周期表中的位置是_______ 。
(2)②有多种同素异形体,例如足球烯和_______ (填名称)
(3)元素③单质的化学式为_______ ;④的单质与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
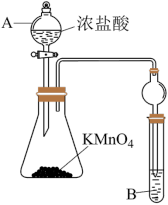
(4)已知 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为_______ ,仪器B中盛放淀粉-碘化钾溶液,所发生的离子反应方程式为_______ ,当观察到_______ 现象时,即可证明非金属性: 。
。

(1)表中所列元素中,①的元素符号是
(2)②有多种同素异形体,例如足球烯和

(3)元素③单质的化学式为
 溶液反应的化学方程式为
溶液反应的化学方程式为(4)已知
 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为 。
。
您最近一年使用:0次



