1 . 回答下列问题
(1)已知 1g 甲烷完全燃烧生成二氧化碳和液态水释放 56kJ 的热量,则甲烷燃烧的热化学方程式___________ 。
(2)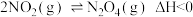 增大压强,平衡
增大压强,平衡___________ 填(“正向移动”“逆向移动”或“不移动”),颜色___________ (填“变深”“变浅”或“不变”)。
(3)工业制备纯硅的反应为 ,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是
,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是___________ kJ。
(1)已知 1g 甲烷完全燃烧生成二氧化碳和液态水释放 56kJ 的热量,则甲烷燃烧的热化学方程式
(2)
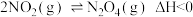 增大压强,平衡
增大压强,平衡(3)工业制备纯硅的反应为
 ,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是
,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是
您最近一年使用:0次
解题方法
2 . 铜与浓硫酸在加热条件下反应生成CuSO4、SO2和H2O,现将6.4g铜与足量的浓硫酸充分反应,铜完全溶解,反应后将溶液稀释至100mL。请计算:
(1)铜的物质的量为_______ mol。
(2)反应生成的SO2的体积(标准状况下)为_______ L。
(3)稀释后溶液中硫酸铜的物质的量浓度_______ 。
(1)铜的物质的量为
(2)反应生成的SO2的体积(标准状况下)为
(3)稀释后溶液中硫酸铜的物质的量浓度
您最近一年使用:0次
解题方法
3 . 某温度(t℃)时,纯水中c(H+)=1.0×10-6.5mol∙L-1。
(1)则该温度下水的离子积常数KW=___________ ;t℃___________ (填“>”、“<”或“=”) 25℃。
(2)将此温度下pH=12的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为___________ ,溶液中由水电离出的c(H+)=___________ (忽略溶液混合时体积的变化)
(3)室温下,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合后混合液的pH=10,则所用H2SO4溶液与NaOH溶液的体积之比是___________ (忽略溶液混合时体积的变化)。
(1)则该温度下水的离子积常数KW=
(2)将此温度下pH=12的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为
(3)室温下,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合后混合液的pH=10,则所用H2SO4溶液与NaOH溶液的体积之比是
您最近一年使用:0次
解题方法
4 . 一定温度下,向容积为 的密闭容器中通入
的密闭容器中通入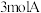 和
和 ,混合气体起始压强为
,混合气体起始压强为 。发生反应:
。发生反应: ,反应进行到
,反应进行到 时测得剩余
时测得剩余 ,此时
,此时 的浓度为
的浓度为 。反应进行到
。反应进行到 时该容器内混合气体总压强为p,5min后反应达到平衡。
时该容器内混合气体总压强为p,5min后反应达到平衡。
(1)x为___________ 。
(2)反应在 内,B的平均反应速率为
内,B的平均反应速率为___________ 。
(3)请用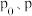 来表示
来表示 时反应物B的转化率为
时反应物B的转化率为___________ 。
(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是___________。
 的密闭容器中通入
的密闭容器中通入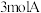 和
和 ,混合气体起始压强为
,混合气体起始压强为 。发生反应:
。发生反应: ,反应进行到
,反应进行到 时测得剩余
时测得剩余 ,此时
,此时 的浓度为
的浓度为 。反应进行到
。反应进行到 时该容器内混合气体总压强为p,5min后反应达到平衡。
时该容器内混合气体总压强为p,5min后反应达到平衡。(1)x为
(2)反应在
 内,B的平均反应速率为
内,B的平均反应速率为(3)请用
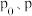 来表示
来表示 时反应物B的转化率为
时反应物B的转化率为(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是___________。
A. | B.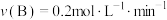 |
C. | D.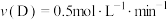 |
您最近一年使用:0次
解题方法
5 . 将硝酸钠(NaNO3)和硝酸钡[Ba(NO3)2]的混合物29.1g放入烧杯,加入100.0g水使其完全溶解,再加入94.2g硫酸钠溶液恰好完全反应,过滤(忽略溶液的损失),称得滤液的质量为200.0g。请计算:
(1)恰好完全反应后产生的沉淀质量为______ g。
(2)所得滤液的溶质质量分数(写出完整的解题过程)________ 。
(1)恰好完全反应后产生的沉淀质量为
(2)所得滤液的溶质质量分数(写出完整的解题过程)
您最近一年使用:0次
6 . 计算填空:
(1)在 时,
时, 在
在 中完全燃烧生成
中完全燃烧生成 放出
放出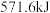 的热量,则
的热量,则 的燃烧热为
的燃烧热为____________________ 。
(2)已知: 的燃烧热为
的燃烧热为 ,
, 和
和 的混合气体
的混合气体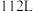 (标准状况下)完全燃烧生成
(标准状况下)完全燃烧生成 和液态水时放出的热量为
和液态水时放出的热量为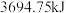 ,则混合气体中
,则混合气体中 和
和 的体积比为
的体积比为____________________ 。
(1)在
 时,
时, 在
在 中完全燃烧生成
中完全燃烧生成 放出
放出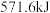 的热量,则
的热量,则 的燃烧热为
的燃烧热为(2)已知:
 的燃烧热为
的燃烧热为 ,
, 和
和 的混合气体
的混合气体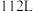 (标准状况下)完全燃烧生成
(标准状况下)完全燃烧生成 和液态水时放出的热量为
和液态水时放出的热量为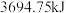 ,则混合气体中
,则混合气体中 和
和 的体积比为
的体积比为
您最近一年使用:0次
7 . )某化学小组为测定有机物G的组成和结构,设计如图实验装置:
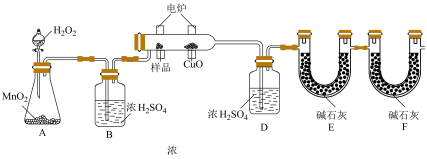
回答下列问题:
(1)实验开始时,先打开__________ (填装置名称),一段时间后再加热反应管C,目的是__________ 。写出A中发生的反应方程式:__________ 。
(2)装置B和装置D中浓硫酸的作用分别是__________ 和__________ 。
(3)装置E和装置F中碱石灰的作用分别是__________ 和__________ 。
(4)若准确称取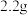 样品G(只含C、H、O三种元素),经充分燃烧后(
样品G(只含C、H、O三种元素),经充分燃烧后( 的作用是确保有机物充分氧化,最终生成
的作用是确保有机物充分氧化,最终生成 和
和 ),装置D质量增加
),装置D质量增加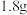 ,U形管E质量增加
,U形管E质量增加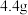 。又知有机物G的质谱图如图所示。
。又知有机物G的质谱图如图所示。
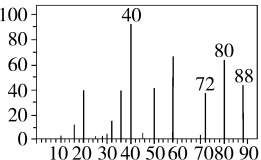
该有机物的分子式为__________ 。
(5)已知有机物G中含有羧基,经测定其核磁共振氢谱有3组峰,且峰面积之比为 。综上所述,G的结构简式为
。综上所述,G的结构简式为__________ 。

回答下列问题:
(1)实验开始时,先打开
(2)装置B和装置D中浓硫酸的作用分别是
(3)装置E和装置F中碱石灰的作用分别是
(4)若准确称取
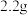 样品G(只含C、H、O三种元素),经充分燃烧后(
样品G(只含C、H、O三种元素),经充分燃烧后( 的作用是确保有机物充分氧化,最终生成
的作用是确保有机物充分氧化,最终生成 和
和 ),装置D质量增加
),装置D质量增加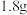 ,U形管E质量增加
,U形管E质量增加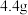 。又知有机物G的质谱图如图所示。
。又知有机物G的质谱图如图所示。
该有机物的分子式为
(5)已知有机物G中含有羧基,经测定其核磁共振氢谱有3组峰,且峰面积之比为
 。综上所述,G的结构简式为
。综上所述,G的结构简式为
您最近一年使用:0次
解题方法
8 . 顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化:

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=_______ 。

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=
您最近一年使用:0次
9 . 常温下 的某一元强碱
的某一元强碱 溶液与
溶液与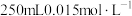 的硫酸溶液相混合,假设混合后液体体积为
的硫酸溶液相混合,假设混合后液体体积为 ,试求:
,试求:
(1)混合液的
___________ 。
(2)若原 一元强碱中含溶质
一元强碱中含溶质 ,则
,则 的相对原子质量为
的相对原子质量为___________ 。
(3)若给混合液中分别滴入几滴甲基橙试液,则溶液的颜色是___________ 。
 的某一元强碱
的某一元强碱 溶液与
溶液与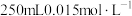 的硫酸溶液相混合,假设混合后液体体积为
的硫酸溶液相混合,假设混合后液体体积为 ,试求:
,试求:(1)混合液的

(2)若原
 一元强碱中含溶质
一元强碱中含溶质 ,则
,则 的相对原子质量为
的相对原子质量为(3)若给混合液中分别滴入几滴甲基橙试液,则溶液的颜色是
您最近一年使用:0次
10 . 化学反应原理对化学反应的研究具有指导意义。
(1)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
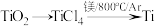
已知:①C(s)+O2(g)=CO2(g);ΔH=-3935kJ·mol-1
②2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);ΔH=+141kJ·mol-1则
(1)TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(2)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2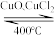 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.此条件下反应A中,4molHCl被氧化,放出115.6kJ的热量。
ⅱ.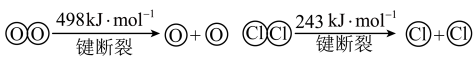
(2)写出该条件下,反应A的热化学方程式为_______ 。
(3)断开1molH-O键与断开1molH-Cl键所需能量相差约为_______ kJ。
(3)利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
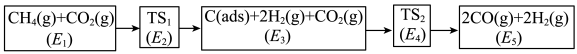
说明:C(ads)为吸附性活性炭,E表示方框中物质总能量(单位:kJ/mol),TS表示过渡态。
(4)制备合成气总反应的 可表示为
可表示为_______ kJ·mol-1。
(5)若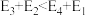 ,则决定速率步骤的化学方程式为
,则决定速率步骤的化学方程式为_______ 。
(1)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
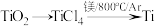
已知:①C(s)+O2(g)=CO2(g);ΔH=-3935kJ·mol-1
②2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);ΔH=+141kJ·mol-1则
(1)TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
(2)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2
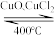 2Cl2+2H2O
2Cl2+2H2O已知:ⅰ.此条件下反应A中,4molHCl被氧化,放出115.6kJ的热量。
ⅱ.
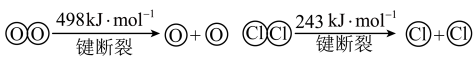
(2)写出该条件下,反应A的热化学方程式为
(3)断开1molH-O键与断开1molH-Cl键所需能量相差约为
(3)利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
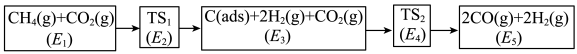
说明:C(ads)为吸附性活性炭,E表示方框中物质总能量(单位:kJ/mol),TS表示过渡态。
(4)制备合成气总反应的
 可表示为
可表示为(5)若
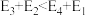 ,则决定速率步骤的化学方程式为
,则决定速率步骤的化学方程式为
您最近一年使用:0次



