解题方法
1 . 高铁酸盐( )被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
)被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
(1)KClO饱和溶液与 饱和溶液反应可制备K2FeO4,反应的离子方程为
饱和溶液反应可制备K2FeO4,反应的离子方程为___________ 。
(2)聚合硫酸铁[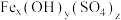 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用 的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
通过计算确定该聚合硫酸铁的化学式_______ (写出计算过程)。
 )被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
)被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。(1)KClO饱和溶液与
 饱和溶液反应可制备K2FeO4,反应的离子方程为
饱和溶液反应可制备K2FeO4,反应的离子方程为(2)聚合硫酸铁[
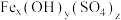 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用
 的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。通过计算确定该聚合硫酸铁的化学式
您最近一年使用:0次
2 . 一定温度下,体积为2L的密闭容器中装有4molSO2和2molO2,发生反应2SO2+O2 2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:
2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:
(1)2min末SO3的浓度是___________ ;
(2)2min内SO2的平均反应速率是___________ 。
(3)2min内O2的转化率是___________ 。
(4)该温度下的平衡常数为K=___________ L·mol-1。(计算结果)
 2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:
2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:(1)2min末SO3的浓度是
(2)2min内SO2的平均反应速率是
(3)2min内O2的转化率是
(4)该温度下的平衡常数为K=
您最近一年使用:0次
解题方法
3 . 回答下列问题:
(1)0.1 mol/l HCl溶液和0.05 mol/L H2SO4溶液等体积混合,pH=_______ 。
(2)在25℃下,将pH=3的强酸溶液和pH=12强碱溶液混合,当混合溶液的pH=11时,强酸溶液和强碱溶液的体积比是_______ 。
(3)某温度(t℃) 时,测得0.01 mol/L的NaOH溶液的pH=11,则该温度下水的Kw=_______ 。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合。
①若所得混合液为中性,且a=12,b=2,则Va:Vb=_______ 。
②若所得混合液为中性,且a+b=12,则Va:Vb=_______ 。
③若所得混合液的pH=10,且a=12,b=2,则Va:Vb=_______ 。
(1)0.1 mol/l HCl溶液和0.05 mol/L H2SO4溶液等体积混合,pH=
(2)在25℃下,将pH=3的强酸溶液和pH=12强碱溶液混合,当混合溶液的pH=11时,强酸溶液和强碱溶液的体积比是
(3)某温度(t℃) 时,测得0.01 mol/L的NaOH溶液的pH=11,则该温度下水的Kw=
①若所得混合液为中性,且a=12,b=2,则Va:Vb=
②若所得混合液为中性,且a+b=12,则Va:Vb=
③若所得混合液的pH=10,且a=12,b=2,则Va:Vb=
您最近一年使用:0次
4 . 将10.6gNa2CO3粉末投入500mL一定浓度的硫酸溶液中,恰好完全反应。求:
(1)标准状况下收集到CO2气体体积为___________ 。
(2)硫酸溶液的物质的量浓度为___________ 。
(1)标准状况下收集到CO2气体体积为
(2)硫酸溶液的物质的量浓度为
您最近一年使用:0次
5 . 常温时,用石墨电极电解500mLNaCl和CuSO4混合溶液,当电路中通过2mol电子时,两极均产生标准状况下16.8L气体,其中阳极产生的O2在标准状况下是5.6L(假定产生的气体全部放出,电解前后溶液体积变化忽略不计),求:
(1)原溶液中c(NaCl)=___________ ,c(CuSO4)=___________ 。
(2)电解后溶液的c(OH-)=___________ 。
(1)原溶液中c(NaCl)=
(2)电解后溶液的c(OH-)=
您最近一年使用:0次
6 . 用铂作电极电解1000mL 0.1mol/L AgNO3溶液,通电一段时间后关闭电源,测得溶液的质量减少了13.4g。请回答:
(1)写现电解过程中阴极反应的电极反应式___________ 。
(2)电解过程中流经外电路的电子数目为___________ 。
(3)加入___________ 使电解液彻底复原(填具体物质及其物质的量)。
(1)写现电解过程中阴极反应的电极反应式
(2)电解过程中流经外电路的电子数目为
(3)加入
您最近一年使用:0次
23-24高二下·全国·课前预习
7 . 某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.16%,氢的质量分数为13.14%。则:
(1)氧的质量分数为___________ 。
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈___________ 。
(3)该未知物A的实验式为___________ 。
(1)氧的质量分数为
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈
(3)该未知物A的实验式为
您最近一年使用:0次
解题方法
8 . 常温下,将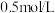 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以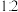 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与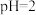 的某一元弱酸溶液
的某一元弱酸溶液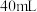 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液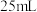 ,试求:
,试求:
(1) 溶液的物质的量浓度为
溶液的物质的量浓度为______  。
。
(2)该一元弱酸的物质的量浓度为______  。
。
(3)此条件下该一元弱酸的电离度为______ 。
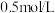 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以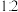 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与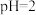 的某一元弱酸溶液
的某一元弱酸溶液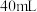 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液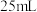 ,试求:
,试求:(1)
 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(2)该一元弱酸的物质的量浓度为
 。
。(3)此条件下该一元弱酸的电离度为
您最近一年使用:0次
9 . 利用化学反应为人类提供能量,研究反应中的能量变化意义重大。
(1) 和
和 可发生反应
可发生反应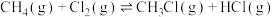 ,部分反应进程如图所示。
,部分反应进程如图所示。
___________  。
。
②图中第1步基元反应为___________ ;第2步反应的活化能为___________  。
。
(2)某实验小组用50mL配制好的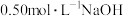 溶液和
溶液和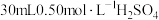 溶液进行中和反应热的测定。
溶液进行中和反应热的测定。___________ (填仪器名称)。
②实验中硫酸溶液相对NaOH溶液是过量的,目的是___________ 。
③实验数据如表所示:
近似认为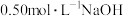 溶液和
溶液和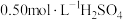 溶液的密度都是
溶液的密度都是 ,中和后混合溶液的比热容
,中和后混合溶液的比热容 ,则
,则
___________  (结果精确至0.1)。
(结果精确至0.1)。
(3)联氨(又称肼, ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
①已知12.8g的液态联氨在氧气中燃烧,生成气态 和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式
和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式___________ 。
②已知:a.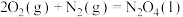

b.

c.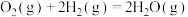

d.

上述反应热效应之间的关系式为
___________ 。
(1)
 和
和 可发生反应
可发生反应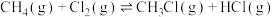 ,部分反应进程如图所示。
,部分反应进程如图所示。

 。
。②图中第1步基元反应为
 。
。(2)某实验小组用50mL配制好的
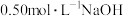 溶液和
溶液和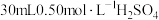 溶液进行中和反应热的测定。
溶液进行中和反应热的测定。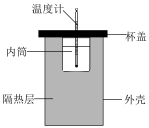
②实验中硫酸溶液相对NaOH溶液是过量的,目的是
③实验数据如表所示:
| 温度 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | ||
 溶液 溶液 | NaOH溶液 | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
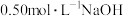 溶液和
溶液和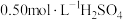 溶液的密度都是
溶液的密度都是 ,中和后混合溶液的比热容
,中和后混合溶液的比热容 ,则
,则
 (结果精确至0.1)。
(结果精确至0.1)。(3)联氨(又称肼,
 ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。①已知12.8g的液态联氨在氧气中燃烧,生成气态
 和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式
和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式②已知:a.
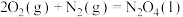

b.


c.
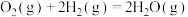

d.


上述反应热效应之间的关系式为

您最近一年使用:0次
名校
10 . 某有机物X(分子组成可表示为CxHyOz)是生物体的一种代谢产物,在不同的生命体中发挥不同的功能。现对X进行相关实验:
①取纯净的X固体9.0g(不含结晶水),控制在125℃~150℃缓慢加热,将其完全转化为蒸气,所得X气体所占体积为2.24L(已折算成标准状况);
②取纯净的X固体18.0g(不含结晶水),迅速加热到190℃以上,使其完全分解,得到三种气体产物;
③将分解产物依次通过足量浓硫酸和无水硫酸铜固体,浓硫酸增重3.6g,无水硫酸铜不显蓝色;
④将剩余的气体8.96L(已折算成标准状况)通过足量澄清石灰水,有白色沉淀生成,最后剩余的气体在装置末端可以被点燃;
⑤被点燃的尾气产生蓝色火焰,用干冷的烧杯罩在火焰上方没有水雾产生,用涂有澄清石灰水的烧杯罩在火焰上方有浑浊。
回答下列问题:
(1)有机物X的摩尔质量为___________ ;X分解产物的化学式为___________ 。
(2)通过计算推导出X的分子式(写出计算过程)___________ 。
(3)取0.5g含有杂质的X固体,溶于水配成25.00mL溶液,取所配溶液于锥形瓶中,加入少量硫酸酸化,用KMnO4溶液滴定至X恰好全部氧化成二氧化碳,共消耗0.002mol 的KMnO4.(MnO 转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为___________ 。
①取纯净的X固体9.0g(不含结晶水),控制在125℃~150℃缓慢加热,将其完全转化为蒸气,所得X气体所占体积为2.24L(已折算成标准状况);
②取纯净的X固体18.0g(不含结晶水),迅速加热到190℃以上,使其完全分解,得到三种气体产物;
③将分解产物依次通过足量浓硫酸和无水硫酸铜固体,浓硫酸增重3.6g,无水硫酸铜不显蓝色;
④将剩余的气体8.96L(已折算成标准状况)通过足量澄清石灰水,有白色沉淀生成,最后剩余的气体在装置末端可以被点燃;
⑤被点燃的尾气产生蓝色火焰,用干冷的烧杯罩在火焰上方没有水雾产生,用涂有澄清石灰水的烧杯罩在火焰上方有浑浊。
回答下列问题:
(1)有机物X的摩尔质量为
(2)通过计算推导出X的分子式(写出计算过程)
(3)取0.5g含有杂质的X固体,溶于水配成25.00mL溶液,取所配溶液于锥形瓶中,加入少量硫酸酸化,用KMnO4溶液滴定至X恰好全部氧化成二氧化碳,共消耗0.002mol 的KMnO4.(MnO
 转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
您最近一年使用:0次
2024-02-24更新
|
149次组卷
|
2卷引用:浙江省宁波市北仑中学2023-2024学年高二下学期期中考试化学试题



